Av & VV förseningar
1. Grundläggande begrepp
- grundläggande begrepp : av-fördröjning och VV-fördröjningsoptimering
- av-fördröjningsoptimering
- VV-fördröjningsoptimering
- lv-pacing ensam eller biventrikulär pacing ?
- AdaptivCRT-algoritm
biventrikulär resynkronisering ger signifikant klinisk fördel, en omvänd ombyggnad med minskning av hjärtvolymen och en minskning av sjuklighet och dödlighet hos patienter med hjärtsvikt med bred QRS. Huvudbegränsningen för denna terapi är att alla studier fann en betydande andel patienter som inte svarar positivt på resynkroniseringsterapin. Olika tillvägagångssätt har föreslagits för att minska andelen icke-svarande. När patienten har implanterats kan en suboptimal justering av CRT-enheten bidra till att ändra kvaliteten på svaret. Principen för CRT är att ändra aktiveringssekvensen hos en patient med elektrisk ledningsstörning genom att justera aktiveringsfördröjningarna mellan en höger atriell ledning, en höger ventrikulär ledning och en vänster ventrikulär ledning. Två programmerbara parametrar är tillgängliga i detta sammanhang: 1) av-fördröjningen som bestämmer aktiveringstiden mellan höger atrium och höger ventrikel, med oberoende programmering av en detekterad av-fördröjning (efter detektering av en spontan atriell (som cykel-BV)) och en tempo av-fördröjning efter en atriell takt (AP-cykel BV). Det är möjligt att programmera en variabel av-fördröjning med en linjär reduktion av av-fördröjningen parallellt med ökningen av hjärtfrekvensen; 2) VV-fördröjningen reglerar aktiveringsfördröjningen mellan höger ventrikel och vänster ventrikel; samtidig aktivering (VV-fördröjning till 0), en höger föraktivering (RV Kazakh LV, X ms) eller en vänster föraktivering (lv Kazakh RV, X ms) är programmerbara; det är inte möjligt att programmera en variabel VV-fördröjning med olika värden i vila och under träning. Akuta hemodynamiska studier har tydligt visat en signifikant fördel som tillhandahålls av optimeringen av av-och / eller VV-fördröjningen. Den kliniska demonstrationen av denna fördel är mycket mindre övertygande.
av-FÖRDRÖJNINGSOPTIMERING
den atriella sammandragningen bidrar till 20-30% av hjärtutgången i vila hos hjärtsvikt patienter med systolisk dysfunktion, detta bidrag ökar under träning. Hjärtsvikt patienter med elektrisk ledningsstörning visar ofta atrioventrikulär asynkroni med en förkortning av fyllningstiden, en sammanslagning av E och A vågor och diastolisk mitral regurgitation.
hos resynkroniserade patienter möjliggör programmering av en kort av-fördröjning att förutse E-vågen, en dissociation av E-och A-vågor och förlängning av fyllningstiden. Av-fördröjningen bör inte ställas in för kort eftersom detta skulle resultera i amputation av A-vågen genom mitralförslutning. Justering av av-fördröjningen rekommenderas efter implantation av en CRT-pacemaker eller defibrillator även om nivån på kliniska bevis är blygsam.
det finns stora interindividuella variationer i intra-atriell ledning och intra-ventrikulära störningar som genererar markanta skillnader i termer av optimal av-fördröjning som motiverar teoretiskt ett skräddarsytt tillvägagångssätt för varje patient. De avkända och paced av-förseningarna är oberoende programmerbara och måste också optimeras oberoende. En begränsning av optimeringen av av-fördröjningen är att den vanligtvis utförs i vila i ryggläge och för en given hjärtfrekvens. Dessa förhållanden skiljer sig avsevärt från de som observeras i vardagen. Under träning, till skillnad från patienter med friskt hjärta där den optimala av-fördröjningen förkortas med ökande hjärtfrekvens, verkar det som att resynkroniserade patienter som svarar på stress inte är stereotypa. Hos vissa patienter är den optimala av-fördröjningen under träning längre än i vila, hos andra är den kortare. Den systematiska användningen av den automatiska av-fördröjningsalgoritmen säkerställer förmodligen kontinuerlig fångst under träning men är inte nödvändigtvis förknippad med en ytterligare hemodynamisk fördel. Därför bör dess programmering diskuteras för varje patient. Biventrikulär resynkronisering möjliggör omvänd ombyggnad med en progressiv minskning över tiden av det tele-systoliska och slutdiastoliska volymsandtrycket. Därför bör optimeringen av av-fördröjningen helst upprepas regelbundet.
den optimala av-fördröjningen möjliggör ett maximalt bidrag av vänster atriell sammandragning till vänster ventrikulär fyllning, förlänger fyllningstiden, förbättrar hjärtutgången i frånvaro av diastolisk mitral regurgitation.
om av-fördröjningen är inställd för lång, inträffar förmakskontraktionen för tidigt i diastolen, vilket begränsar förmaksbidraget till ventrikulär fyllning. Den atriella sammandragningen överlagras med den initiala diastoliska fasen. Hjärtekokardiografi finner en fusion mellan e-våg och en våg och en kort fyllningstid med en ihållande diastolisk mitral regurgitation.
om av-fördröjningen är inställd för kort inträffar den ventrikulära sammandragningen för tidigt vilket resulterar i för tidig mitralförslutning som avbryter den aktuella fyllningen och begränsar förmaks bidrag till ventrikulär fyllning. Ekokardiografin finner en för tidig e-våg, en lång fyllningstid och dela E och A-vågor med en stympad a-våg genom mitralförslutningen. Minskningen i slutdiastoliskt tryck och den minskade förbelastningen leder till en minskning av dP / dt max och hjärtutgången.
innan du startar av-fördröjningsoptimeringen måste vissa element vara kända. Hos patienter med fullständigt atrioventrikulärt block och höggradigt AV-block eller med ett mycket långt PR-intervall kommer förändringar i av-fördröjning inte att ha någon direkt effekt på graden av ventrikulär infångning och fusion. Däremot kommer förlängning av av-fördröjningen hos patienter med bevarad atrioventrikulär ledning att orsaka en progressiv fusion med spontan aktivering. Justering av av-fördröjningen måste utföras under elektrokardiografisk kontroll genom att integrera tanken att i gruppen av patienter utan fullständigt AV-block, som representerar majoriteten av patienterna, kommer av-fördröjningen att variera fördröjningen mellan atriell systole och ventrikulär systole men kommer också direkt att störa den ventrikulära aktiveringssekvensen och graden av ventrikulär fusion. För att övervinna denna svårighet programmeras av-fördröjningen ofta systematiskt kort (mellan 90 och 120 ms efter en avkänd atriell aktivitet och mellan 130 och 150 ms efter atriell stimulering).
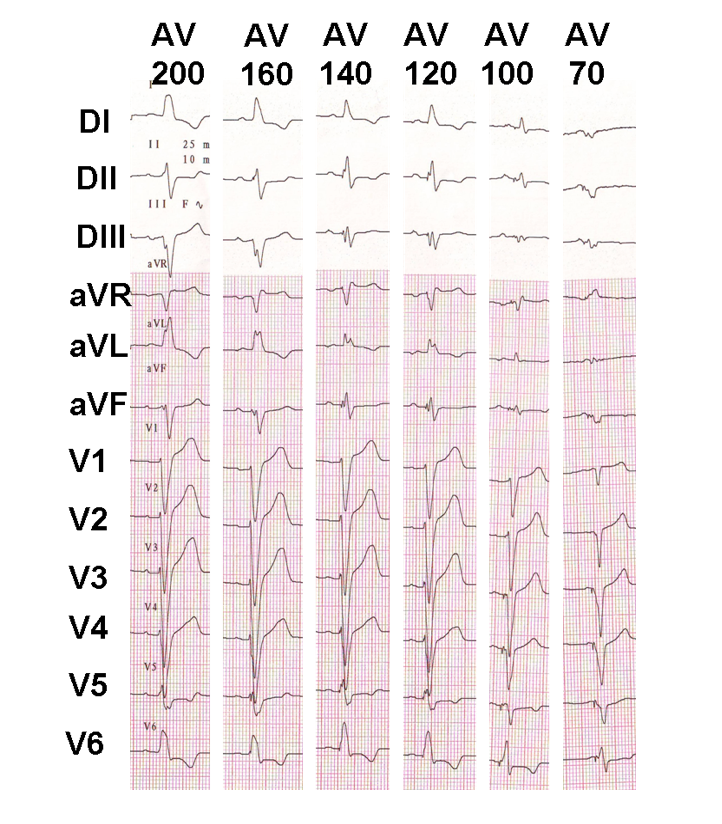
exempel på progressiv av-fördröjningsjustering hos en resynkroniserad patient med bevarad AV-ledning; progressiv fusion visas med förlängningen av av-fördröjningen.
olika tekniker har föreslagits för att optimera av-fördröjningen:
- ekokardiografi
olika ekokardiografiska metoder har föreslagits för att optimera av-fördröjningen: Ritter-metoden (som inte har validerats i en population av patienter med hjärtsvikt), sökandet efter en maximal aorta-eller mitral VTI, en maximal dP / dt max och den iterativa metoden. Den senare används ofta i klinisk praxis, målet är att få den längsta fyllningstiden utan amputation av A-vågen baserad på trans-mitralflödesanalys. - andra metoder
olika uppskattningar av hjärtkontraktilitet eller hjärtutgång kan användas: vågpuls, blodtryck, dP / dt max, elektrokardiografiskt utseende … Den kliniska tillämpligheten i daglig praxis är ofta begränsad. - automatisk optimeringsalgoritm inbäddad i enheten
om upprepade optimeringar av av-fördröjning är nödvändiga och måste göras under olika förhållanden för förbelastning, skulle den ideala lösningen vara att pacemakern inser det själv. AdpativCRT-funktionen är tillgänglig i den senaste generationen av Medtronic defibrillatorer; driftsprinciperna för denna nya algoritm kommer att diskuteras i slutet av detta kapitel.
VV-FÖRDRÖJNINGSOPTIMERING
vissa patienter svarar inte på CRT och fortsätter att visa en signifikant mekanisk ventrikulär dyssynkroni efter implantation. Justering av VV-fördröjningen resulterar i sekventiell biventrikulär pacing och har en direkt inverkan på sekvensen av ventrikulär aktivering. Modifiering av VV-fördröjningen kan föreslås för att minska den ihållande asynkronin hos patienter som inte svarar. Denna parameter verkar intressant i teorin hos patienter med en suboptimal position av LV-ledningen, eller en latens och en förlängd ledningstid vid stimuleringsstället. Om optimeringen av VV-fördröjning möjliggör signifikant akut hemodynamisk fördel, är frågan om den kliniska relevansen av denna parameter fortfarande debatterad och inte bekräftad av kliniska studier. När det gäller inställning av av-fördröjning är det troligt att ombyggnadsprocessen direkt påverkar optimeringen av VV-fördröjning och att optimeringen av denna parameter måste upprepas över tid och under olika förbelastningsförhållanden.
samma verktyg kan användas för att optimera av-och VV-fördröjning. Hjärtekokardiografi används ofta i klinisk praxis. Aorta VTI som återspeglar hjärtutgången, dP/dt max som återspeglar hjärtkontraktiliteten eller mätningen av graden av ventrikulär asynkroni används mest. Återigen föreslår AdaptivCRT-funktionen att automatiskt optimera VV-fördröjningen. Mot bakgrund av de praktiska gränserna för VV-optimeringen ser den upprepade automatiska justeringen av denna parameter av själva enheten lovande ut. Det är dock fortfarande nödvändigt att visa sin kliniska relevans.
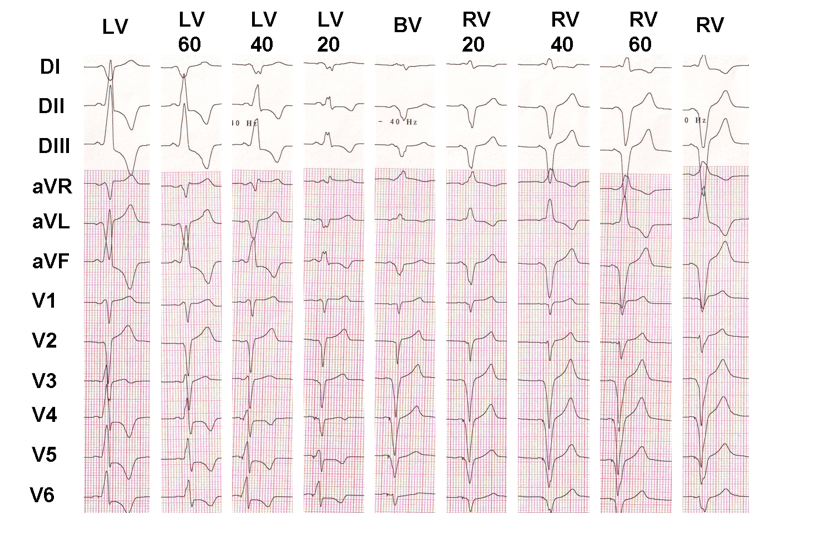
detta exempel visar effekten av VV-fördröjning på den ventrikulära elektriska aktiveringen; om det är lätt att visa att det elektrokardiografiska utseendet faktiskt skiljer sig från en konfiguration till en annan, är det mycket svårare att avgöra vilken konfiguration som ger det bästa kliniska svaret.
LV PACING ensam eller biventrikulär PACING ?
en av driftsprincipen för AdaptivCRT-algoritmen består i att välja mellan vänster ventrikulär med fusion och biventrikulär pacing.
ingen studie har någonsin visat överlägsenhet av biventrikulär pacing på en ren vänster ventrikulär stimulering. Däremot har akuta hemodynamiska studier konsekvent funnit betydande fördelar med isolerad vänster ventrikulär pacing. På liknande sätt fann kliniska studier en fördel som var mer eller mindre identisk när det gäller NYHA-klass, träningskapacitet och ventrikulär ombyggnad till de som observerades med biventrikulär pacing. Ändå utfördes stora studier som visade fördelarna med resynkronisering med biventrikulär stimulering och inte med vänster ventrikulär stimulering.
i lv-pacingkonfiguration kan resynkroniseringen av de två ventriklarna erhållas genom fusion mellan vänster ventrikulär paced aktivering av den högra ventrikelns inneboende aktivering. Om det verkar som om den optimala akuta hemodynamiska nyttan kan erhållas med en viss grad av fusion (begränsade data på ett mycket begränsat antal patienter) är denna optimala grad av fusion svår att definiera och upprätthålla under träning (förändringar i hjärtfrekvens och PR-intervall).
isolerad vänster ventrikulär pacing är ett attraktivt alternativ, särskilt om den implanterade enheten är en CRT-pacemaker. Faktum är att det kan utföras med hjälp av en konventionell dubbelkammarpacemaker utan implantation av höger ventrikulär bly vilket ökar förhållandet mellan kostnad och effektivitet och minskar risken för komplikationer. I AV-block pacemakerberoende patienter verkar emellertid implantering av endast en vänster ventrikulär ledning riskabel med tanke på den högre andelen blyförlust och hög stimuleringströskel. Hos patienter implanterade med en CRT-defibrillator är implantationen av en höger ventrikulär ledning nödvändig. Programmering av enheten i en ”endast lv-stimulering” – konfiguration undviker emellertid förbrukningen i samband med höger ventrikulär stimulering.
ADAPTIV – CRT-algoritm
som tidigare sett är idealet för upprepade optimeringar av pacingkonfigurationen att enheten själv utför detta automatiskt. Denna optimeringsprocedur har inga extra kostnader och är ”enkel” för läkaren och de olika kliniska avdelningarna (ekokardiografi, elektrofysiologi…). Dessutom är majoriteten av mätningarna gjorda av anordningen reproducerbara. Optimeringsalgoritmen AdaptivCRT utvecklades med detta mål. Demonstrationen av dess gynnsamma kliniska inverkan på resynkroniserade patienter förblir emellertid obevisad.
driftsprinciper
adaptivcrt-algoritmen är endast tillgänglig i DDD-eller DDDR-läge och kan programmeras på genom att välja antingen: 1) inställningen” Adaptive Bi-V ”- enheten optimerar automatiskt pacingparametrarna (av – och VV-förseningar) – eller 2) inställningen” Adaptive Bi-V och LV ” – enheten väljer mellan en ren lv-pacingkonfiguration med fusion och en vanlig biventrikulär pacing med optimering av av-och VV-förseningarna. Denna algoritm kan också stängas av genom programmering 3) ”Nonadaptive CRT”.
denna algoritm leder aldrig till användning av extrema värden för av-eller VV-förseningar. För AdaptivCRT-funktion varierar möjliga avkända av-fördröjningar mellan 80 ms och 140 ms. Möjliga paced av-förseningar varierar mellan 100 ms och 180 ms. tidsintervallet för intraventrikulära VV-förseningar varierar från 0 ms till 40 ms (vänster eller höger pre-excitation).
AdaptivCRT-funktion är beroende av regelbunden utvärdering av 1) den atrioventrikulära ledningstiden, vilket motsvarar fördröjningen mellan EGM inspelad av höger förmaksledningen och EGM inspelad av höger ventrikulär ledning; 2) bredden på P-vågen, vilket motsvarar fördröjningen mellan den atriella EGM inspelad på den bipolära kanalen i den högra atriella ledningen och änden av den atriella EGM inspelad av chockkanalen; 3) bredden på QRS-komplexet som motsvarar fördröjningen mellan EGM detekterad av den högra ventrikulära bipolen och änden av EGM inspelad på chockkanalen.
algoritmen bedömer patientens inneboende atrioventrikulära ledning varje minut och bestämmer om patientens av-intervall är normalt eller förlängt. Av-intervallmätningen utförs genom att förlänga den avkända och tempo av-fördröjningen till 300 ms för att möjliggöra inneboende ledning. I avsaknad av spontan genomförd ventrikulär händelse i mer än 3 på varandra följande cykler diagnostiseras en långvarig av-ledning och tidsintervallet mellan av-intervallmätningar fördubblas (till exempel 2 min, 4 min, 8 min… och så vidare tills max 16 timmar uppnås).
p-vågens och QRS-breddmätningarna planeras var 16: e timme. Detta intervall garanterar ett urval vid olika tidpunkter på dagen. Under mätningen växlar enheten inspelningskanalen EGM 1 till RV-spole (HVA)/ SVC-spole (HVB) (eller HVA/förmaksanod i frånvaro av SVC-spole). Efter 5 slag mäts fördröjningen mellan atriella och ventrikulära EGMs, bredden på P-vågen och bredden på QRS.
den första mätningen av P-vågen och QRS-bredden är planerad 30 minuter efter implantatet. Efter implantation kan P-vågen och QRS-bredden mätas när som helst genom att programmera parametern AdaptivCRT.
om AdaptivCRT-parametern är inställd på ”Adaptive Bi-V och LV” kan den växla automatiskt mellan auto BIV och LV-läget. Patienten kommer att stimuleras i rent LV-läge om följande villkor respekteras: 1) patientens hjärtfrekvens måste vara mindre än eller lika med 100 bpm; 2) ledningsfördröjningen mellan det spontana atriella EGM och det spontana ventrikulära EGM måste vara mindre än eller lika med 200 ms; 3) ledningsfördröjningen mellan det tempo atriella EGM och det spontana ventrikulära EGM måste vara mindre än eller lika med 250 ms.
om ett av dessa kriterier inte hittas stimuleras patienten i ett biventrikulärt läge.
detaljer om algoritmens funktionsfunktion
den exakta funktionen för denna algoritm är relativt konfidentiell.
i ett första steg bedömer enheten inneboende ledning för att avgöra om en patients av-intervall är normalt eller förlängt. Normala av-intervall definieras som mindre än 200 ms för förmaksavkända intervall och mindre än 250 ms för förmaksintervall.
i närvaro av en normal av-ledningstid och om patientens hjärtfrekvens är under 100 bpm, kommer enheten att använda det Adaptativa lv-pacingläget (endast LV-pace). Tidpunkten för LV-takten justeras automatiskt baserat på den inneboende av-intervallmätningen som sker varje minut.
om patientens av-ledningstid överstiger 133, 3 ms uppträder LV-stimuleringen vid cirka 70% av det inneboende av-intervallet.
Om av-ledningstiden är sämre än 133,3 ms, kommer LV – stimuleringen att levereras 40 ms före den inneboende QRS (beräknad av-fördröjning-40 ms).
När inneboende av-intervall förlängs, eller när patientens hjärtfrekvens är över 100 bpm, eller om en förlust av lv-infångning bekräftas av lv capture management (LVCM), kommer det adaptiva BiV-läget att fungera.
av-fördröjningen beräknas sedan enligt följande:
- efter en avkänd förmakshändelse justeras av-fördröjningen till takt 40 ms efter slutet av P-vågen (mätt på chockkanalen) men minst 50 ms före början av den inneboende QRS.
- efter en paced atrial händelse justeras av-fördröjningen till takt 30 ms efter slutet av P-vågen (mätt på chockkanalen) men minst 50 ms före starten av den inneboende QRS under förmakspacing (timing mellan förmaksstimulans och bipolär höger ventrikulär EGM).
under adaptiv BiV-pacing dras den optimala VV-fördröjningen från QRS-bredden.
om QRS-varaktigheten (timing mellan bipolär RV-EGM och slutet av QRS-EGM på chockkanalen) ingår mellan 50 ms och 150 ms, kommer LV att vara upphetsad. Om QRS-bredden ingår mellan 150 och 180 ms, ställs en höger ventrikulär pre-excitation in. Om QRS-bredden inte ingår mellan 50 och 180 ms, a lv eller RV pre-excitation av 10 ms kommer att användas.
av-ledningstiderna och p-vågbredden kommer också att användas för att optimera VV-fördröjningen. Om av-ledningstiden under spontan förmaksrytm är längre än P-vågbredden, kommer VV-fördröjningen att ställas in på 0 ms.