Cellbiologi 07: mikrotubuli och celldelning
dessa är anteckningar från föreläsning 7 i Harvard Extension Cell Biology course.
föreläsning 6 introducerade mikrotubuli, och denna föreläsning kommer att diskutera deras roll i celldelning. Här är en introduktionsvideo:
översikt över cellcykeln
cellcykeln – processen för celldelning och replikering-styrs av en serie biokemiska omkopplare som kallas cellcykelstyrsystemet.
cellcykeln är uppdelad i faser som är indelade i faser – människor kommer att hänvisa till ”4 faser” men då finns det faktiskt 5, och människor använder också andra ord för att gruppera dessa faser tillsammans och andra ord för att dela upp dem. Jag har gjort mitt bästa för att sammanfatta förhållandet mellan dessa termer i följande tabell. (ändrad / utökad från Wikipedia):
| MOST general grouping | the supposed ”4 phases” | subphases |
|---|---|---|
| non-dividing | Gap 0 (G0) | |
| interphase | Gap 1 (G1) | G1a R G1b |
| Synthesis (S) | ||
| Gap 2 (G2) | ||
| Mitosis | Mitosis (M) | prophase prometaphase metaphase anaphase telophase cytokinesis |
The innehållet i varje fas sammanfattas vackert i denna enastående Wikimedia Commons-bild av Kelvinsong:

de snabbast delande mänskliga cellerna kan slutföra en cellcykel på cirka 24 timmar (G1: 9h, S: 10h, G2: 4h, M: 30 min). Jäst kan avsluta en cykel på 30 minuter, och de snabbast delande Drosophila-cellerna tar så lite som 8 minuter.
huvudkontroller av denna process inkluderar cyklinerna, som reglerar cyklinberoende Kinas eller CDK. Minns att kinaser är proteiner som fosforylerar andra proteiner. CDK: s fosforylering av dess mål gör det möjligt för mitos att fortsätta. För att vara exakt är mognadsfrämjande faktor eller MPF ett obligatoriskt heterodimeriskt komplex bestående av cyklin B och CDK, som endast gör sin fosforyleringsverkan när båda proteinerna är närvarande.
roll av mikrotubuli
mikrotubuli är kritiska under hela cellcykeln – de organiserar cellulära komponenter och delar dem i två. Här är en serie videor av cellcykeln som lyfter fram mikrotubulernas Roll:
hos djur har vilande celler och till och med celler i interfas vanligtvis bara en MTOC, kallad en centrosom, som fungerar som det centrala navet för alla mikrotubuli i cellen. En centrosom består av två centrioler som visas nedan (tack igen till Kelvinsong):

de två centriolerna lossnar från varandra och replikerar sig under S-fasen och separeras sedan för att bilda motsatta”poler”i cellen under M-fasen, så att det nu finns två MTOCs, som var och en så småningom kommer att vara den enda MTOC i en ny cell (en annan boss Kelvinsong-bild):
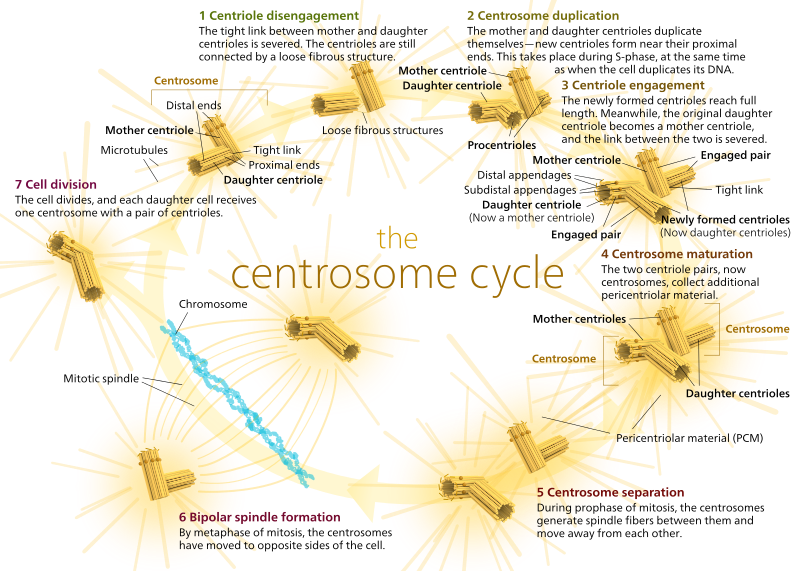
under mitos har du de två”polerna”i cellen, var och en med mikrotubuli förankrade vid (-) änden och med deras (+) ändar överlappande, pekar in i mitten av cellen, som visas här (Wikimedia Commons-bild av Lordjuppiter):
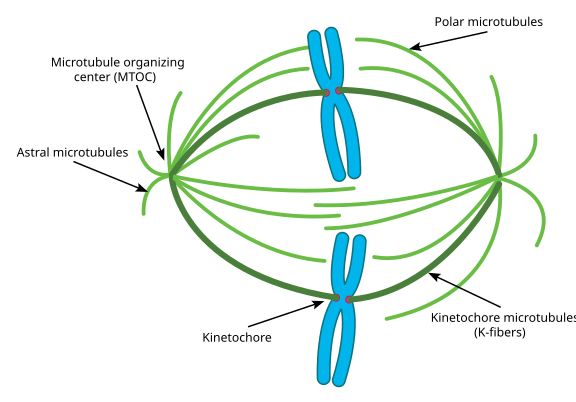
det hela kallas en spindelapparat, och området där de två Mtoc: erna’ mikrotubuli överlappar kallas ’interdigitationszonen.’Du kommer ibland att höra varje MTOC och dess urchin-liknande uppsättning mikrotubuli som kallas en ’mitotisk aster.’
mikrotubuli under detta steg sägs falla i tre kategorier:
- astrala mikrotubuli pekar utåt, mot cellbarken, för att förankra hela spindelapparaten längs celldelningens axel.
- Kinetochore mikrotubuli fäster vid kinetochore av kromatider.
- polära mikrotubuli, orienterade parallellt med varandra men i motsatta riktningar, är avgörande för att skjuta spindelapparaten isär under mitos. (I själva verket är polära mikrotubuli också närvarande tidigare och hjälper till att skjuta centrosomerna isär under profas).
om du föredrar foton framför diagram, så ser hela spindelapparaten ut, med kromatider i blått, mikrotubuli i grönt och kinetochorerna som röda prickar:

mikrotubuli blir mycket mer dynamiska under mitos: mer gamma-tubulin främjar lättare kärnbildning, men XMAP215, en mikrotubul stabilisator, fosforyleras och inaktiveras därmed under mitos, vilket gör att Kinesin-13 är fri att katastrofera mikrotubuli. Förmögenheter görs och förloras snabbt. Halveringstiden för en mikrotubuli under mitos är cirka 15 minuter, jämfört med 30 minuter under interfas. Människor studerar mikrotubuldynamiken med FRAP: Lägg till en fluorescerande mikrotubuli, bleka den och se hur snabbt återmontering sker baserat på hur snart fluorescens återkommer. + Tips spelar också en viktig roll för att hjälpa och montera mikrotubuli.
Kinesin-5 IS har två polära huvuden som binder till motsatta mikrotubuli och försöker gå mot (+) slutet av varje. Detta skjuter de två mikrotubuli isär och ger drivkraften för separation av MTOCs.
Centromeriskt DNA har låg information entropi och speciella histoner som skiljer sig från andra kromatin. Centromerer är en del av genomet som du nästan aldrig tar upp i nästa gensekvensering, även vid riktigt högt djup. Det beror på att centromerer tjänar ett annat syfte än mycket av resten av genomet: sekvensen där är gynnsam för interaktion med centromera proteiner och kinetochore-bindning. Kohesiner är proteiner som håller de två systerkromatiderna tillsammans. Vi kommer att hänvisa till kinetochore proteiner som har två lager, den inre kinetochore och yttre kinetochore.
under prometafas rör sig kromosomer fram och tillbaka. Kinesiner förankrar kromosomerna till kinetochore-mikrotubuli bortom spetsen där Kinesin-13 depolymeriserar mikrotubuli, med hjälp av brist på tillgängliga tubulindimerer. En kombination av motorproteiner, mikrotubuli-interagerande proteiner och löpband tjänar till att flytta kromosomerna. Under tiden, dynein och dynactin – motoriska proteiner som går mot (-) slutarbetet på astrala mikrotubuli, dra MTOCs mot cellens periferi. I metafas kommer kromatiderna att anpassas längs ’metafasplattan’.
under denna process upplöses kärnhöljet och så blir kärnimport irrelevant. Ran-GEF lokaliserar nära kromosomer och genererar höga koncentrationer av Ran-GTP som ger energi för vissa nödvändiga processer (?).
celler har någon mekanism för att detektera spänningen i mikrotubuli som indikerar deras fästkromatider innan mitos kan fortsätta. Att se till att varje kromatid är ordentligt förankrad är avgörande för att undvika aneuploidi.
förresten spelar andra cytoskeletala element förutom mikrotubuli också en nyckelroll i cellcykeln. I cytokinesis bildar aktin en kontraktil ring och, med hjälp av myosin II-motorproteiner, cinches cellen i två.
betydelsen av modellorganismer
upptäckten av cellcykelreglerande processer förlitade sig starkt på några snygga egenskaper hos populära modellorganismer.
Saccharomyces cerevisiae (spirande jäst) och Schizosaccharomyces pombe (fissionsjäst) kan existera som haploider eller diploider. Det är viktigt eftersom en mutation i den haploida fasen kan slå ut en gen – du behöver inte träffa båda allelerna. Och i jäst är många mutationer, särskilt i Cdc__ (cell division control) gener, temperaturberoende, där ett protein med en missense-mutation fortfarande kan fungera korrekt vid ’tillåtna’ temperaturer men förlorar sin ursprungliga funktion vid ’icke-tillåtna’ temperaturer. Detta gör det möjligt att studera knockout-fenotypen (vid den icke-tillåtna temperaturen) samtidigt som det är bekvämt att enkelt kunna sprida organismerna (vid den tillåtna temperaturen). Hela S. cerevisiae-genomet är tillgängligt som plasmidbibliotek, vilket gör det möjligt att screena för vilken plasmid räddar fenotypen för en given mutant. Det är hur många av de gener som reglerar cellcykeln upptäcktes.
i S. cerivisiae, spirande är en del av fas G1, och när dottercellen når en viss storlek, i ett ögonblick som kallas ”START”, är de två engagerade i att komma in i S och slutligen slutföra cellcykeln. Däggdjursceller har sin egen engagemangspunkt som kallas begränsningspunkten eller R, i G1, som är analog med START.
temperaturkänsliga Cdc28-mutanter knoppar inte vid den icke-tillåtna temperaturen. Cdc28-genen kodar för jästens homolog av vårt cyklinberoende Kinas (CDK) som, när och endast när det är komplext med cyklin, kan fosforylera andra proteiner för att reglera deras deltagande i cellcykelfaser. Temperaturkänsliga mutanter vid den icke-tillåtna temperaturen fastnar inte i knopp och går in i S-fasen. Istället beter de sig som vildtypsceller berövade näringsämnen: de växer tillräckligt stora för att passera START men fortsätter sedan inte.
Xenopus (en slags groda) visade sig vara kritisk för att förstå cellcykeln, eftersom dess reproduktion involverar ett mycket stort antal celler (dvs. tillräckligt utgångsmaterial för västerländska blottar etc.) som är perfekt synkroniserade (dvs alla är i samma fas av cellcykeln i samma ögonblick. (Jämför med jäst, till exempel, där celler inte alla kommer att vara i samma fas samtidigt). Även ägget i sig är stort och lätt att arbeta med, och flera cellcykler följer befruktning. I grodor börjar ägg meiotisk uppdelning men arresteras sedan i G2-fasen i 8 månader medan de växer i storlek och lagrar saker som kommer att behövas för tillväxt vid befruktning.
mellanliggande filament
förutom mikrofilament och mikrotubuli har eukaryota celler också en mängd ’andra’ cytoskeletala proteiner som kallas mellanliggande filament (IFs). Även mer varierande än mikrofilament och mikrotubuli, IFs är inte bara en catch-all term för ’någon annan filament’ – snarare, de är en grupp av besläktade proteiner. De sträcker sig i allmänhet genom cytoplasman och det inre kärnhöljet, är icke-polära och har inga motorproteiner associerade med dem. De har stor draghållfasthet och är mycket stabila, med en långsam växelkurs och inte mycket nedbrytning, även om fosforylering kan främja deras demontering. Här är några populära exempel:
- keratiner finns i epitelceller, mesodermceller och neuroner. De ger styrka och kommer i sura och basiska former. Var och en kan bilda sin egen sträng, men de flesta IFs består av två strängar – en basisk och en sur, som vrids runt varandra. Hår och naglar är gjorda av ’hård’ keratin rik på cystein för disulfidbindningar som ger den enorma styrkan. Perms och rätning är beroende av att minska disulfidbindningarna, omforma håret och sedan reformera disulfidbindningarna. Du har också ’mjuk’ keratin i huden.
- Desminer som vimentin finns i mesenkymala celler (ben, cartiledge och fett).
- Neurofilament finns i neuronala axoner och reglerar diametern därav, vilket i sin tur bestämmer hastigheten för aktionspotentialutbredning.
- laminer är båda de mest utbredda och tros vara mest lik den fylogenetiska förfadern till alla andra IFs. De ger strukturellt stöd för kärnmembranet. De kan hjälpa till att rymma de nukleära porkomplexen och även organisera DNA.
slutligen en sammanfattande video: