Stor granulär Lymfocytleukemi som komplikation av reumatoid artrit / reumatolog Korica cl nica
introduktion
Feltys syndrom (FS) är en sällsynt systemisk komplikation (mindre än 1%) av reumatoid artrit (RA), kännetecknad av triaden av RA, ihållande neutropeni (3
) och splenomegali av varierande storlek som kan sträcka sig från subklinisk splenomegali, endast detekterbar genom avbildning, till massiv1 splenomegali. Det förekommer främst i långvariga fall med svår ledsjukdom och extraartikulära manifestationer och har en stark koppling till HLA-DR4-haplotypen (nästan 95% av fallen).2 hos 30% -40% av patienterna med FS finns en expansion av stora granulära lymfocyter (LGL).1 LGL representerar 10% -15% av cirkulerande mononukleära celler och identifieras morfologiskt av deras stora storlek (15–18 kg), deras runda eller indragna kärna och riklig cytoplasma med azurofila granuler. Fenotypen av dessa celler kan vara cytotoxisk T-lymfocyt (CD8+, CD57+) eller naturlig mördare (NK) (CD3−, CD8−, CD56+).3 när expansion av LGL är monoklonal och är associerad med infiltrering av benmärgen och mjälten av dessa celler kallas den stor granulär lymfocytleukemi (LGLL) och anses vara en kronisk låggradig lymfoproliferativ sjukdom. Dess kliniska presentation liknar den för FS, vilket belyser den ökade mottagligheten för bakterieinfektioner associerade med neutropeni, anemi och splenomegali, som också har kallats ”pseudo-Felty”.3,4 klinisk Presentation
en 70-årig pensionerad arbetare från ett granitbrott diagnostiserades vid 43 års ålder med seropositiv RA med inblandning av händer, fötter, knän och höfter. Han utvecklade därefter pneumokonios och pulmonella reumatoida noduler (Fig. 1), diagnostiseras som Caplans syndrom. Under hans progression behandlades han med NSAID, kortikosteroider, guldsalter, cyklosporin och metotrexat. Trots detta utvecklade patienten strukturella skador i händer, fötter och höfter, vilket krävde placering av protes i båda höfterna vid 51 respektive 54 års ålder. Under de senaste åren förblev hans sjukdom stabil, behandlad med metotrexat 10 mg varje vecka och låga doser glukokortikoider, utan tecken på inflammatorisk ledaktivitet. Han presenterade ’svanhals’ deformiteter i alla fingrar och reumatoida knölar på armbågarna. För 12 månader sedan utvecklade han plötsligt feber och smärta i höger ljumsk, med efterföljande septisk chock, vilket visade en infektion i höger höft av Salmonella spp. Metotrexat och glukokortikoider suspenderades, och han behandlades med långvarig antibiotikabehandling och partiell ersättning av protesen. Laboratorietester visade ihållande neutropeni, trots tillbakadragandet av myelotoxiska läkemedel och förbättring av sepsis, når 0neutrofiler/mm3. Retroaktivt, när han granskade antalet neutrofiler, hade han låga räkningar ett år tidigare, mellan 1800 och 1000 / mm3. Resten av blodantalet och biokemi var normala. ESR var 80 mm/h och CRP 111 mg/l. han upprätthöll höga nivåer av reumatoid faktor (6930u/ml) och anti-CCP (300U / ml) och hade också polyklonal hypergammaglobulinemi. Antinukleära antikroppar och extraherbara nukleära antigener var negativa och komplementnivåerna var inom normala värden. HLA-typning visade att han bar haplotypen DRB1 * 0404 (DR4) och mild splenomegali detekterades (13,7 cm) på bukberäknad tomografi.

pneumokonios och pulmonella reumatoida noduler.
det perifera blodutstryket visade lymfocytos av LGL (Fig. 2), som i immunofenotypen motsvarade 42% av de totala leukocyterna, med en avvikande fenotyp av cytotoxisk T− lymfocyt (CD3+, CD8+, CD5+, CD7+/−, CD4−, CD56-och DR+). Benmärgsbiopsin visade 20% av den totala märgcellulariteten motsvarande samma klonal expansion (bekräftad genom omläggning av den variabla regionen av TCR gamma). Baserat på dessa fynd ställdes en diagnos av LGLL och behandling med metotrexat 15 mg varje vecka återupptogs trots 3 månader med ihållande neutropeni (3
), vilket kräver frekvent administrering av granulopoiesis stimulerande faktorer. Han behandlades därefter med cyklofosfamid, vincristin och prednison vid höga doser. Efter 6 månaders behandling kvarstår neutropeni.
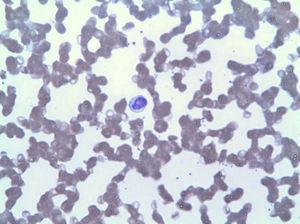
lymfocytos på grund av LGL.
diskussion
LGLL är en kronisk leukemi som kännetecknas av expansion av LGL monoklonal fenotyp av aktiverade cytotoxiska T-lymfocyter eller mindre ofta NK-celler.5 medelåldern för diagnos är 60 år och den är ofta associerad med autoimmuna sjukdomar, särskilt RA, men har också beskrivits i ulcerös kolit, Sjabbiggrens syndrom, lupus erythematosus och multiple1 skleros. Patienter med RA som har associerat LGLL har en klinisk presentation som liknar FS. De är vanligtvis patienter med långvarig RA, allvarlig ledskada och signifikanta konsekvenser och ökad frekvens av extraartikulära manifestationer såsom reumatoida knölar, lymfadenopati, pretibiala sår, pleurit, hudpigmentering, neuropati eller episklerit.6 patienten hade också en annan sällsynt komplikation av RA, reumatoid pneumokonios eller Caplans syndrom, kännetecknad av utseendet av lungknutor med histopatologi som liknar den hos typiska reumatoida knölar hos patienter med en historia av yrkesmässig exponering för oorganiska damm såsom kiseldioxid, kol eller granit.7 Så vitt vi vet är det aktuella fallet det första som beskriver presentationen av Caplans syndrom och LGLL hos samma patient. I de flesta fall är presentationen LGLL svår neutropeni associerad med återkommande bakterieinfektioner. De mikroorganismer som oftast är involverade är Staphylococcus aureus, Streptococcus spp. och gramnegativa baciller. Mindre vanligt anemi, feber, nattsvett och förstoring av lever och mjälte5 kan också följa med det. Upp till en tredjedel av patienterna med LLGG har ingen uppenbar RA klinisk aktivitet vid diagnostidpunkten, men upprätthåller höga nivåer av ESR.6 upp till 40% av patienterna med FS har LGL-lymfocytos.7 detta faktum, tillsammans med den kliniska likheten och associeringen med HLA-DR4, har starkt föreslagit att FS och LGLL associerade med RA är uttryck för samma enhet som kännetecknas av spridningen av LGL.8 andra former inkluderar också mildare former såsom reaktiv lymfocytos och infektioner till mer aggressiva former av NK5 LGLL. Lgll-diagnosen är baserad på upptäckten av en monoklonal expansion av LGL i perifert blod och benmärg med en karakteristisk immunofenotyp (CD3+, CD4−, CD8 +, CD16+, CD28− och CD57+). Klonaliteten bekräftas genom att studera reTCR9-genen. I allmänhet har LGL en kronisk och indolent progression, med en genomsnittlig överlevnad på 10 år.1 i sällsynta fall, särskilt när expansionen beror på LGL med nk-fenotyp, kan denna leukemi uppträda mer aggressivt.5 Den vanligaste indikationen för behandling är återkommande infektioner och, mindre ofta, anemi, symptomatisk splenomegali eller uppkomsten av allvarliga B-symtom B1.
den första linjens behandling i LGLL är immunsuppressiva läkemedel ensamma, specifikt metotrexat (10 mg/vecka), cyklosporin A (1-1, 5 mg/kg/2 gånger dagligen) eller oral cyklofosfamid (50-100 mg/dag). Denna behandling är effektiv hos cirka 50% av patienterna, vilket ger korrigering av cytopenier, men inte utrotar leukemiska celler.1 glukokortikoider kan användas för att påskynda svaret och granulopoiesstimulerande faktorer är användbara vid initial hantering av neutropeni. Hos refraktära patienter och hos dem med mycket aggressiv presentationsbehandling med kemoterapiregimer som liknar CHOP (cyklofosfamid, vinkristin, doxorubicin och prednison) och andra system för lymfom har testats, men har inte tydligt visat deras effektivitet. Andra behandlingar som har testats är purinanaloger, Alemtuzumab, bortezomib, splenektomi och allogen benmärgstransplantation, med varierande resultat.3
slutsatser
både FS och LGLL är sällsynta komplikationer av RA, som förekommer i långvarig sjukdom, med signifikant strukturell skada och extraartikulära manifestationer. Hos patienter med långvarig RA och neutropeni bör förekomsten av klonala proliferationer av LGL i perifert blod och/eller benmärg uteslutas, vilket möjliggör diagnos av LGLL. Första linjens behandling är användningen av immunsuppressiva läkemedel, såsom lågdos metotrexat, och glukokortikoider kan associeras med granulopoiesstimulerande faktorer. Andra behandlingsmetoder som kemoterapi eller splenektomi har visat varierande resultat i vissa eldfasta fall.
etiska upplysningar
skydd av människor och djur. Författarna förklarar att inga experiment utfördes på människor eller djur för denna undersökning.
sekretess för Data. Författarna förklarar att de har följt protokollen från sitt arbetscenter för publicering av patientdata och att alla patienter som ingår i studien har fått tillräcklig information och har gett sitt informerade samtycke skriftligen för att delta i den studien.