biologická Homochiralita: Jedním z Života Největších Záhad

V každé formě života na Zemi, cukry jsou vždy pravák, a aminokyseliny, které jsou vždy levou rukou. Co to znamená A proč se to děje? Tento bizarní jev zahrnuje chirální molekuly a je znám jako „homochiralita.“
chirální molekuly jsou molekuly stejného vzorce, ale s mírně odlišnými strukturami. Vaše ruka je chirální objekt, protože není překryta zrcadlovým obrazem; když položíte levou ruku na pravou stranu, palce budou ukazovat různými směry. V organických molekulách, když čtyři různé skupiny obklopují centrální uhlík, bude mít molekula dvě různé chirální formy zvané enantiomery. Tyto dvě molekuly jsou navzájem zrcadlovými obrazy, protože skupiny kolem uhlíku jsou orientovány v různých směrech, jako pravá a levá ruka. V chemii se tyto sloučeniny nazývají enantiomery R A S (nebo izomery). Když jsou však aminokyseliny nebo cukry chirální, vědci jim říkají izomery D A L (vědci jsou strašní v důsledném pojmenování věcí). D-znamená „pravák“ a L-znamená “ levák.“

D-a L-isomerů jsou normálně přítomny v poměru 50/50. Chemici to nazývají racemickou směsí. Přirozeně byste očekávali, že budou oba stejně přítomni v našem těle, že? Špatně! Ve skutečnosti všechny formy života používají pouze L-aminokyseliny a D-cukry. Přítomnost pouze jednoho izomeru se nazývá homochiralita. Od nejmenších bakterií až po slony tvoří proteiny pouze L-aminokyseliny a polysacharidy tvoří pouze d-cukry. Jinými slovy, všechny proteiny jsou praváky a všechny polysacharidy jsou leváky*. Proč je tohle? Je to tajemství, které Biology po celá léta zmatilo. Navzdory nejlepšímu úsilí fyziků, chemiků a evolučních biologů to stále nevíme jistě. Zde se podíváme na některé z předních současných teorií.
*(je třeba poznamenat, že některé l-cukry mohou být také rozloženy metabolickými cestami. Cukry mohou tvořit kruhy a D-cukr tvoří stabilnější kruh než l-cukr, ale L-cukry mohou stále existovat. Stabilita kruhu může být hlavním přispěvatelem k prevalenci d-cukrů. Níže se zaměříme především na aminokyseliny, které striktně dodržují jednu chirální formaci v biologických systémech.)
Enzymy a Evoluce

zde je to, co víme: enzymy v buňkách mohou metabolizovat pouze jeden izomer, ale ne druhý. Enzymy katalyzují reakce na štěpení a budování molekul vazbou na ně velmi specifickými způsoby. Enzym, který štěpí d-glukózu, nebude schopen rozložit l-glukózu. Kdybychom chtěli použít a vytvořit oba izomery, museli bychom mít dvě sady enzymů. To by vyžadovalo více DNA, více jídla a mnohem více energie. Přirozeně, buňky chtějí být co nejúčinnější, takže mít další sadu enzymů by bylo zdanění.
ale kdybychom měli ty extra enzymy, nemohli bychom také získat dvakrát tolik energie z prostředí? Mohli bychom použít dalších 50% izomerů, kdybychom měli enzymy, které je rozloží, místo abychom je plýtvali. Odpověď má co do činění s evolucí a potravinovou pyramidou.
Když se časný život vyvíjel, organismus by měl enzymy, které selektivně reagují s jedním izomerem. Organismy, které snědly tuto první formu života, by musely mít stejné selektivní enzymy, aby je strávily. Pokud všechny vaše jídlo obsahuje pouze d-cukry, tak budete! Pokud tedy dno potravinového řetězce používá pouze L-aminokyseliny, homochiralita se rozšíří do každého organismu v potravinovém řetězci! Protože život musel nejprve vyvinout jednu sadu enzymů, skončili jsme s touto selektivitou. Selektivní tlak z evoluce přinutil každý nový organismus používat stejné typy aminokyselin a cukru jako ty před ním.
takže jakmile je vybrán jeden izomer, použije ho každá forma života. Ale proč L-aminokyseliny místo D-aminokyselin a proč d-cukry místo L-cukrů? To je skutečná záhada. Něco na samém začátku života muselo vybrat jeden nad druhým. Je možné, že v raných stádiích života některé organismy vyvinuly jednu sadu enzymů, zatímco jiné organismy měly druhou. Mohla to být náhodná událost, která zničila jednu řadu enzymů, ale vědci nejsou s touto odpovědí spokojeni. Musí existovat nějaký důvod, že L-aminokyseliny a D-cukry jsou pro přežití lepší než jejich protějšky.
zadejte fyziku
racemické směsi jsou 50/50 směsí obou izomerů. Existuje však důvod se domnívat, že v našem hvězdném systému existuje ve skutečnosti mírná energetická preference jednoho izomeru před druhým. Abychom pochopili tuto preferenci, musíme cestovat hluboko do Mléčné dráhy.
naše galaxie má chirální spin a magnetickou orientaci. To způsobuje, že kosmický prach kruhově polarizuje světlo v jednom směru. V podstatě, protože světlo je 2-dimenzionální vlna, bude se šířit ve spirále. Kosmický prach způsobuje, že se tato šroubovice otáčí přednostně v jednom směru.

kruhově polarizované světlo degraduje D-aminokyselin, více než L-aminokyseliny, tak L-aminokyseliny jsou stabilnější. To je podporováno studiemi meteorů a komet. Kosmická hmota, alespoň v Mléčné dráze, má přednost L-aminokyselinám kvůli kruhové polarizaci světla.
další fyzikální vysvětlení preference jednoho izomeru nad druhým souvisí s elektroslabou silou. Fyziku řídí čtyři základní síly: gravitace, elektromagnetismus, silná jaderná síla a elektroslabá síla (aka slabá jaderná síla). První tři jsou achirální: ovlivňují L-A D-izomery stejným způsobem. Elektroslabá síla je však ovlivněna chiralitou. Elektroslabá síla řídí radioaktivní rozpad atomů a molekul. V tomto rozpadu není parita vesmíru vždy zachována. Během rozpadu beta emitované elektrony upřednostňují jeden typ rotace. Spin elektronů opět degraduje D-aminokyseliny více než L-aminokyseliny, což způsobuje posun rovnováhy molekul ve prospěch L-izomeru.
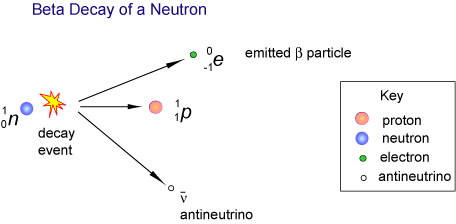
Oba polarizované světlo a elektroslabých kazu přispívají k mírné preference jednoho izomeru nad ostatními v naší galaxii. Ve velkém schématu věcí však tento rozpor nestačí k vysvětlení, proč každá forma života používá pouze d-cukry a L-aminokyseliny. Musí tu být něco víc. Což nás vede k …
Autokatalýze
jakmile fyzika dává malý okraj jednomu izomeru nad druhým, existuje chemický důvod, který zesiluje rozdíl. Autokatalýza znamená, že přítomnost chemické látky stimuluje vlastní výrobu. Kolem roku 1950 F. C. Frank navrhl, že dominantní izomery mohou aktivovat svou vlastní produkci a zároveň potlačit produkci druhého izomeru.

Na výše uvedeném obrázku znázorňuje bod. Při spuštění s 3 L-izomery a 2 D-izomery může být poměr velmi rychle amplifikován, takže L-izomery výrazně převyšují d-izomery. L-izomer stimuluje vlastní produkci, a L-izomer se také váže na D-izomer v procesu zvaném “ vzájemný antagonismus.“Tím se zabrání tvorbě více d-izomerů a L-izomer je rychle upřednostňován.
to byl jen hypotetický rámec, který vysvětluje, proč máme pouze L-aminokyseliny a D-cukry. Tento koncept však získal podporu, když byla objevena reakce Soai. Toto je jedna ukázka toho, jak mohou být určité izomery upřednostňovány před jinými v biologických procesech. Ačkoli neexistují žádné důkazy pro všudypřítomnou autokatlýzu způsobující homochiralitu, v některých případech to může být určitě faktor pro zesílení.
pracovní Model
dnes nejpopulárnější teorie biologické homochirality zahrnuje všechny tyto závěry. Fyzikální jevy, jako je polarizované světlo a elektroslabá síla, vytvářejí mírnou nerovnováhu D-A L-izomerů. Tento malý rozpor je autokatalýzou zesílen do nerovnoměrnější nerovnováhy. Poté, jakmile byl vytvořen život, byl rychle vybrán jeden izomer potravinovým řetězcem a specificitou enzymů. Dnes tedy vidíme pouze L-aminokyseliny a D-cukry.
tato teorie má stále nějaké díry. Nikdy nemusí existovat dokonalé vysvětlení události, která začala před miliardami let. Nyní však máme alespoň potenciální řešení tajemství biolgické homochirality.
“ tajemství vytváří zázrak a zázrak je základem touhy člověka porozumět.“— Neil Armstrong