Homochiralité biologique: Un des plus grands mystères de la vie

Dans toutes les formes de vie sur Terre, les sucres sont toujours droitiers et les acides aminés sont toujours gauchers. Qu’est-ce que cela signifie et pourquoi cela arrive-t-il? Ce phénomène bizarre implique des molécules chirales et est connu sous le nom « d’homochiralité. »
Les molécules chirales sont des molécules de même formule, mais avec des structures légèrement différentes. Votre main est un objet chiral car elle n’est pas superposable à son image miroir; lorsque vous placez votre main gauche sur votre droite, vos pouces pointent dans des directions différentes. Dans les molécules organiques, lorsque quatre groupes différents entourent un carbone central, la molécule aura deux formes chirales différentes appelées énantiomères. Ces deux molécules sont des images miroir l’une de l’autre, car les groupes autour du carbone sont orientés dans des directions différentes, comme les mains droite et gauche. En chimie, ces composés sont appelés énantiomères (ou isomères) R et S. Cependant, lorsque les acides aminés ou les sucres sont chiraux, les scientifiques les appellent isomères D et L (les scientifiques sont terribles pour nommer les choses de manière cohérente). D – signifie « droitier » et L – signifie « gaucher.”

Les isomères D et L sont normalement présents dans un rapport 50/50. Les chimistes appellent cela un mélange racémique. Naturellement, vous vous attendez à ce qu’ils soient tous les deux également présents dans notre corps, n’est-ce pas? Faux ! En fait, toutes les formes de vie n’utilisent que des acides aminés L et des sucres D. La présence d’un seul isomère est appelée homochiralité. Des plus petites bactéries aux éléphants, seuls les acides aminés L composent les protéines et seuls les sucres D composent les polysaccharides. En d’autres termes, toutes les protéines sont droitières et tous les polysaccharides sont gauchers *. Pourquoi est-ce? C’est un mystère qui laisse perplexe les biologistes depuis des années. Malgré les meilleurs efforts des physiciens, des chimistes et des biologistes de l’évolution, nous ne savons toujours pas avec certitude. Ici, nous allons jeter un coup d’œil à certaines des principales théories actuelles.
* (Il convient de noter que certains sucres L peuvent également être décomposés par des voies métaboliques. Les sucres peuvent former des anneaux, et le sucre D forme un anneau plus stable que le sucre L, mais les sucres L peuvent toujours exister. La stabilité de l’anneau peut être le principal contributeur à la prévalence des sucres D. Ci-dessous, nous nous concentrerons principalement sur les acides aminés, qui adhèrent strictement à une seule formation chirale dans les systèmes biologiques.)
Enzymes et évolution

Voici ce que nous savons: les enzymes des cellules ne peuvent métaboliser qu’un seul isomère, mais pas l’autre. Les enzymes catalysent des réactions pour décomposer et construire des molécules en se liant à elles de manière très spécifique. Une enzyme qui décompose le D-glucose ne pourra pas décomposer le L-glucose. Si nous voulions utiliser et construire les deux isomères, nous devrions avoir deux ensembles d’enzymes. Cela nécessiterait plus d’ADN, plus de nourriture et beaucoup plus d’énergie. Naturellement, les cellules veulent être aussi efficaces que possible, donc avoir un ensemble supplémentaire d’enzymes serait taxant.
Mais si nous avions ces enzymes supplémentaires, ne pourrions-nous pas également obtenir deux fois plus d’énergie de l’environnement? Nous pourrions utiliser les 50% d’isomères restants si nous avions les enzymes pour les décomposer au lieu de les gaspiller. La réponse concerne l’évolution et la pyramide alimentaire.
Au début de la vie, un organisme avait des enzymes qui réagissaient sélectivement avec un isomère. Les organismes qui ont mangé cette première forme de vie devraient avoir les mêmes enzymes sélectives pour les digérer. Si tous vos aliments ne contiennent que des sucres D, vous le ferez aussi! Donc, si le bas de la chaîne alimentaire n’utilise que des acides aminés L, l’homochiralité se propagera à tous les organismes de la chaîne alimentaire! Puisque la vie devait d’abord développer un ensemble d’enzymes, nous avons fini par être coincés avec cette sélectivité. La pression sélective de l’évolution a forcé chaque nouvel organisme à utiliser les mêmes types d’acides aminés et de sucres que ceux qui l’ont précédé.
Ainsi, une fois qu’un isomère est choisi, chaque forme de vie l’utilisera. Mais pourquoi les acides aminés L au lieu des acides aminés D, et pourquoi les sucres D au lieu des sucres L? C’est le vrai mystère. Quelque chose au tout début de la vie devait choisir l’un par rapport à l’autre. Il est possible qu’au début de la vie, certains organismes aient développé un ensemble d’enzymes, tandis que différents organismes en avaient l’autre. Cela aurait pu être un événement aléatoire qui a effacé une lignée d’enzymes, mais les scientifiques ne sont pas satisfaits de cette réponse. Il doit y avoir une raison pour laquelle les acides aminés L et les sucres D sont meilleurs pour la survie que leurs homologues.
Entrez en physique
Les mélanges racémiques sont des mélanges 50/50 des deux isomères. Mais il y a des raisons de croire que dans notre système stellaire, il y a en fait une légère préférence énergétique pour un isomère par rapport à l’autre. Pour comprendre cette préférence, nous devons voyager profondément dans la Voie Lactée.
Notre galaxie a un spin chiral et une orientation magnétique. Cela provoque la polarisation circulaire de la lumière par la poussière cosmique dans une direction. Fondamentalement, parce que la lumière est une onde à 2 dimensions, elle se propagera en hélice. La poussière cosmique fait tourner préférentiellement cette hélice dans un sens.

Cette lumière polarisée circulairement dégrade les acides aminés D plus que les acides aminés L, de sorte que les acides aminés L sont plus stables. Ceci est soutenu par des études de météores et de comètes. La matière cosmique, du moins dans la Voie lactée, a une préférence pour les acides aminés L en raison de la polarisation circulaire de la lumière.
Une autre explication physique de la préférence d’un isomère par rapport à l’autre est liée à la force électrofaible. Il y a quatre forces fondamentales qui régissent la physique: la gravitation, l’électromagnétisme, la force nucléaire forte et la force électrofaible (aussi appelée force nucléaire faible). Les trois premiers sont achiraux: ils affectent les isomères L et D de la même manière. La force électrofaible, cependant, est affectée par la chiralité. La force électrofaible régit la désintégration radioactive des atomes et des molécules. Dans cette décadence, la parité de l’univers n’est pas toujours préservée. Pendant la désintégration bêta, les électrons émis favorisent un type de spin. Le spin des électrons dégrade à nouveau les acides aminés D plus que les acides aminés L, ce qui provoque un décalage de l’équilibre des molécules en faveur de l’isomère L.
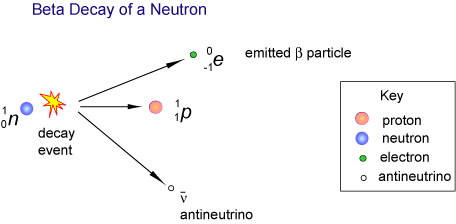
La lumière polarisée et la désintégration électrofaible contribuent à une légère préférence d’un isomère par rapport à l’autre dans notre galaxie. Cependant, dans le grand schéma des choses, cet écart ne suffit pas à expliquer pourquoi CHAQUE forme de vie utilise uniquement des sucres D et des acides aminés L. Il doit y avoir quelque chose de plus. Ce qui nous amène àAutoc
Autocatalyse
Une fois que la physique donne un léger avantage à un isomère par rapport à l’autre, il y a une raison chimique qui amplifie la différence. L’autocatalyse signifie que la présence d’un produit chimique stimule sa propre production. Vers 1950, F.C. Frank a suggéré que les isomères dominants peuvent activer leur propre production tout en supprimant la production de l’autre isomère.

Le graphique ci-dessus illustre le point. En commençant avec 3 isomères L et 2 isomères D, le rapport peut être très rapidement amplifié, de sorte que les isomères L sont largement plus nombreux que les isomères D. L’isomère L stimule sa propre production, et l’isomère L se lie également à l’isomère D dans un processus appelé « antagonisme mutuel. »Cela empêche la formation de plus d’isomères D, et l’isomère L est rapidement favorisé.
Ce n’était qu’un cadre hypothétique pour expliquer pourquoi nous n’avons que des acides aminés L et des sucres D. Mais ce concept a gagné en soutien lorsque la réaction Soai a été découverte. C’est une démonstration de la façon dont certains isomères peuvent être favorisés par rapport à d’autres dans les processus biologiques. Bien qu’il n’y ait aucune preuve d’une autocatalyse omniprésente provoquant une homochiralité, elle peut certainement être un facteur d’amplification dans certains cas.
Un modèle de travail
Aujourd’hui, la théorie la plus populaire de l’homochiralité biologique comprend toutes ces conclusions. Des phénomènes physiques tels que la lumière polarisée et la force électrofaible créent un léger déséquilibre des isomères D et L. Ce petit écart est amplifié en un déséquilibre plus inégal par autocatalyse. Ensuite, une fois la vie formée, un seul isomère a été sélectionné rapidement par la chaîne alimentaire et la spécificité des enzymes. Ainsi, aujourd’hui, nous ne voyons que des acides aminés L et des sucres D.
Cette théorie a encore quelques trous. Il n’y aura peut-être jamais d’explication parfaite pour un événement qui a commencé il y a des milliards d’années. Mais nous avons maintenant au moins une solution potentielle au mystère de l’homochiralité biolgique.
« Le mystère crée l’émerveillement, et l’émerveillement est la base du désir de l’homme de comprendre.”— Neil Armstrong