a biológia fogalmai-1.kanadai kiadás
a vírusokat először egy porcelánszűrő kifejlesztése után fedezték fel, amelyet Chamberland-Pasteur szűrőnek hívtak, amely eltávolíthatja a mikroszkóp alatt látható összes baktériumot bármely folyékony mintából. 1886-ban Adolph Meyer bebizonyította, hogy a dohánynövények betegsége, a dohánymozaik betegség folyékony növényi kivonatok révén átvihető egy beteg növényről egészségesre. 1892-ben Dmitrij Ivanowski kimutatta, hogy ez a betegség ilyen módon továbbítható, még akkor is, ha a Chamberland-Pasteur szűrő eltávolította az összes életképes baktériumot a kivonatból. Ennek ellenére sok év telt el, mire bebizonyosodott, hogy ezek a “szűrhető” fertőző ágensek nem egyszerűen nagyon kicsi baktériumok, hanem egy új típusú apró, betegséget okozó részecskék.
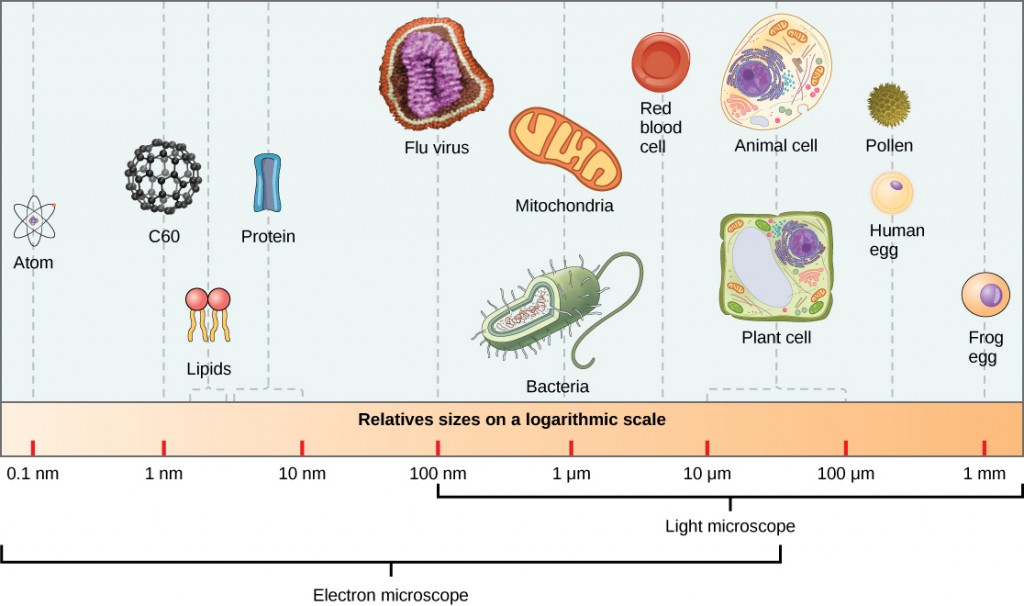
virionok, egyetlen vírusrészecskék, nagyon kicsiek,körülbelül 20-250 nanométer (1 nanométer = 1/1 000 000 mm). Ezek az egyes vírusrészecskék a vírus fertőző formája a gazdasejten kívül. A baktériumokkal ellentétben (amelyek körülbelül 100-szor nagyobbak) nem láthatunk vírusokat fénymikroszkóppal, kivéve a poxvirus család néhány nagy virionját (12.3 ábra).
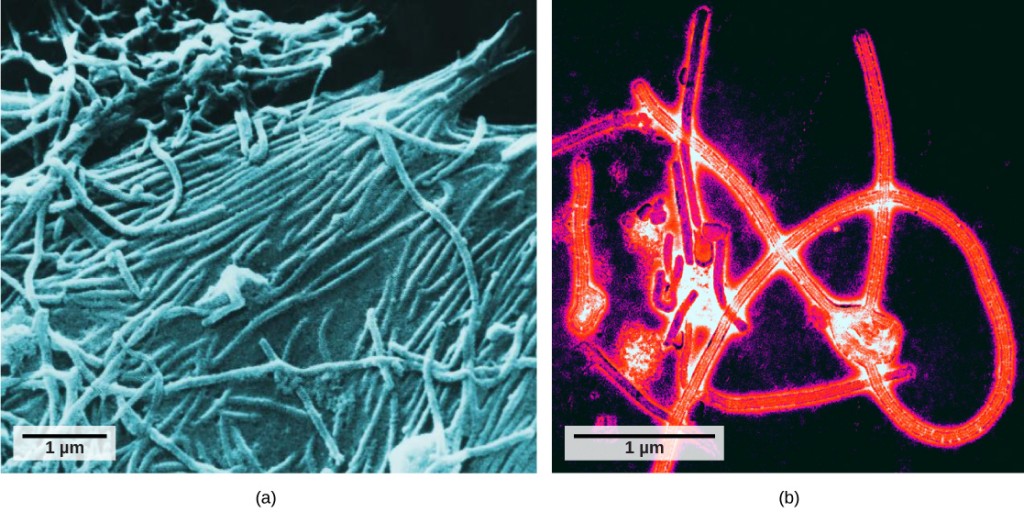
csak az 1940-es évek elektronmikroszkópjának kifejlesztése után kaptak a tudósok első jó képet a dohánymozaik vírus szerkezetéről (12.2 Ábra) és mások. A virionok felületi szerkezete mind szkenneléssel, mind transzmissziós elektronmikroszkóppal megfigyelhető, míg a vírus belső szerkezete csak transzmissziós elektronmikroszkóp képein figyelhető meg (12.4.ábra).
ennek a technológiának a használata lehetővé tette az összes típusú élő szervezet számos vírusának felfedezését. Kezdetben megosztott morfológia szerint csoportosították őket, ami méretüket, alakjukat és megkülönböztető szerkezetüket jelentette. Később a víruscsoportokat az általuk tartalmazott nukleinsav típusa, DNS vagy RNS szerint osztályozták, valamint hogy nukleinsavuk egy – vagy kettős szálú volt-e. Újabban a vírusreplikációs ciklusok molekuláris elemzése tovább finomította osztályozásukat.
a virion egy nukleinsav-magból, egy külső fehérjebevonatból és néha a gazdasejtből származó fehérje-és foszfolipid membránokból álló külső burokból áll. A víruscsaládok tagjai közötti legszembetűnőbb különbség a morfológiájuk, amely meglehetősen változatos. A vírus összetettségének érdekes tulajdonsága, hogy a gazdaszervezet összetettsége nem korrelál a virion összetettségével. A legösszetettebb virionszerkezetek egy részét bakteriofágokban, a legegyszerűbb élő szervezeteket, baktériumokat megfertőző vírusokban figyelik meg.
a vírusok sokféle formában és méretben léteznek, de ezek konzisztensek és különböznek minden víruscsalád esetében (12.5 ábra). Minden virionnak van egy nukleinsav-genomja, amelyet egy protein védőréteg borít, az úgynevezett kapszid. A kapszid kapszomereknek nevezett fehérje alegységekből áll. Egyes vírusos kapszidok egyszerű poliéderes “gömbök”, míg mások meglehetősen összetett szerkezetűek. Egyes vírusok kapszidját körülvevő külső szerkezetet vírusos borítéknak nevezzük. Minden vírus valamilyen glikoproteint használ, hogy a sejt vírusreceptoroknak nevezett molekuláihoz kapcsolódjon gazdasejtjeihez. A vírus kihasználja ezeket a sejtfelszíni molekulákat, amelyeket a sejt más célra használ fel, hogy felismerje és megfertőzze az egyes sejttípusokat. Például a kanyaró vírus egy sejtfelszíni glikoproteint használ az emberekben, amely általában immunreakciókban, esetleg a spermium-tojás kölcsönhatásban működik a megtermékenyítéskor. A kötődés követelménye, hogy a vírusok később behatoljanak a sejtmembránba, befecskendezzék a vírusgenomot, és befejezzék replikációjukat a sejten belül.
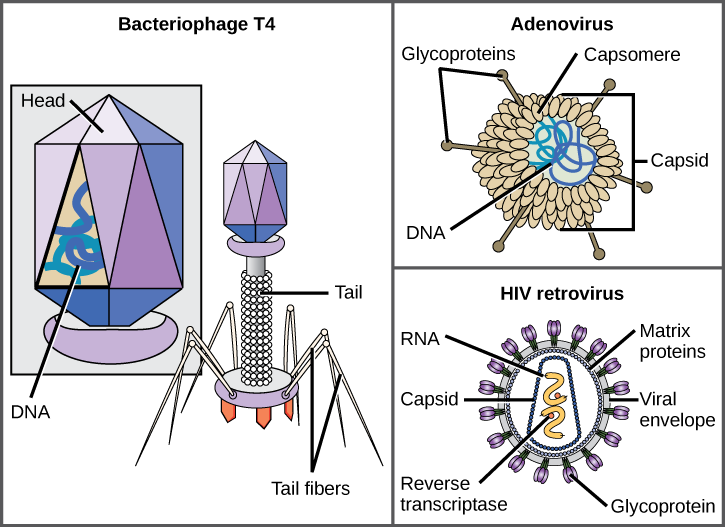
a T4 bakteriofág, amely megfertőzi az E. coli baktériumot, az egyik legösszetettebb ismert virion; a T4 fehérje farokszerkezettel rendelkezik, amelyet a vírus a gazdasejthez köt, valamint egy fejszerkezettel, amely a DNS-ét tartalmazza.
az adenovírus, egy nem fertőzött állati vírus, amely légúti betegségeket okoz az emberekben, a kapszomerjeiből kinyúló fehérjetüskéket használja a gazdasejthez való kötődéshez. A nem fertőzött vírusok közé tartoznak azok is, amelyek polio-t (poliovírust), növényi szemölcsöket (papillomavírust) és hepatitis A-t (hepatitis A vírus) okoznak. A nem fertőzött vírusok általában robusztusabbak és nagyobb valószínűséggel élnek túl zord körülmények között, például a bélben.
a burkolt virionok, mint a HIV (humán immundeficiencia vírus), az AIDS kórokozója (szerzett immunhiányos szindróma) nukleinsavból (HIV esetén RNS) és kapszid fehérjékből állnak, amelyeket foszfolipid kétrétegű burok és a hozzájuk kapcsolódó fehérjék vesznek körül (12.5 ábra). A bárányhimlő, az influenza, a mumpsz példák a borítékkal ellátott vírusok által okozott betegségekre. A boríték törékenysége miatt a nem fertőzött vírusok jobban ellenállnak a hőmérséklet, a pH és néhány fertőtlenítőszer változásainak, mint a burkolt vírusok.
összességében a virion alakja és a boríték jelenléte vagy hiánya keveset mond arról, hogy a vírusok milyen betegségeket okozhatnak, vagy milyen fajokat fertőzhetnek meg, de még mindig hasznos eszköz a vírus osztályozásának megkezdéséhez.
a vírusszerkezettel kapcsolatos alábbi állítások közül melyik igaz?
a) minden vírus vírusmembránba van burkolva.
B) a kapszomer kis fehérje alegységekből áll, amelyeket kapszidoknak neveznek.
C) A DNS az összes vírus genetikai anyaga.
D) a glikoproteinek segítenek a vírusnak a gazdasejthez való kötődésében.
<!–D – >
ellentétben minden olyan élő organizmussal, amely genetikai anyagként DNS-t használ, a vírusok DNS-t vagy RNS-t használhatnak. A vírusmag tartalmazza a vírus genomját vagy teljes genetikai tartalmát. A vírusgenomok általában kicsiek a baktériumokhoz vagy eukariótákhoz képest, csak azokat a géneket tartalmazzák, amelyek olyan fehérjéket kódolnak, amelyeket a vírus nem tud a gazdasejtből megszerezni. Ez a genetikai anyag lehet egyszálú vagy kettős szálú. Lehet lineáris vagy kör alakú is. Míg a legtöbb vírus egyetlen szegmens nukleinsavat tartalmaz, másoknak több szegmensből álló genomja van.
a DNS-vírusok DNS-maggal rendelkeznek. A vírus DNS irányítja a gazdasejt replikációs fehérjéit, hogy szintetizálják a vírusgenom új példányait, és átírják és lefordítják ezt a genomot vírusfehérjékké. A DNS-vírusok olyan emberi betegségeket okoznak, mint a bárányhimlő, a hepatitis B és néhány nemi betegség, mint a herpesz és a genitális szemölcsök.
az RNS vírusok csak RNS-t tartalmaznak a magjukban. A gazdasejtben lévő genomjaik replikálásához az RNS-vírusok genomjai olyan enzimeket kódolnak, amelyek nem találhatók meg a gazdasejtekben. Az RNS polimeráz enzimek nem olyan stabilak, mint a DNS polimerázok, és gyakran hibákat követnek el a transzkripció során. Emiatt az RNS-vírusokban a mutációk, a nukleotidszekvencia változásai gyakrabban fordulnak elő, mint a DNS-vírusokban. Ez gyorsabb evolúcióhoz és az RNS vírusok megváltozásához vezet. Például az a tény, hogy az influenza RNS vírus, az egyik oka annak, hogy minden évben új influenza oltásra van szükség. Az RNS vírusok által okozott emberi betegségek közé tartozik a hepatitis C, a kanyaró és a veszettség.
a vírusok kötelező intracelluláris parazitáknak tekinthetők. A vírusnak hozzá kell kapcsolódnia egy élő sejthez, be kell vennie, előállítania a fehérjéit és lemásolnia a genomját, és meg kell találnia a módját, hogy elkerülje a sejtet, hogy a vírus megfertőzhessen más sejteket és végül más személyeket. A vírusok csak bizonyos gazdaszervezeteket képesek megfertőzni, és csak bizonyos sejteket a gazdaszervezeten belül. Ennek a specifitásnak a molekuláris alapja az, hogy egy adott felületi molekulát, amelyet vírusreceptornak neveznek, meg kell találni a gazdasejt felületén a vírus kötődéséhez. A differenciális génexpresszió alapján a különböző sejttípusokban megfigyelt metabolikus különbségek valószínűleg olyan tényezők, amelyekben a vírus felhasználhatja a sejteket a replikációhoz. A sejtnek olyan anyagokat kell előállítania, amelyekre a vírusnak szüksége van, például olyan enzimeket, amelyekhez maga a vírusgenom nem rendelkezik génekkel, vagy a vírus nem lesz képes megismételni ezt a sejtet.
A vírusfertőzések lépései
a vírusnak” át kell vennie ” egy sejtet a replikációhoz. A vírusreplikációs ciklus drámai biokémiai és szerkezeti változásokat eredményezhet a gazdasejtben, ami sejtkárosodást okozhat. Ezek a citopátiás hatásoknak nevezett változások megváltoztathatják a sejt funkcióit, vagy akár elpusztíthatják a sejtet. Egyes fertőzött sejtek, például a közönséges hideg vírus (rhinovírus) által fertőzöttek, lízis (feltörés) vagy apoptózis (programozott sejthalál vagy “sejt öngyilkosság”) útján halnak meg, egyszerre felszabadítva az összes utód viriont. A vírusos betegségek tünetei a vírusra adott immunválaszból származnak, amely megpróbálja ellenőrizni és eltávolítani a vírust a szervezetből, valamint a vírus által okozott sejtkárosodásból. Számos állati vírus, például a HIV (humán immunhiányos vírus) az immunrendszer fertőzött sejtjeit egy bimbózásnak nevezett eljárással hagyja el, ahol a virionok külön-külön hagyják el a sejtet. A bimbózási folyamat során a sejt nem megy át lízisen, és nem azonnal elpusztul. A HIV által fertőzött sejtek károsodása azonban lehetetlenné teheti, hogy a sejtek az immunitás közvetítőjeként működjenek, annak ellenére, hogy a sejtek egy ideig életben maradnak. A legtermékenyebb vírusfertőzések hasonló lépéseket követnek a vírus replikációs ciklusában: rögzítés, behatolás, uncoating, replikáció, összeszerelés és kiadás.
egy vírus a kapsidban lévő kötődési fehérjék vagy a borítékába ágyazott fehérjék révén kapcsolódik a gazdasejt membránjának egy specifikus receptorhelyéhez. A kötődés specifikus, és általában egy vírus csak egy vagy néhány faj sejtjeihez kötődik,és csak bizonyos sejttípusokhoz a megfelelő receptorokkal.
koncepció akcióban

tekintse meg ezt a videót, hogy vizuálisan elmagyarázza, hogyan támadja meg a HIV és az influenza a testet.
az állati vírusokkal ellentétben a bakteriofágok nukleinsavját meztelenül injektálják a gazdasejtbe, így a kapszid a sejten kívül marad. A növényi és állati vírusok endocitózis útján juthatnak be sejtjeikbe, amelyben a sejtmembrán körülveszi és elnyeli az egész vírust. Néhány burkolt vírus akkor lép be a sejtbe, amikor a vírusboríték közvetlenül a sejtmembránnal összeolvad. A sejt belsejében a vírus kapszid lebomlik, és a vírus nukleinsav szabadul fel, amely ezután elérhetővé válik a replikációhoz és a transzkripcióhoz.
a replikációs mechanizmus a vírusgenomtól függ. A DNS-vírusok általában gazdasejt-fehérjéket és enzimeket használnak további DNS előállításához, amelyet a genom másolására vagy a messenger RNS (mRNS) átírására használnak, amelyet ezután a fehérjeszintézisben használnak. Az RNS-vírusok, mint például az influenzavírus, általában az RNS-magot használják sablonként a vírus genomiális RNS és mRNS szintéziséhez. A virális mRNS vírusenzimekké és kapszidfehérjékké alakul át, hogy új virionokat állítsanak össze (12.6.ábra). Természetesen vannak kivételek erre a mintára. Ha egy gazdasejt nem biztosítja a vírusreplikációhoz szükséges enzimeket, a vírusgének szolgáltatják az információt a hiányzó fehérjék közvetlen szintéziséhez. A retrovírusok, például a HIV, rendelkeznek egy RNS-genommal, amelyet vissza kell írni a DNS előállításához, amelyet aztán beillesztenek a gazdaszervezet DNS-ébe. Az RNS DNS-vé történő átalakításához a retrovírusok olyan géneket tartalmaznak, amelyek kódolják a vírusspecifikus enzim reverz transzkriptázt, amely RNS-sablont ír át DNS-re. Az a tény, hogy a HIV saját enzimeket termel, amelyek nem találhatók meg a gazdaszervezetben, lehetővé tette a kutatók számára, hogy olyan gyógyszereket fejlesszenek ki, amelyek gátolják ezeket az enzimeket. Ezek a gyógyszerek, beleértve az azt reverz transzkriptáz inhibitort, gátolják a HIV replikációját azáltal, hogy csökkentik az enzim aktivitását anélkül, hogy befolyásolnák a gazdaszervezet anyagcseréjét.
a vírusreplikáció utolsó szakasza az új virionok felszabadulása a gazdaszervezetbe, ahol képesek megfertőzni a szomszédos sejteket és megismételni a replikációs ciklust. Egyes vírusok akkor szabadulnak fel, amikor a gazdasejt meghal, más vírusok pedig a membránon keresztül bimbózva hagyhatják el a fertőzött sejteket anélkül, hogy közvetlenül megölnék a sejtet.
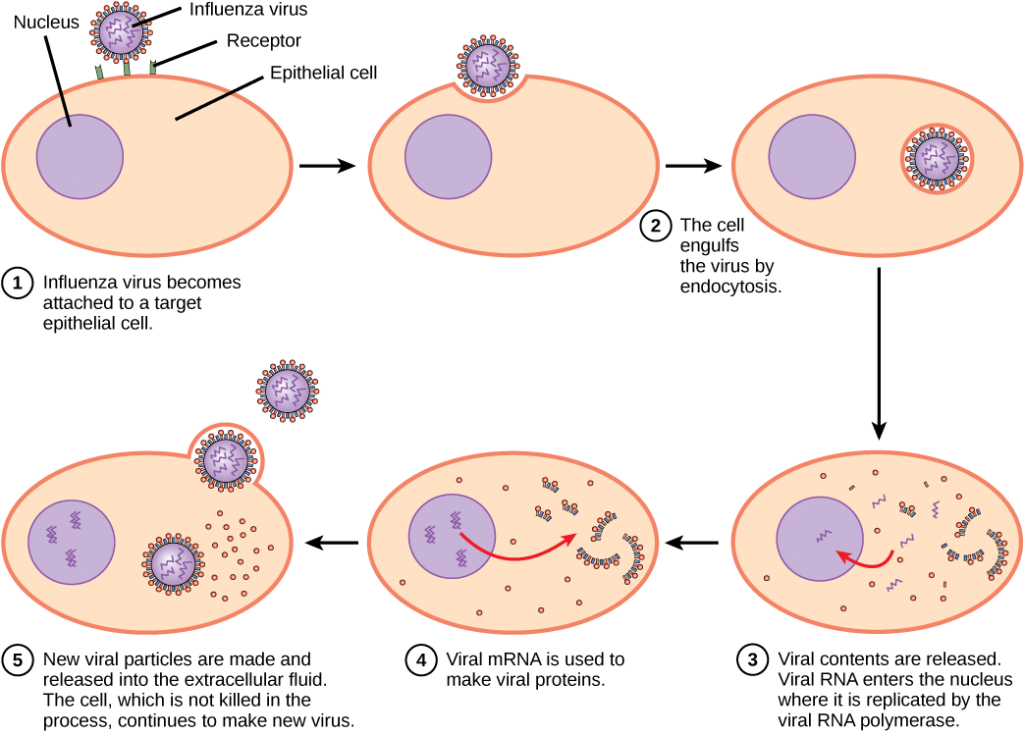
az influenzavírus vírusos borítékba van csomagolva, amely összeolvad a plazmamembránnal. Ily módon a vírus kiléphet a gazdasejtből anélkül, hogy megölné. Milyen előnye van a vírusnak, ha életben tartja a gazdasejtet?
<!–A gazdasejt továbbra is új vírusrészecskéket készíthet.–>
koncepció működés közben

kattintson a vírusokról szóló oktatóanyagra a struktúrák, az átviteli módok, a replikáció stb.azonosításához.