A young lady with seronegative systemic lupus erythematosus
Case Report – International Journal of Clinical Rheumatology (2017) Volume 12, Issue 2
Teaching Hospital, Jaffna, Sri Lanka
*Corresponding Author: De Zoysa HDJ
Teaching Hospital, Jaffna, Sri Lanka
E-mail:
Abstract
Systemic lupus erythematosus (SLE) is a chronic inflammatory autoimmune disease. È una malattia multisistemica che può coinvolgere qualsiasi organo del corpo. La maggior parte dei casi di SLE sono sieropositivi che dipendono dal test positivo per anticorpi antinucleari (ANA), cellule Lupus eritematose (LE) e anticorpi al DNA, ma i casi di SLE sieronegativi raramente possono presentare complicanze.
Keywords
il lupus eritematoso sistemico, anticorpi antinucleo, PRES sindrome
Introduzione
il lupus eritematoso Sistemico (LES) è una malattia cronica infiammatoria malattia autoimmune che può colpire qualsiasi organo del corpo come la pelle, le articolazioni, i reni, il sistema nervoso, il cuore, i polmoni e le membrane sierose . Questa malattia è caratterizzata dalla produzione di anticorpi ai componenti del nucleo cellulare. Mostra un ampio spettro di manifestazioni cliniche e immunologiche. La malattia è comune nelle donne con fascia di età fertile. L’anticorpo antinucleare (ANA) e l’anticorpo anti-DNA a doppio filamento (anti ds-DNA) sono solitamente associati a SLE. Ma non è essenziale per la diagnosi. ANA negativo SLE è stato introdotto da Koller et al. con cinque casi con caratteristiche cliniche simili a SLE . Qui riportiamo una giovane donna presentata con piressia di origine sconosciuta che è stata complicata con insufficienza renale acuta e livello alterato di coscienza e successivamente diagnosticata come SLE sieronegativo.
Case report
Una paziente di 27 anni con anamnesi di subfertilità primaria presentata con febbre attiva e disattiva per 6 mesi di durata. È stato associato a episodi intermittenti di dolore e gonfiore asimmetrici non migratori grandi e piccoli. Il paziente ha avuto perdita di appetito e riduzione di peso di 10 kg entro quel periodo. Non aveva alcun sintomo intestinale o vescicale. Non c’era storia di contatto con malattie croniche come la tubercolosi.
All’esame, il paziente era febbrile e malato. Era sprecata e l’indice di massa corporea (BMI) era di 16,3 kg/m2. Il paziente ha avuto alopecia e linfoadenopatia generalizzata. C’era un’eruzione popolare diffusa fotosensibile sulla fronte e sulla parte superiore del torace (Figura 1). Gli esami cardiovascolari, respiratori e neurologici erano normali. Aveva l’artrite interfalangiale prossimale, ma nessuna deformità articolare.

Figura 1. Eruzione fotosensibile sulla fronte.
Ma il 13 ° giorno del secondo ricovero ospedaliero il paziente divenne improvvisamente irrequieto e confuso. Ha sviluppato una ridotta produzione di urina. Anche se aveva la febbre, non ci sono stati episodi di crisi. La scala del coma di Glasgow del paziente (GCS) era 12/15 ma non c’era papilledema o rigidità del collo. Non aveva segni neurologici focali come segni del tratto lungo o paralisi del nervo cranico. BP era 180/120 mmHg in due occasioni in quel giorno, anche se altre letture BP erano normali prima di questo evento.
Le nostre diagnosi differenziali iniziali per la sua presentazione erano malattie del tessuto connettivo come SLE, tubercolosi polmonare, istiocitosi emofagocitica, neoplasie ematologiche come leucemia e linfoma, altre infezioni come il virus di Ebstein Barr (EBV) e la malattia di kikuchi.
La conta ematica completa (FBC) ha mostrato lieve leucopenia e anemia microcitica ipocromica con Emoglobina (Hb) 8,3 g / dl. L’analisi iniziale delle urine del paziente era anormale con globuli rossi e calchi di globuli rossi. Il tasso di sedimentazione degli eritrociti era di 106 mm/1 ° h e la proteina C reattiva era di 65 mg / dl al momento del ricovero. Ad eccezione delle proteine totali, il resto della funzionalità epatica era normale. L’albumina era bassa durante il ricovero ospedaliero con rapporto invertito di albumina e globulina. Le funzioni renali erano normali al momento del ricovero, ma aumentavano dopo il ricovero. La creatinina sierica ha raggiunto il valore massimo di 345 mg / dl entro il 20 ° giorno. Ma ha iniziato a venire giù con il trattamento. La radiografia del torace, l’ecografia addominale e l’ecocardiografia 2D erano normali. Lo screening settico era normale. ANA, ds-DNA e fattore reumatoide erano negativi. Il test di Mantoux e 3 campioni di espettorato erano negativi. La biopsia linfonodale ha mostrato linfonodo reattivo con cellule interfollicolari prominenti. L’aspirazione del midollo osseo ha mostrato un midollo reattivo. Ci sono stati T2W e FLAIR iper intensità visto in lobi parieto-occipitali bilaterali in risonanza magnetica della testa. La risonanza magnetica è stata riportata in quanto le apparenze erano probabilmente dovute a leucoencefalopatia reversibile posteriore (Figura 2).
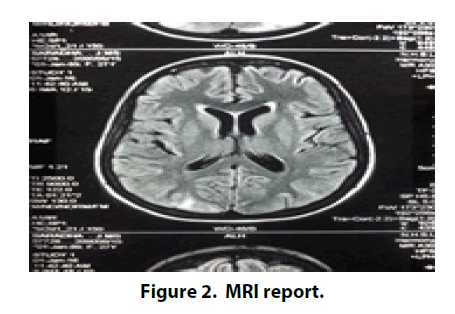
Figura 2. Referto della risonanza magnetica.
Dopo aver considerato le manifestazioni cliniche sopra e i risultati delle indagini, SLE sieronegativo complicato con sindrome da encefalopatia reversibile posteriore (PRESS) è stato diagnosticato secondo i criteri dell’American College of Rheumatology (ACR) del 1997 per SLE . Questo paziente aveva manifestazioni cutanee, artrite non erosiva, lupus cerebrale, nefrite lupica e leucopenia per la diagnosi del LES.
Il paziente è stato inizialmente trattato con metilprednisolone per impulso endovenoso 1 g/die per 3 giorni seguito da prednisolone orale 1 mg/kg / die. Ha migliorato significativamente con gli steroidi. La sua anemia è stata trattata con 3 pinte di trasfusioni di sangue seguite da ematinici orali. Dopo che lo steroide è stato eliminato, l’idrossiclorochina 200 mg bd e l’azatioprina 50 mg al giorno sono stati avviati come farmaci immunosoppressori risparmiatori di steroidi.
Discussione
SLE è un disturbo immunitario auto multi-sistema con varie presentazioni cliniche. È di eziologia sconosciuta e si manifesta con la deposizione di autoanticorpi patologici e immunocomplessi nei tessuti e nelle cellule. il 90-95% dei pazienti con LES è positivo per ANA e il suo titolo è uno dei criteri diagnostici chiave per SLE. Ma la positività ANA non è obbligatoria per la diagnosi . La sieronegatività nei pazienti con lupus può essere dovuta a un guasto tecnico o all’intrappolamento di ANA nei complessi immunitari circolanti.
Il concetto di lupus ANA-negativo è stato introdotto per la prima volta da Koller et al. La manifestazione cutanea, in particolare la fotosensibilità, è stata la caratteristica predominante nei primi casi di LES sieronegativo.
La diagnosi di LES può essere fatta combinando i risultati clinici e di laboratorio, ma al momento non esiste un criterio disponibile per l’identificazione precoce della malattia. I criteri dell’American College of Rheumatology (ACR) del 1997 e i suoi criteri complementari; i criteri SLICC (systemic lupus international collaborating clinic) del 2012 sono progettati per la classificazione del LES ma non per la diagnosi. I criteri SLICC 2012 sono molto complessi e possono essere utilizzati quando i criteri ACR non possono classificare SLE.
Il LES è ancora una malattia con morbilità e mortalità significative. Studi più recenti hanno dimostrato che l’ultima sopravvivenza a 5 anni è ora più vicina al 90-95% e che i pazienti 70-85% hanno una sopravvivenza a 10 anni . Nella maggior parte degli studi, il paziente con coinvolgimento renale aveva una prognosi infausta rispetto al paziente senza di esso.
La CRP di solito parallelizza l’attività della malattia in condizioni infiammatorie in quanto è un reagente di fase acuta prodotto dal fegato. Ma SLE è un’eccezione. Il paziente con SLE attivo mostra solo livelli di CRP modestamente elevati o addirittura normali nonostante la malattia attiva. Un marcato aumento della PCR nei pazienti con LES indica infezione e sierosite . Il nostro paziente aveva anche una CRP modestamente elevata durante l’ammissione; ciò potrebbe essere dovuto a un’infezione coesistente in questo paziente poiché non aveva caratteristiche cliniche di sierosite.
Il nostro paziente aveva sviluppato una rara complicanza neuropsichiatrica chiamata sindrome da leucoencefalopatia posteriore reversibile (PRES). Di solito si presenta con sintomi di insorgenza rapida che consistono in mal di testa, convulsioni, alterazione della coscienza e disturbi visivi. È fortemente associato a malattie che coesistono in pazienti con malattie renali come ipertensione, malattie autoimmuni e vascolari, esposizione a farmaci immunosoppressori come ciclofosfamide e ciclosporina e trapianto di organi . Deve essere considerato in qualsiasi paziente che sviluppa sintomi neurologici rapidi sullo sfondo di qualsiasi malattia renale.
Gli steroidi quale Prednisolone hanno azioni terapeutiche doppie in SLE. Ha sia azioni antinfiammatorie che immunosoppressive. Di solito è usato per trattare le principali complicanze dell’organo come la nefrite lupica e il lupus cerebrale. Steroidi risparmiando altri agenti immunosoppressori come azatioprina, ciclofosfamide e micofenolato mofetile devono essere considerati se viene utilizzato a lungo termine. Quando la dose giornaliera richiesta di Prednisolone supera i 60 mg / die, deve essere utilizzata la via endovenosa sotto forma di terapia a impulsi Metilprednisolone (30 mg/Kg, massimo 1 g/die). Idrossiclorochina (HCQ) 200-400 mg/die protegge contro la malattia flare e usato per trattare manifestazioni dermatologiche e articolari di SLE.
Non ci sono studi clinici valutati la gestione di PRES al momento. Ma la rimozione delle condizioni predisponenti tra cui la gestione aggressiva della pressione sanguigna, il ritiro dei farmaci incriminati o la consegna in eclampsia fissa il recupero e previene le complicanze .
In conclusione, questo paziente inizialmente presentava piressia di origine sconosciuta complicata da compromissione renale e coinvolgimento cerebrale nonostante la sieronegatività, è stata diagnosticata come LES . Se il paziente soddisfa i criteri per il LES nonostante la sieronegatività, la diagnosi non deve essere ritardata poiché il 5-10% dei pazienti con LES è sieronegativo.
- Uomo BL, Mok CC. Sierosite correlata alla prevalenza e all’esito del lupus eritematoso sistemico. Lupus. 14(10), 822–826 (2005).
- Koller SR, Johnston CL Jr, Moncure CW. Preparazione delle cellule del Lupus eritematoso-incongruenza del fattore antinucleare. Una revisione dei test diagnostici per il lupus eritematoso sistemico. Essere. J. Clin. Pathol. 66(3), 495–505 (1976).
- Hochberg MC. Aggiornamento dell’American College of Rheumatology dei criteri rivisti per la classificazione del lupus eritematoso sistemico. Artrite Rheum. 40(9), 1725 (1997).
- Berden JHM. Nefrite lupica. Rene Int. 52, 538–558 (1997).
- Petri M, Orbai AM, Alarcons GS et al. Derivazione e validazione dei criteri di collaborazione della clinica internazionale per il lupus eritematoso sistemico. Artrite Rheum. 64(8), 2677–2686 (2012).
- Trager J, Ward MM. Mortalità e cause di morte nel lupus eritematoso sistematico. Curr. Opin. Reumatolo. 13(5), 345–351 (2001).
- Honig S, Gorevic P, Weisssmann G. C-proteina reattiva nel lupus eritematoso sistemico. Artrite Rheum. 20(5), 1065–1070 (1977).
- Fugate JE, Claassen DO, Cloft HJ et al. Sindrome da encepaalopatia reversibile posteriore: associated clinical and radiological findings. Mayo. Clin. Proc. 85(5), 427–432 (2010).
- Tsakonas E, Joseph L, Esdalie JM et al. A long term study of hydroxychloroquine withdrawal on exacerbations in systemic lupus erythematosus. The Canadian Hydroxychloroquine study Group. Lupus 7(2), 80–85 (1997).