Omochiralità biologica: Uno dei Grandi Misteri

In ogni forma di vita sulla Terra, gli zuccheri sono sempre con la mano destra, e gli aminoacidi sono sempre con la mano sinistra. Cosa significa questo e perché succede? Questo bizzarro fenomeno coinvolge molecole chirali ed è noto come ” omochiralità.”
Le molecole chirali sono molecole della stessa formula, ma con strutture leggermente diverse. La tua mano è un oggetto chirale perché non è sovrapponibile alla sua immagine speculare; quando metti la mano sinistra sulla tua destra, i tuoi pollici punteranno in direzioni diverse. Nelle molecole organiche, quando quattro diversi gruppi circondano un carbonio centrale, la molecola avrà due diverse forme chirali chiamate enantiomeri. Queste due molecole sono immagini speculari l’una dell’altra, poiché i gruppi attorno al carbonio sono orientati in direzioni diverse, come le mani destra e sinistra. In chimica, questi composti sono chiamati enantiomeri R e S (o isomeri). Tuttavia, quando gli amminoacidi o gli zuccheri sono chirali, gli scienziati li chiamano isomeri D e L (gli scienziati sono terribili nel nominare le cose in modo coerente). D-significa “destrorso” e L-significa ” mancino.”

I D e L isomeri sono normalmente presenti in un rapporto 50/50. I chimici chiamano questa miscela racemica. Naturalmente, ci si aspetterebbe che entrambi siano ugualmente presenti nei nostri corpi, giusto? Sbagliato! Infatti, tutte le forme di vita usano solo L-aminoacidi e D-zuccheri. La presenza di un solo isomero è chiamata omochiralità. Dai batteri più piccoli agli elefanti, solo gli aminoacidi L costituiscono le proteine e solo gli zuccheri D costituiscono i polisaccaridi. In altre parole, tutte le proteine sono destrorse e tutti i polisaccaridi sono mancini*. Perché è questo? È un mistero che ha perplesso i biologi per anni. Nonostante i migliori sforzi di fisici, chimici e biologi evoluzionisti, non lo sappiamo ancora per certo. Qui, daremo un’occhiata ad alcune delle principali teorie attuali.
*(Va notato che alcuni L-zuccheri possono anche essere suddivisi per vie metaboliche. Gli zuccheri possono formare anelli e lo zucchero D forma un anello più stabile dello zucchero L, ma gli zuccheri L possono ancora esistere. La stabilità dell’anello può essere il principale contributore alla prevalenza di D-zuccheri. Di seguito, ci concentreremo principalmente sugli amminoacidi, che aderiscono rigorosamente a una singola formazione chirale nei sistemi biologici.)
gli Enzimi e l’Evoluzione

Ecco cosa sappiamo: gli enzimi nelle cellule possono metabolizzare solo un isomero, ma non l’altro. Gli enzimi catalizzano le reazioni per abbattere e costruire molecole legandosi a loro in modi molto specifici. Un enzima che scompone il D-glucosio non sarà in grado di scomporre il L-glucosio. Se volessimo usare e costruire entrambi gli isomeri, dovremmo avere due set di enzimi. Ciò richiederebbe più DNA, più cibo e molta più energia. Naturalmente, le cellule vogliono essere il più efficiente possibile, quindi avere un set extra di enzimi sarebbe tassativo.
Ma se avessimo quegli enzimi extra, non potremmo anche ottenere il doppio dell’energia dall’ambiente? Potremmo usare l’altro 50% degli isomeri se avessimo gli enzimi per scomporli invece di sprecarli. La risposta ha a che fare con l’evoluzione e la piramide alimentare.
Quando la vita precoce stava evolvendo, un organismo avrebbe enzimi che reagiscono selettivamente con un isomero. Gli organismi che hanno mangiato questa prima forma di vita avrebbero dovuto avere gli stessi enzimi selettivi per digerirli. Se tutto il tuo cibo contiene solo zuccheri D, lo farai anche tu! Quindi, se il fondo della catena alimentare utilizza solo L-aminoacidi, l’omochiralità si diffonderà in ogni organismo della catena alimentare! Dal momento che la vita ha dovuto sviluppare una serie di enzimi prima, abbiamo finito per essere bloccato con quella selettività. La pressione selettiva dell’evoluzione costrinse ogni nuovo organismo a utilizzare gli stessi tipi di aminoacidi e zuccheri di quelli precedenti.
Quindi una volta scelto un isomero, ogni forma di vita lo userà. Ma perché L-aminoacidi invece di D-aminoacidi, e perché D-zuccheri invece di L-zuccheri? Questo è il vero mistero. Qualcosa all’inizio della vita doveva selezionare l’uno sull’altro. È possibile che nelle prime fasi della vita, alcuni organismi abbiano sviluppato un insieme di enzimi, mentre diversi organismi hanno avuto l’altro. Potrebbe essere stato un evento casuale che ha spazzato via una linea di enzimi, ma gli scienziati non sono soddisfatti di questa risposta. Ci deve essere qualche ragione per cui gli aminoacidi L e gli zuccheri D sono migliori per la sopravvivenza rispetto alle loro controparti.
Inserisci fisica
Le miscele racemiche sono 50/50 miscele dei due isomeri. Ma c’è ragione di credere che nel nostro sistema stellare ci sia in realtà una leggera preferenza energetica per un isomero rispetto all’altro. Per capire questa preferenza, dobbiamo viaggiare in profondità nella Via Lattea.
La nostra galassia ha uno spin chirale e un orientamento magnetico. Questo fa sì che la polvere cosmica polarizzi circolarmente la luce in una direzione. Fondamentalmente, poiché la luce è un’onda 2-dimensionale, si propagherà in un’elica. La polvere cosmica causa questa elica di ruotare preferenzialmente in una direzione.

Questa luce polarizzata circolarmente degrada gli amminoacidi D più degli amminoacidi L, quindi gli amminoacidi L sono più stabili. Ciò è supportato da studi su meteore e comete. La materia cosmica, almeno nella Via Lattea, ha una preferenza per gli aminoacidi L a causa della polarizzazione circolare della luce.
Un’altra spiegazione fisica per la preferenza di un isomero rispetto all’altro ha a che fare con la forza elettrodebole. Ci sono quattro forze fondamentali che governano la fisica: gravitazione, elettromagnetismo, forza nucleare forte, e la forza elettrodebole (aka forza nucleare debole). I primi tre sono achirali: influenzano gli isomeri L e D allo stesso modo. La forza elettrodebole, tuttavia, è influenzata dalla chiralità. La forza elettrodebole governa il decadimento radioattivo di atomi e molecole. In questo decadimento, la parità dell’universo non è sempre preservata. Durante il decadimento beta, gli elettroni emessi favoriscono un tipo di spin. Lo spin degli elettroni degrada nuovamente gli amminoacidi D più degli amminoacidi L, causando lo spostamento dell’equilibrio delle molecole a favore dell’isomero L.
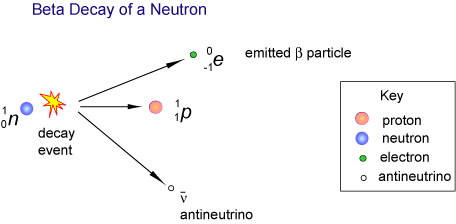
Sia la luce polarizzata e elettrodebole decadimento contribuire a una leggera preferenza di un isomero sopra l’altro nella nostra galassia. Tuttavia, nel grande schema delle cose, questa discrepanza non è sufficiente a spiegare perché OGNI forma di vita utilizza solo D-zuccheri e L-aminoacidi. Ci deve essere qualcosa di più. Il che ci porta a Autoc
Autocatalisi
Una volta che la fisica dà un leggero vantaggio a un isomero rispetto all’altro, c’è una ragione chimica che amplifica la differenza. Autocatalisi significa che la presenza di una sostanza chimica stimola la propria produzione. Intorno al 1950, F. C. Frank suggerì che gli isomeri dominanti possono attivare la propria produzione sopprimendo la produzione dell’altro isomero.

Il grafico sopra riportato illustra il punto. Quando si inizia con 3 isomeri L e 2 isomeri D, il rapporto può essere amplificato molto rapidamente in modo che gli isomeri L superino notevolmente gli isomeri D. L-isomero stimola la propria produzione, e L-isomero si lega anche al D-isomero in un processo chiamato “antagonismo reciproco.”Ciò impedisce la formazione di più isomeri D e l’isomero L viene rapidamente favorito.
Questo era solo un quadro ipotetico per spiegare perché abbiamo solo L-aminoacidi e D-zuccheri. Ma questo concetto ha ottenuto supporto quando è stata scoperta la reazione Soai. Questa è una dimostrazione di come alcuni isomeri possono essere favoriti rispetto ad un altro nei processi biologici. Anche se non ci sono prove per l’autocatlisi onnipresente che causa l’omochiralità, può certamente essere un fattore di amplificazione in alcuni casi.
Un modello funzionante
Oggi, la teoria più popolare per l’omochiralità biologica include tutte queste conclusioni. Fenomeni fisici come la luce polarizzata e la forza elettrodebole creano un leggero squilibrio degli isomeri D e L. Questa piccola discrepanza viene amplificata in uno squilibrio più irregolare mediante autocatalisi. Quindi, una volta formata la vita, un singolo isomero è stato selezionato rapidamente dalla catena alimentare e dalla specificità degli enzimi. Quindi, oggi vediamo solo L-aminoacidi e D-zuccheri.
Questa teoria ha ancora alcuni buchi. Potrebbe non esserci mai una spiegazione perfetta per un evento iniziato miliardi di anni fa. Ma ora abbiamo almeno una potenziale soluzione per il mistero dell’omochiralità biolgica.
“Il mistero crea meraviglia, e la meraviglia è la base del desiderio dell’uomo di capire.” Neil Armstrong