Ritardi AV & VV
1. Concetti di base
- Concetti di base : AV delay e VV delay optimization
- AV delay optimization
- VV delay optimization
- LV pacing alone o biventricular pacing ?
- Algoritmo AdaptivCRT
La risincronizzazione biventricolare fornisce un significativo beneficio clinico, un rimodellamento inverso con riduzione del volume cardiaco e una diminuzione della morbilità e della mortalità nei pazienti con insufficienza cardiaca con ampio QRS. La limitazione principale di questa terapia è che tutti gli studi hanno trovato una percentuale significativa di pazienti che non rispondono favorevolmente alla terapia di risincronizzazione. Sono stati proposti diversi approcci per ridurre la percentuale di non-responder. Una volta impiantato il paziente, una regolazione non ottimale del dispositivo CRT può contribuire ad alterare la qualità della risposta. Il principio del CRT è quello di modificare la sequenza di attivazione in un paziente con disturbo della conduzione elettrica regolando i ritardi di attivazione tra un cavo atriale destro, un cavo ventricolare destro e un cavo ventricolare sinistro. Due parametri programmabili sono accessibili in questo contesto: 1) il ritardo AV che determina l’attivazione temporizzazione tra l’atrio destro e il ventricolo destro, con programmazione indipendente di rilevamento di un ritardo AV (dopo il rilevamento di una spontanea atriale (COME ciclo -BV)) e un ritmo di ritardo AV a seguito di un atriale ritmo (AP-ciclo BV). È possibile programmare una variabile di ritardo AV con una riduzione lineare del ritardo AV in parallelo l’aumento della frequenza cardiaca; 2) I VV ritardo regola l’attivazione di ritardo tra il ventricolo destro e ventricolo sinistro; attivazione simultanea (VV ritardo a 0), un diritto di pre-attivazione (RV à LV, X ms) o a sinistra pre-attivazione (LV à RV, X ms) sono programmabili; non è possibile programmare una variabile VV ritardo con diversi valori a riposo e durante l’esercizio. Gli studi emodinamici acuti hanno chiaramente dimostrato un beneficio significativo fornito dall’ottimizzazione del ritardo AV e / o VV. La dimostrazione clinica di questo beneficio è molto meno convincente.
AV DELAY OPTIMIZATION
La contrazione atriale contribuisce al 20-30% della gittata cardiaca a riposo nei pazienti con insufficienza cardiaca con disfunzione sistolica, questo contributo aumenta durante l’esercizio. I pazienti con insufficienza cardiaca con disturbo della conduzione elettrica spesso mostrano asincronia atrioventricolare con un accorciamento del tempo di riempimento, una fusione delle onde E e A e rigurgito mitralico diastolico.
Nei pazienti risincronizzati, la programmazione di un breve ritardo AV consente di anticipare l’onda E, una dissociazione delle onde E e A e un prolungamento del tempo di riempimento. Il ritardo AV non dovrebbe essere impostato troppo breve perché ciò comporterebbe l’amputazione dell’onda A mediante chiusura mitralica. La regolazione del ritardo AV è raccomandata dopo l’impianto di un pacemaker CRT o di un defibrillatore anche se il livello di evidenza clinica è modesto.
Ci sono grandi variazioni interindividuali nella conduzione intra-atriale e nei disturbi intra-ventricolari che generano marcate differenze in termini di ritardo AV ottimale che giustificano teoricamente un approccio su misura per ciascun paziente. I ritardi AV rilevati e percorsi sono programmabili in modo indipendente e devono anche essere ottimizzati in modo indipendente. Una limitazione dell’ottimizzazione del ritardo AV è che di solito viene eseguita a riposo in posizione supina e per una data frequenza cardiaca. Queste condizioni differiscono significativamente da quelle osservate nella vita di tutti i giorni. Durante l’esercizio, a differenza dei pazienti con cuore sano in cui il ritardo AV ottimale si accorcia con l’aumento della frequenza cardiaca, sembra che la risposta dei pazienti risincronizzati allo stress non sia stereotipata. In alcuni pazienti il ritardo AV ottimale durante l’esercizio è più lungo che a riposo, in altri è più breve. L’uso sistematico dell’algoritmo di ritardo automatico AV probabilmente garantisce una cattura continua durante l’esercizio fisico, ma non è necessariamente associato a un ulteriore beneficio emodinamico. Pertanto la sua programmazione dovrebbe essere discussa per ciascun paziente. La risincronizzazione biventricolare consente il rimodellamento inverso con una progressiva riduzione nel tempo delle pressioni di sabbia del volume tele-sistolico e fine-diastolico. Pertanto, l’ottimizzazione del ritardo AV dovrebbe essere idealmente ripetuta periodicamente.
Il ritardo AV ottimale consente un massimo contributo della contrazione atriale sinistra al riempimento ventricolare sinistro, prolunga il tempo di riempimento, migliora la gittata cardiaca in assenza di rigurgito mitralico diastolico.
Se il ritardo AV è impostato troppo a lungo, la contrazione atriale si verifica troppo presto nella diastole, limitando il contributo atriale al riempimento ventricolare. La contrazione atriale è sovrapposta alla fase diastolica iniziale. L’ecocardiografia cardiaca trova una fusione tra onda E e un’onda e un breve tempo di riempimento con un rigurgito mitralico diastolico persistente.
Se il ritardo AV è impostato troppo breve, la contrazione ventricolare si verifica troppo presto con conseguente chiusura mitralica prematura interrompendo il riempimento corrente e limita il contributo atriale al riempimento ventricolare. L’ecocardiografia trova un’onda E prematura, un lungo tempo di riempimento e divide E e un’onda con un’onda troncata dalla chiusura mitrale. La diminuzione della pressione diastolica e la diminuzione del precarico portano ad una riduzione del dP / dt max e della gittata cardiaca.
Prima di iniziare l’ottimizzazione del ritardo AV, alcuni elementi devono essere noti. Nei pazienti con blocco atrioventricolare completo e blocco AV di alto grado o con un intervallo PR molto lungo, i cambiamenti nel ritardo AV non avranno alcun effetto diretto sul grado di cattura e fusione ventricolare. Al contrario, nei pazienti con conduzione atrioventricolare conservata, il prolungamento del ritardo AV causerà una fusione progressiva con attivazione spontanea. Regolazione del ritardo AV deve essere eseguita sotto controllo elettrocardiografico, integrando l’idea che nel gruppo di pazienti con blocco AV, che rappresenta la maggior parte dei pazienti, messa a punto del ritardo AV può variare il ritardo tra la sistole atriale e la sistole ventricolare ma anche di interagire direttamente con l’attivazione ventricolare sequenza e il grado di fusione ventricolare. Per superare questa difficoltà, il ritardo AV è spesso programmato sistematicamente breve (tra 90 e 120 ms dopo un’attività atriale rilevata e tra 130 e 150 ms dopo stimolazione atriale).
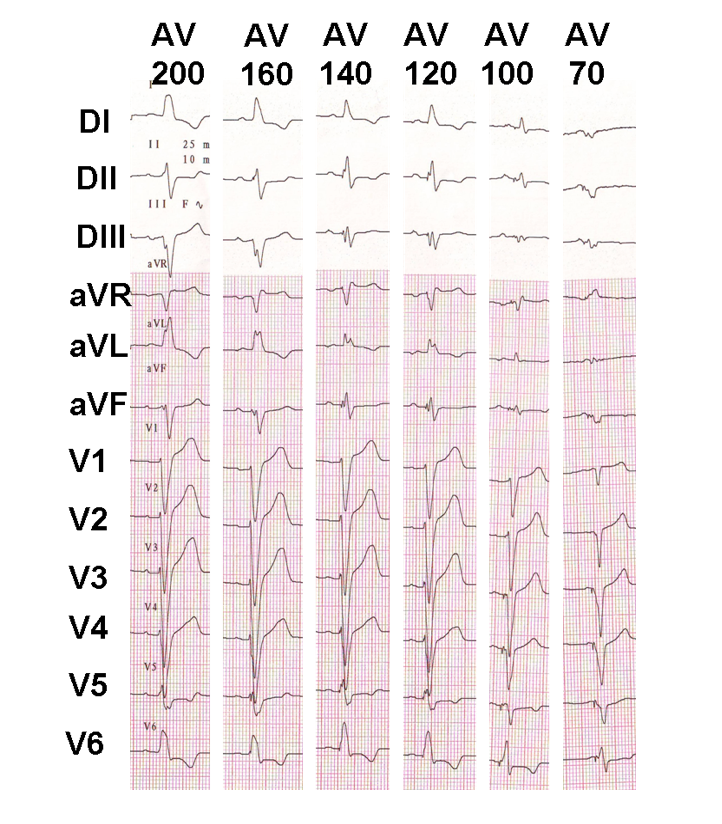
Esempio di regolazione progressiva del ritardo AV in un paziente risincronizzato con conduzione AV preservata; la fusione progressiva appare con il prolungamento del ritardo AV.
Sono state proposte varie tecniche per ottimizzare il ritardo AV:
- Ecocardiografia
Sono stati proposti diversi metodi ecocardiografici per ottimizzare il ritardo AV: il metodo di Ritter (che non è stato convalidato in una popolazione di pazienti con insufficienza cardiaca), la ricerca di un VTI massimo aortico o mitrale, un massimo dP / dt max e il metodo iterativo. Quest’ultimo è ampiamente utilizzato nella pratica clinica, con l’obiettivo di ottenere il tempo di riempimento più lungo senza amputazione dell’onda A basata sull’analisi del flusso trans-mitralico. - Altri metodi
È possibile utilizzare varie stime della contrattilità cardiaca o della gittata cardiaca: impulso ondulatorio, pressione sanguigna, dP / dt max, aspetto elettrocardiografico … L’applicabilità clinica nella pratica quotidiana è spesso limitata. - Algoritmo di ottimizzazione automatica incorporato nel dispositivo
Se sono necessarie ripetute ottimizzazioni del ritardo AV e devono essere eseguite in varie condizioni di pre carico, la soluzione ideale sarebbe che il pacemaker lo realizzi da solo. La funzione AdpativCRT è disponibile nell’ultima generazione di defibrillatori Medtronic; i principi operativi di questo nuovo algoritmo saranno discussi alla fine del presente capitolo.
OTTIMIZZAZIONE DEL RITARDO VV
Alcuni pazienti non rispondono alla CRT e continuano a mostrare una significativa dissincronia ventricolare meccanica dopo l’impianto. La regolazione del ritardo VV provoca una stimolazione biventricolare sequenziale e ha un impatto diretto sulla sequenza di attivazione ventricolare. La modifica del ritardo VV può essere proposta per ridurre l’asincronia persistente nei pazienti non rispondenti. Questo parametro appare interessante in teoria nei pazienti con una posizione subottimale del piombo LV, o una latenza e un tempo di conduzione prolungato nel sito di stimolazione. Se l’ottimizzazione del ritardo VV consente un significativo beneficio emodinamico acuto, la questione della rilevanza clinica di questo parametro rimane dibattuta e non confermata da studi clinici. Per quanto riguarda l’impostazione del ritardo AV, è probabile che il processo di rimodellamento influenzi direttamente l’ottimizzazione del ritardo VV e che l’ottimizzazione di questo parametro debba essere ripetuta nel tempo e in varie condizioni di precarico.
Gli stessi strumenti possono essere utilizzati per ottimizzare il ritardo AV e VV. L’ecocardiografia cardiaca è spesso utilizzata nella pratica clinica. Il VTI aortico che riflette la gittata cardiaca, il dP/dt max che riflette la contrattilità cardiaca o la misurazione del grado di asincronia ventricolare sono per lo più utilizzati. Ancora una volta, la funzione AdaptivCRT propone anche di ottimizzare automaticamente il ritardo VV. Alla luce dei limiti pratici dell’ottimizzazione VV, la ripetuta regolazione automatica di questo parametro da parte del dispositivo stesso sembra promettente. Tuttavia, è ancora necessario dimostrare la sua rilevanza clinica.
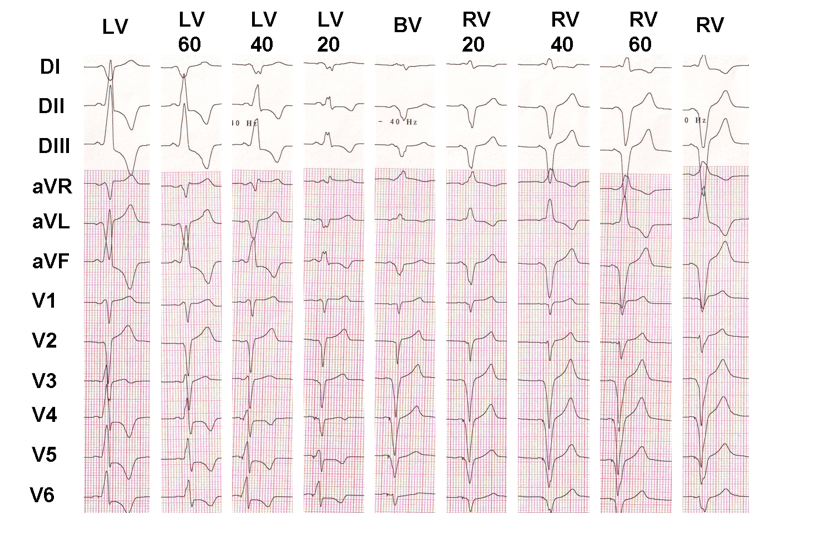
in Questo esempio viene illustrato l’effetto dei VV ritardo sulla ventricolare attivazione elettrica; se è facile dimostrare che il elettrocardiografici aspetto è effettivamente diverso da una configurazione all’altra, è molto più difficile determinare che cosa configurazione, per offrire la migliore risposta clinica.
STIMOLAZIONE LV DA SOLA O STIMOLAZIONE BIVENTRICOLARE ?
Uno dei principi di funzionamento dell’algoritmo AdaptivCRT consiste nella scelta tra ventricolo sinistro con fusione e stimolazione biventricolare.
Nessuno studio ha mai dimostrato la superiorità della stimolazione biventricolare su una stimolazione ventricolare sinistra pura. Al contrario, gli studi emodinamici acuti hanno costantemente riscontrato un beneficio significativo con la stimolazione ventricolare sinistra isolata. Allo stesso modo, gli studi clinici hanno trovato un beneficio più o meno identico in termini di classe NYHA, capacità di esercizio e rimodellamento ventricolare a quelli osservati con stimolazione biventricolare. Tuttavia, ampi studi che dimostrano i benefici forniti dalla risincronizzazione sono stati tutti eseguiti con stimolazione biventricolare e non con stimolazione ventricolare sinistra.
Nella configurazione di stimolazione LV, la risincronizzazione dei due ventricoli può essere ottenuta dalla fusione tra l’attivazione ritmica ventricolare sinistra dell’attivazione intrinseca del ventricolo destro. Se sembra che l’ottimale acuta emodinamica beneficio può essere ottenuto con un certo grado di fusione (dati limitati su un numero molto limitato di pazienti), questo grado ottimale di fusione è difficile da definire e mantenere durante l’esercizio (cambiamenti nella frequenza cardiaca e dell’intervallo PR).
La stimolazione ventricolare sinistra isolata è un’opzione interessante, in particolare se il dispositivo impiantato è un pacemaker CRT. In effetti, può essere eseguito utilizzando un pacemaker a doppia camera convenzionale senza impianto di piombo ventricolare destro che aumenta il rapporto costo / efficacia e riduce il rischio di complicanze. Tuttavia, nei pazienti dipendenti dal pacemaker del blocco AV, impiantare solo un cavo ventricolare sinistro sembra rischioso data la maggiore percentuale di dislocamento del piombo e l’alta soglia di stimolazione. Nei pazienti impiantati con un defibrillatore CRT, l’impianto di un cavo ventricolare destro è essenziale. Tuttavia, la programmazione del dispositivo in una configurazione “solo stimolazione LV” evita il consumo associato alla stimolazione ventricolare destra.
ALGORITMO ADAPTIV-CRT
Come visto in precedenza, l’ideale per ripetute ottimizzazioni della configurazione di stimolazione sarebbe che il dispositivo stesso esegua automaticamente questo. Questa procedura di ottimizzazione non ha costi aggiuntivi ed è “senza sforzo” per il medico e i diversi reparti clinici (ecocardiografia, elettrofisiologia…). Inoltre, la maggior parte delle misurazioni effettuate dal dispositivo sono riproducibili. L’algoritmo di ottimizzazione AdaptivCRT è stato sviluppato con questo obiettivo. La dimostrazione del suo impatto clinico favorevole sui pazienti risincronizzati rimane, tuttavia, non dimostrata.
Principi operativi
L’algoritmo AdaptivCRT è disponibile solo in modalità DDD o DDDR e può essere programmato selezionando: 1) l’impostazione” Adaptive Bi-V “- il dispositivo ottimizza automaticamente i parametri di stimolazione (ritardi AV e VV) – o 2) l’impostazione” Adaptive Bi-V e LV ” – il dispositivo sceglierà tra una configurazione di stimolazione LV pura con fusione e una normale stimolazione biventricolare con ottimizzazione dei ritardi AV e VV. Questo algoritmo può anche essere disattivato programmando 3)”CRT non adattivo”.
Questo algoritmo non porta mai all’uso di valori estremi di ritardi AV o VV. Per la funzione AdaptivCRT, possibili ritardi AV rilevati variano tra 80 ms e 140 ms. Possibili ritardi AV ritmo variano tra 100 ms e 180 ms. La gamma di temporizzazione per i ritardi VV intraventricolare varia da 0 ms a 40 ms (pre-eccitazione sinistra o destra).
La funzione operativa di AdaptivCRT si basa sulla valutazione regolare di 1) il tempo di conduzione atrio-ventricolare, che corrisponde al ritardo tra l’EGM registrato dal cavo atriale destro e l’EGM registrato dal cavo ventricolare destro; 2) la larghezza dell’onda P, che corrisponde al ritardo tra l’EGM atriale registrato sul canale bipolare del cavo atriale destro e la fine dell’EGM atriale registrata dal canale d’urto; 3) la larghezza del complesso QRS che corrisponde al ritardo tra l’EGM rilevata dal bipolo ventricolare destro e la fine dell’EGM registrata sul canale d’urto.
L’algoritmo valuta la conduzione atrio-ventricolare intrinseca del paziente ogni minuto e determina se l’intervallo AV del paziente è normale o prolungato. La misurazione dell’intervallo AV viene eseguita estendendo il ritardo AV rilevato e ritmato a 300 ms per consentire la conduzione intrinseca. In assenza di evento ventricolare condotto spontaneo per più di 3 cicli consecutivi, viene diagnosticata una conduzione AV prolungata e l’intervallo di tempo tra le misurazioni dell’intervallo AV raddoppia (ad esempio, 2 min, 4 min, 8 min… e così via fino a raggiungere un massimo di 16 ore).
Le misurazioni dell’onda P e della larghezza QRS sono programmate ogni 16 ore. Questo intervallo garantisce un campionamento in varie ore del giorno. Durante la misurazione, il dispositivo commuta il canale di registrazione EGM 1 in bobina RV (HVA)/bobina SVC (HVB) (o anodo HVA / atriale in assenza di bobina SVC). Dopo 5 battiti, vengono misurati il ritardo tra l’atriale e l’EGMs ventricolare, la larghezza dell’onda P e la larghezza del QRS.
La prima misurazione dell’onda P e della larghezza QRS è prevista 30 minuti dopo l’impianto. Dopo l’impianto, l’onda P e la larghezza QRS possono essere misurati in qualsiasi momento programmando il parametro AdaptivCRT.
Se il parametro AdaptivCRT è impostato su ” Adaptiv Bi-V e LV”, può passare automaticamente tra la modalità auto BIV e LV. Il paziente viene stimolato in puro LV modalità, se le seguenti condizioni sono rispettate: 1) la frequenza cardiaca del paziente deve essere minore o uguale a 100 bpm; 2) il ritardo di conduzione tra spontanea atriale ASSEMBLEA straordinaria e spontanea ventricolare ASSEMBLEA straordinaria deve essere pari o inferiore a 200 ms; 3) il ritardo di conduzione tra il ritmo atriale ASSEMBLEA straordinaria e spontanea ventricolare ASSEMBLEA straordinaria deve essere minore o uguale a 250 ms.
Se uno di questi criteri non viene trovato, il paziente viene stimolato in modalità biventricolare.
Dettagli della funzione operativa dell’algoritmo
L’esatto funzionamento di questo algoritmo è relativamente confidenziale.
In una prima fase, il dispositivo valuta la conduzione intrinseca per determinare se l’intervallo AV di un paziente è normale o prolungato. Gli intervalli AV normali sono definiti come meno di 200 ms per gli intervalli a frequenza atriale e meno di 250 ms per gli intervalli a ritmo atriale.
In presenza di un tempo di conduzione AV normale e se la frequenza cardiaca del paziente è inferiore a 100bpm, il dispositivo utilizzerà la modalità di stimolazione LV adattativa (solo LV pace). La tempistica del ritmo LV viene regolata automaticamente in base alla misurazione dell’intervallo AV intrinseco che si verifica ogni minuto.
Se il tempo di conduzione AV del paziente supera i 133,3 ms, la stimolazione LV avviene a circa il 70% dell’intervallo AV intrinseco.
Se il tempo di conduzione AV è inferiore a 133,3 ms, la stimolazione LV verrà erogata 40 ms prima del QRS intrinseco (ritardo AV calcolato – 40 ms).
Quando gli intervalli AV intrinseci sono prolungati, o quando la frequenza cardiaca del paziente è superiore a 100 bpm, o se una perdita di acquisizione LV è confermata da LV Capture management (LVCM), la modalità BiV adattiva funzionerà.
Il ritardo AV sarà quindi calcolato come segue:
- Dopo un evento atriale rilevato, il ritardo AV viene regolato al ritmo 40 ms dopo la fine dell’onda P (misurata sul canale dello shock) ma almeno 50 ms prima dell’inizio del QRS intrinseco.
- Dopo un evento atriale ritmato, il ritardo AV viene regolato al ritmo 30 ms dopo la fine dell’onda P (misurata sul canale dello shock) ma almeno 50 ms prima dell’inizio del QRS intrinseco durante il ritmo atriale (timing tra lo stimolo atriale e l’EGM bipolare del ventricolo destro).
Durante la stimolazione BiV adattiva, il ritardo VV ottimale verrà detratto dalla larghezza QRS.
Se la durata QRS (timing tra l’EGM RV bipolare e la fine dell’EGM QRS sul canale shock) è compresa tra 50 ms e 150 ms, l’LV sarà pre-eccitato. Se la larghezza QRS è compresa tra 150 e 180 ms, viene impostata una pre-eccitazione ventricolare destra. Se la larghezza QRS non è compresa tra 50 e 180 ms, verrà utilizzata una pre-eccitazione LV o RV di 10 ms.
I tempi di conduzione AV e la larghezza dell’onda P saranno utilizzati anche per ottimizzare il ritardo VV. Se il tempo di conduzione AV durante il ritmo atriale spontaneo è più lungo della larghezza dell’onda P, il ritardo VV verrà impostato su 0 ms.