2.1:原子理論の進化
十九世紀後の原子理論
物質が原子で構成されていた場合、原子は何で構成されていましたか? それらは最小の粒子でしたか、それとももっと小さいものがありましたか? 1800年代後半、このような問題に興味を持った多くの科学者が低圧ガス中で生成される可能性のある放電を調査し、英国の物理学者J.J.Thomsonが陰極線管を使用して行った最も重要な発見を行った。 この装置は密閉されたガラス管で構成され、そこからほとんどすべての空気が除去され、管には二つの金属電極が含まれていた。 電極間に高電圧を印加すると,それらの間に陰極線と呼ばれる可視ビームが現れた。 このビームは正電荷に向かって偏向され、負電荷から離れ、電極に異なる金属を使用したときに同じ特性を持つ同じ方法で生成された。 同様の実験では、光線は同時に印加された磁場によって偏向され、偏向の程度と磁場強度の測定は、Thomsonが陰極線粒子の電荷対質量比を計算することを可 これらの測定の結果は、これらの粒子が原子よりもはるかに軽いことを示した(図\(\PageIndex{1}\))。P>
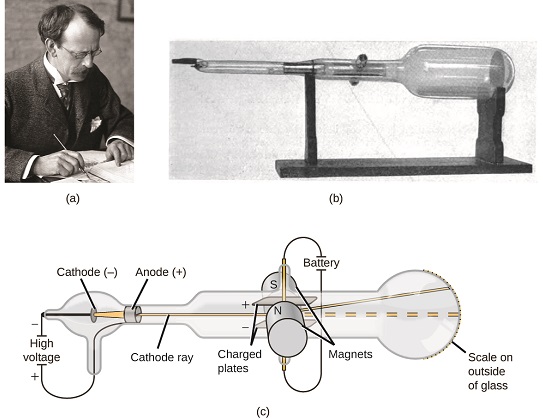
図\(\PageIndex{5}\):(a)J.J.Thomsonは陰極線管で可視ビームを生成しました。 (b)これは、1897年にFerdinand Braunによって発明された初期の陰極線管です。 (c)陰極線では、ビーム(黄色で示されている)は陰極から来、管の端で蛍光スケールの方に陽極を過ぎて加速されます。 印加された電場と磁場による同時偏向は,Thomsonが陰極線を構成する粒子の質量電荷比を計算することを可能にした。 (クレジットa:ノーベル財団による作品の修正、クレジットb:オイゲン-ネスパーによる作品の修正、クレジットc:”Kurzon”/ウィキメディア-コモンズによる作品の修正)。
彼の観察に基づいて、ここでトムソンが提案したものであり、なぜ:粒子は正の(+)電荷によって引き付けられ、負の(−)電荷によってはじかれるので、負 当時は議論の余地があったが、トムソンのアイデアは徐々に受け入れられ、彼の陰極線粒子は、原子の千倍以上の質量を持つ負に帯電した亜原子粒子である電子と呼ばれるものである。 「電子」という用語は、1891年にアイルランドの物理学者George Stoneyによって「electric ion」から造語されました。”
1909年、アメリカの物理学者Robert A.Millikanによって”オイルドロップ”実験によって電子に関するより多くの情報が発見されました。 Millikanは微視的な油滴を作成しましたが、これは摩擦によって形成されるか、またはX線を使用して電気的に帯電する可能性があります。 これらの液滴は最初は重力のために落ちましたが、それらの下向きの進行は、装置内の低い電界によって減速または逆転することさえできました。 電界強度を調整し、慎重な測定と適切な計算を行うことによって、Millikanは個々の滴の電荷を決定することができました(図\(\PageIndex{2}\))。
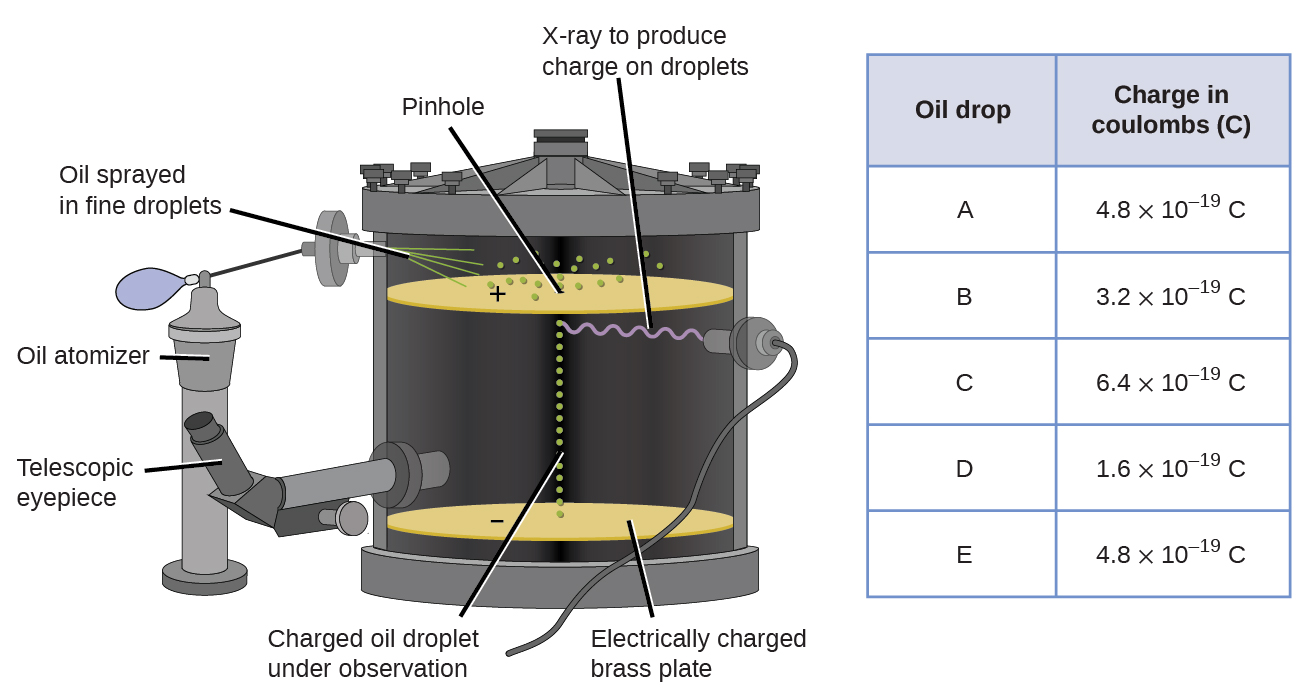
Millikanが収集した電荷データを見ると、油滴の電荷は常に特定の電荷の倍数であることを認識している可能性があります,1.6\(\times\)10—19C.Millikanは、この値は、基本的な電荷でなければならないと結論付けました—単一の電子の電荷-一つの電子の過剰による彼の測定された電荷を持つ(1回1.6\(\times\)10-19C)、2個の電子(2回1.6\(\times\)10-19C)、3個の電子(3回1.6\(\times\)10-19C)などが与えられた油滴上にある。 電子の電荷はミリカンの研究によって知られており、トムソンの研究によって電荷と質量の比はすでに知られていた(1.759\(\times\)1011C/kg)ので、電子の質量も決定するために簡単な計算しか必要としなかった。
\
科学者たちは、ダルトンが信じていたように原子が不可分ではないことを確立し、Thomson、Millikanなどの仕事のために、負の亜原子粒子—電子—の電荷と質量が知られていた。 しかし、原子の正に帯電した部分はまだよく理解されていませんでした。 1904年、トムソンは原子の”plum pudding”モデルを提案し、すべての原子が電気的に中性であるため、電子が埋め込まれた形で等しい量の負電荷を持つ正に荷電した質量を記述した。 1903年に長岡半太郎によって提案された競合モデルは、電子のハローで囲まれた正に帯電した球からなる土星のような原子を仮定していた(図\(\PageIndex{3}\))。
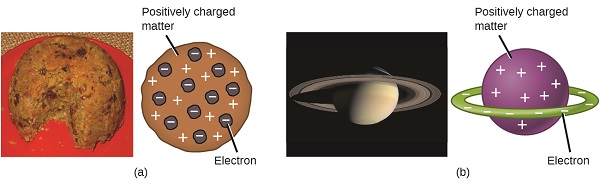
図\(\PageIndex{7}\):(a)トムソンは、原子がプラムプディング、埋め込まれたレーズン(”プラム”)と湿ったケーキからなる英国のデザートに似ていることを示唆しました。 (b)長岡は、原子が土星の惑星に似ており、正の”惑星”を囲む電子の環を持つことを提案した。”(クレジットa:”Man vyi”/ウィキメディア-コモンズによる作品の変更、クレジットb:”NASA”/ウィキメディア-コモンズによる作品の変更)。
原子を理解する上での次の主要な開発は、主にカナダとイギリスで彼の科学的なキャリアを過ごしたニュージーランドの物理学者アーネスト-ラザフォード 彼は、ラジウムの放射性崩壊によって生成された高速、正に帯電したアルファ粒子(α粒子)のビームを使用して一連の実験を行った。α粒子は二つの陽子と二つの中性子からなる(あなたは核化学の章で放射性崩壊についての詳細を学びます)。 ラザフォードとその同僚のハンス・ガイガー(後にガイガーカウンターで有名)とアーネスト・マースデンは、放射線の大部分を吸収するために鉛ブロックに埋め込まれたα粒子のビームを、非常に薄い金箔で狙い、α粒子が当たったところで短時間光る発光スクリーンを用いてα粒子の散乱を調べた。彼らは何を発見しましたか?
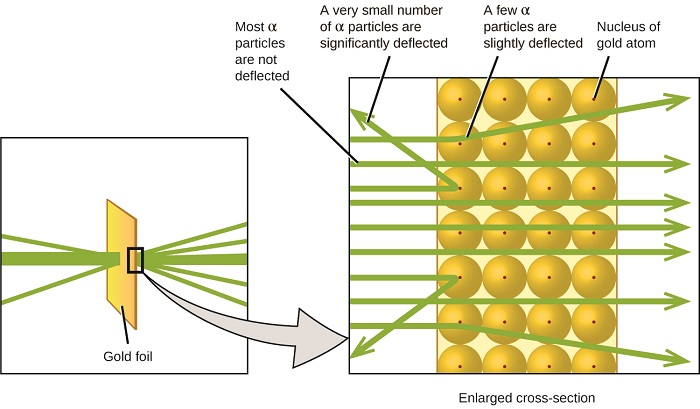
彼らは何を発見しましたか? ほとんどの粒子は、全く偏向されることなく、箔を通って右に通過しました。 しかし、いくつかはわずかに転用され、非常に小さな数はソースに向かってほぼまっすぐに偏向されました(図\(\PageIndex{4}\))。 ラザフォードは、これらの結果を見つけることを説明しました:”それは今まで私の人生で私に起こった最も信じられないほどの出来事でした。 それはあなたがティッシュペーパーの部分で15インチのシェルを発射し、それが戻ってきて、あなたを打つかのようにほぼ信じられないほどだった”1(p.68)。
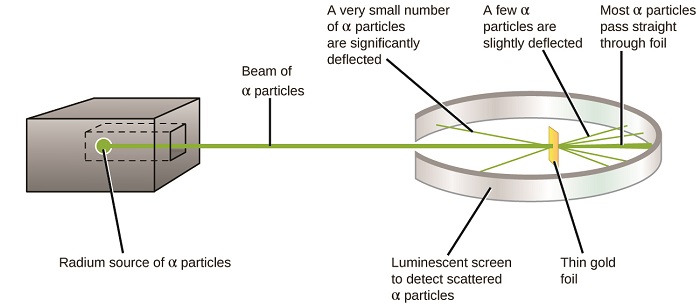
図\(\PageIndex{8}\):ガイガーとラザフォードは、金箔の部分でα粒子を発射し、それらの粒子がどこに行ったかを検出しました,彼らの実験のこの模式図に示 粒子のほとんどは箔をまっすぐに通過したが、いくつかはわずかに偏向され、非常に少数は有意に偏向された。
ここでラザフォードが推測したものです:動きの速いα粒子のほとんどは金原子を透過しないので、原子内の本質的に空の空間を通過したに違いありません。 アルファ粒子は正に帯電しているので、別の正電荷(電荷が互いに反発するような)に遭遇したときに偏向が生じた。 同様の電荷が互いに反発するので、経路を突然変化させたいくつかの正に帯電したα粒子は、非常に集中した正電荷を有する別の物体に衝突するか、 偏向は時間のほんの一部を発生したので、この電荷は金箔内のわずかなスペースを占有しただけであった。 このような一連の実験を詳細に分析すると、ラザフォードは2つの結論を出しました:
- 原子が占める体積は、大量の空のスペースで構成されていなければなりません。
- 小さく、比較的重く、正に帯電した体、核は、各原子の中心になければなりません。
この分析により、ラザフォードは原子が非常に小さく、正に荷電した核で構成され、原子の質量の大部分が負に荷電した電子に囲まれて集中し、原子が電気的に中性になるモデルを提案した(図\(\PageIndex{5}\))。
図\(\PageIndex{9}\):α粒子は、はるかに重い正に帯電した金の核と衝突するか、または近くを通過するときにのみ偏向されます。 核は原子の大きさに比べて非常に小さいため、偏向されるα粒子は非常に少ない。 大部分は、急速に移動する粒子を偏向させるには軽すぎる電子によって占められている比較的大きな領域を通過する。
さらに多くの実験の後、ラザフォードはまた、他の元素の核が”ビルディングブロック”として水素核を含むことを発見し、彼はこのより基本的な粒子を陽子、核に見られる正に荷電した亜原子粒子と命名した。 あなたが次に学ぶ一つの追加で、一世紀以上前に提案された原子のこの核モデルは、今日でもまだ使用されています。別の重要な発見は、同位体の発見でした。
もう一つの重要な発見は、同位体の発見でした。 初期の1900の間に、科学者たちは、放射性鉱石からそれらを単離、新しい元素であると思われるいくつかの物質を同定しました。 例えば、トリウムの放射性崩壊によって生成された「新しい元素」は、最初にメソトリウムという名前を与えられました。 しかし、より詳細な分析は、メソリウムは異なる原子質量を有するにもかかわらず、ラジウム(別の崩壊生成物)と化学的に同一であることを示した。 この結果は、他の元素についても同様の発見とともに、イギリスの化学者Frederick Soddyは、元素が化学的に区別できない異なる質量を持つ原子の種類を持つこ これらの異なるタイプは同位体と呼ばれ、質量が異なる同じ元素の原子です。 ソディはこの発見により1921年にノーベル化学賞を受賞した。
1つのパズルが残っていました:核は原子の質量のほぼすべてを含んでいることが知られていましたが、陽子の数はその質量の半分以下しか提供していませんでした。 核内の中性粒子の存在を含む、残りの質量を構成するものを説明するために、異なる提案がなされた。 ご想像のとおり、非荷電粒子の検出は非常に困難であり、ジェームズ-チャドウィックが陽子とほぼ同じ質量を持つ中性子、非荷電、亜原子粒子の証拠を見つ 中性子の存在はまた、同位体を説明した:彼らは中性子の数が異なるため、質量が異なるが、それらは陽子の数が同じであるため、化学的に同一である。 これについては、この単元の後半で詳しく説明します。