5.3: Chemistry Chemistry
Chemistry brugte enkle diagrammer (nu kaldet Chemistry Chemistry Chemistry) for at holde styr på, hvor mange elektroner der var til stede i den yderste eller valensskal af et givet atom. Atomets kerne, dvs.kernen sammen med de indre elektroner, er repræsenteret af det kemiske symbol, og kun valenselektronerne tegnes som prikker omkring det kemiske symbol. Således kan de tre atomer, der er vist i Figur 1 fra elektroner og Valens, repræsenteres af følgende:
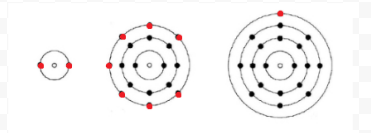

Hvis atomet er et ædelgasatom, er to alternative procedurer mulige. Enten kan vi betragte atomet som nulvalenselektroner, eller vi kan betragte den yderste fyldte skal som valensskallen. De første tre ædelgasser kan således skrives som:
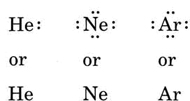
eksempel \(\Sideindeks{1}\): uvis strukturer
tegn uvis diagrammer for et atom af hvert af følgende elementer: Li, N, F, Na
opløsning
Vi finder fra det periodiske bord inde i frontdækslet, at Li har et atomnummer på 3. Den indeholder således tre elektroner, en mere end ædelgassen He. Dette betyder, at den yderste, eller Valens, skal kun indeholder en elektron, og Det Skæve diagram er

efter den samme begrundelse har N syv elektroner, fem mere end han, mens F har ni elektroner, syv mere end han, hvilket giver
![]()
Na har ni flere elektroner end han, men otte af dem er i kernen, svarende til de otte elektroner i den yderste skal af Ne. Da Na kun har 1 mere elektron end Ne, er dets Luvdiagram
![]()
Bemærk fra det foregående eksempel, at uvis-diagrammerne for alkalimetallerne er identiske bortset fra deres kemiske symboler. Dette stemmer fint overens med den meget lignende kemiske opførsel af alkalimetallerne. På samme måde ser diagrammer for alle elementer i andre grupper, såsom alkaliske jordarter eller halogener, det samme ud.
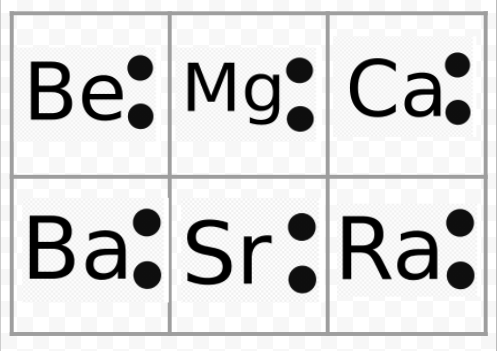
Livis-diagrammerne kan også bruges til at forudsige elementernes valenser. Et atoms valenser var lig med antallet af elektroner i dets valensskal eller antallet af elektroner, som skulle føjes til valensskallen for at opnå den elektroniske skalstruktur af den næste ædelgas. Som et eksempel på denne ide skal du overveje elementerne Be og O. deres Livsdiagrammer og de af ædelgasserne He og Ne er

Når vi sammenligner Be med He, ser vi, at førstnævnte har yderligere to elektroner og derfor skal have en valens på 2. Elementet O kan forventes at have en valens på 6 eller en valens på 2, da det har seks valenselektroner—to mindre end Ne. Ved hjælp af valensregler udviklet på denne måde var han i stand til at redegøre for den regelmæssige stigning og fald i abonnementerne på forbindelserne i tabellen, der findes i Valensafsnittet, og gengivet her. Derudover var han i stand til at tegne sig for mere end 50 procent af formlerne i tabellen. (De, der er enige med hans ideer, er skyggefulde i farve i tabellen. Du ønsker måske at henvise til denne tabel nu og kontrollere, at nogle af de angivne formler følger) Hans succes i denne forbindelse gav en klar indikation af, at elektroner var den vigtigste faktor i at holde atomer sammen, når molekyler dannes.
På trods af disse succeser er der også vanskeligheder at finde i Levis’ teorier, især for elementer ud over calcium i det periodiske system. Elementet Br (å = 35) har for eksempel 17 flere elektroner end ædelgas Ar (å = 18). Dette får os til at konkludere, at Br har 17 valenselektroner, hvilket gør det akavet at forklare, hvorfor Br ligner Cl og F så tæt, selvom disse to atomer kun har syv valenselektroner.
| Element | Atomic Weight | Hydrogen Compounds | Oxygen Compounds | Chlorine Compounds |
|---|---|---|---|---|
| Hydrogen | 1.01 | H2 | H2O, H2O2 | HCl |
| Helium | 4.00 | None formed | None formed | None formed |
| Lithium | 6.94 | LiH | Li2O, Li2O2 | LiCl |
| Beryllium | 9.01 | BeH2 | BeO | BeCl2 |
| Boron | 10.81 | B2H6 | B2O3 | BCl3 |
| Carbon | 12.01 | CH4, C2H6, C3H8 | CO2, CO, C2O3 | CCl4, C2Cl6 |
| Nitrogen | 14.01 | NH3, N2H4, HN3 | N2O, NO, NO2, N2O5 | NCl3 |
| Oxygen | 16.00 | H2O, H2O2 | O2, O3 | <Cl2O, ClO2, Cl2O7 |
| Fluorine | 19.00 | HF | OF2, O2F2 | ClF, ClF3, ClF5 |
| Neon | 20.18 | None formed | None formed | None formed |
| Sodium | 22.99 | NaH | Na2O, Na2O2 | NaCl |
| Magnesium | 24.31 | MgH2 | MgO | MgCl2 |
| Aluminum | 26.98 | AlH3 | Al2O3 | AlCl3 |
| Silicon | 28.09 | SiH4, Si2H6 | SiO2 | SiCl4, Si2Cl6 |
| Phosphorus | 30.97 | PH3, P2H4 | P4O10, P4O6 | PCl3, PCl5, P2Cl4 |
| Sulfur | 32.06 | H2S, H2S2 | SO2, SO3 | S2Cl2, SCl2, SCl4 |
| Chlorine | 35.45 | HCl | Cl2O, ClO2, Cl2O7 | Cl2 |
| Potassium | 39.10 | KH | K2, K2O2, KO2 | KCl |
| Argon | 39.95 | None formed | None formed | None formed |
| Calcium | 40.08 | CaH2 | CaO, CaO2 | CaCl2 |
| Scandium | 44.96 | Relatively Unstable | Sc2O3 | ScCl3 |
| Titanium | 47.90 | TiH2 | TiO2, Ti2O3, TiO | TiCl4, TiCl3, TiCl2 |
| Vanadium | 50.94 | VH2 | V2O5, V2O3, VO2, VO | VCl4, VCl3, VCl2 |
| Chromium | 52.00 | CrH2 | Cr2O3, CrO2, CrO3 | CrCl3, CrCl2 |
Contributors
-
Ed Vitz (Kutztown University), John W. Han er en af de mest populære i verden, og han er en af de bedste i verden.