Mupirocin Cream
generisk navn: mupirocin calcium
doseringsform: creme
medicinsk gennemgået af Drugs.com. sidst opdateret den 1. januar 2021.
- oversigt
- bivirkninger
- dosering
- professionel
- graviditet
- mere
indikationer og anvendelse til mupirocin creme
Mupirocin creme USP, 2% er indiceret til behandling af sekundært inficerede traumatiske hudlæsioner (op til 10 cm i længden eller 100 cm2 i området) på grund af følsomme isolater af Staphylococcus aureus (S. aureus) og Streptococcus pyogenes (S. pyogenes).
mupirocin creme Dosering og Administration
- kun til topisk brug.
- Påfør en lille mængde Mupirocin creme med en vatpind eller gasbind til det berørte område 3 gange dagligt i 10 dage.
- dæk det behandlede område med gasbind dressing, hvis det ønskes.
- revurder patienter, der ikke viser et klinisk respons inden for 3 til 5 dage.
- Mupirocin creme er ikke til intranasal, oftalmisk eller anden slimhindebrug .
- Anvend ikke Mupirocin creme samtidig med andre lotioner, cremer eller salver .
doseringsformer og styrker
Mupirocin Cream USP, 2% er en hvid creme, der indeholder 20 mg (2% vægt / vægt) mupirocin pr.gram i en olie – og vandbaseret emulsion, leveret i 15 gram og 30 gram rør.
kontraindikationer
Mupirocin creme er kontraindiceret hos patienter med kendt overfølsomhed over for mupirocin eller et eller flere af hjælpestofferne i Mupirocin creme.
advarsler og forsigtighedsregler
alvorlige allergiske reaktioner
systemiske allergiske reaktioner, inklusive anafylaksi, urticaria, angioødem og generaliseret udslæt, er rapporteret hos patienter behandlet med formuleringer af mupirocin, inklusive Mupirocin creme .
øjenirritation
undgå kontakt med øjnene. I tilfælde af utilsigtet kontakt skylles godt med vand.
lokal Irritation
i tilfælde af sensibilisering eller alvorlig lokal irritation fra Mupirocin creme, skal brugen seponeres, og passende alternativ behandling til infektionen indledes.
Clostridium difficile-associeret diarre
Clostridium difficile-associeret diarre (CDAD) er rapporteret ved brug af næsten alle antibakterielle midler og kan variere i sværhedsgrad fra mild diarre til dødelig colitis. Behandling med antibakterielle midler ændrer den normale flora i tyktarmen, hvilket fører til overvækst af C. difficile.C. difficile producerer toksiner A og B, som bidrager til udviklingen af CDAD. Hypertoksinproducerende stammer af C. difficile forårsager øget sygelighed og dødelighed, da disse infektioner kan være ildfaste over for antimikrobiel terapi og kan kræve kolektomi. CDAD skal overvejes hos alle patienter, der har diarre efter brug af antibakterielle lægemidler. Omhyggelig medicinsk historie er nødvendig, da CDAD er rapporteret at forekomme over 2 måneder efter administration af antibakterielle midler.
hvis CDAD er mistænkt eller bekræftet, kan det være nødvendigt at afbryde den igangværende antibakterielle stofbrug, der ikke er rettet mod C. difficile. Passende væske-og elektrolytstyring, proteintilskud, antibakteriel behandling af C. difficile og kirurgisk evaluering bør indledes som klinisk indiceret.
potentiale for mikrobiel overvækst
som med andre antibakterielle produkter kan langvarig brug af Mupirocin-creme resultere i overvækst af ikke-observerbare mikroorganismer, herunder svampe .
risiko forbundet med Mucosal brug
Mupirocin creme er ikke formuleret til brug på slimhindeoverflader. En separat formulering, mupirocin calcium nasal salve, er tilgængelig til intranasal brug.
bivirkninger
følgende bivirkninger diskuteres mere detaljeret i andre afsnit af mærkningen:
- alvorlige allergiske reaktioner
- øjenirritation
- lokal Irritation
- Clostridium difficile-associeret diarre
kliniske forsøg erfaring
da kliniske forsøg udføres under vidt forskellige forhold, observeres bivirkningshastigheder i de kliniske forsøg, der af et lægemiddel kan ikke sammenlignes direkte med satser i de kliniske forsøg med et andet lægemiddel og afspejler muligvis ikke de satser, der er observeret i praksis.
i 2 randomiserede, dobbeltblinde, dobbelt-dummy forsøg blev 339 forsøgspersoner behandlet med topisk Mupirocin creme plus oral placebo. Bivirkninger forekom hos 28 (8,3%) forsøgspersoner. Følgende bivirkninger blev rapporteret af mindst 1% af forsøgspersonerne i forbindelse med brugen af Mupirocin creme i kliniske forsøg: hovedpine (1, 7%), udslæt (1, 1%) og kvalme (1, 1%).
andre bivirkninger, der forekom hos mindre end 1% af forsøgspersonerne, var: mavesmerter, forbrænding på applikationsstedet, cellulitis, dermatitis, svimmelhed, kløe, sekundær sårinfektion og ulcerøs stomatitis.
i et understøttende forsøg til behandling af sekundært inficeret eksem blev 82 forsøgspersoner behandlet med Mupirocin creme. Forekomsten af bivirkninger var som følger: kvalme (4, 9%), hovedpine og forbrænding på applikationsstedet (3, 6% hver), kløe (2, 4%) og 1 rapporterer hver af mavesmerter, blødning sekundært til eksem, smerter sekundært til eksem, nældefeber, tør hud og udslæt.
erfaring efter markedsføring
ud over bivirkninger rapporteret fra kliniske forsøg er følgende reaktioner blevet identificeret under brug efter markedsføring af Mupirocin Cream. Da de rapporteres frivilligt fra en population af ukendt størrelse, kan der ikke foretages skøn over hyppigheden. Disse reaktioner er valgt til inklusion på grund af en kombination af deres alvorlighed, rapporteringshyppighed eller potentielle årsagssammenhæng med Mupirocin creme.
immunsystemet
systemiske allergiske reaktioner, herunder anafylaksi, urticaria, angioødem og generaliseret udslæt .
anvendelse i specifikke populationer
graviditet
Risikooversigt
der er utilstrækkelige humane data til at fastslå, om der er en lægemiddelassocieret risiko med Mupirocin creme hos gravide kvinder. Systemisk absorption af mupirocin gennem intakt human hud er minimal efter topisk administration af Mupirocin creme . Der blev ikke observeret udviklingstoksicitet hos rotter eller kaniner behandlet med mupirocin subkutant under organogenese i doser på henholdsvis 160 eller 40 mg pr.kg pr. dag (22 og 11 gange den humane topiske dosis baseret på beregninger af dosis divideret med hele kropsoverfladearealet).
den estimerede baggrundsrisiko for større fødselsdefekter og abort for den angivne population er ukendt. Den estimerede baggrundsrisiko i den amerikanske generelle befolkning for større fødselsdefekter er 2% til 4%, og abort er 15% til 20% af klinisk anerkendte graviditeter.
data
Dyredata: Der er udført udviklingstoksicitetsundersøgelser med mupirocin administreret subkutant til rotter og kaniner i doser op til 160 mg pr.kg pr. dag under organogenese. Denne dosis er henholdsvis 22 og 43 gange den humane topiske dosis (ca.60 mg mupirocin pr. dag) baseret på beregninger af dosis divideret med hele kropsoverfladearealet. Maternel toksicitet blev observeret (vægttab/nedsat vægtøgning og reduceret fodring) hos begge arter uden tegn på udviklingstoksicitet hos rotter. Hos kaniner udelukkede overdreven maternel toksicitet ved den høje dosis evaluering af føtale resultater. Der var ingen udviklingstoksicitet hos kaniner ved 40 mg pr.kg pr. dag, 11 gange den humane topiske dosis baseret på beregninger af dosis divideret med hele kropsoverfladearealet.
Mupirocin administreret subkutant til rotter i et præ – og postnatalt udviklingsstudie (doseret under sen drægtighed gennem amning) var forbundet med nedsat Afkoms levedygtighed i den tidlige postnatale periode i en dosis på 106.7 mg pr. kg i tilfælde af irritation på injektionsstedet og / eller subkutan blødning. Denne dosis er 14 gange den humane topiske dosis baseret på beregninger af dosis divideret med hele kropsoverfladearealet. Det ikke-observerede bivirkningsniveau i dette studie var 44,2 mg pr. kg pr.dag, hvilket er 6 gange den humane topiske dosis.
amning
Risikooversigt
det vides ikke, om mupirocin er til stede i modermælk, har virkninger på det ammede barn eller har virkninger på mælkeproduktionen. Imidlertid forventes amning ikke at resultere i eksponering af barnet for lægemidlet på grund af den minimale systemiske absorption af mupirocin hos mennesker efter topisk administration af Mupirocin creme . De udviklingsmæssige og sundhedsmæssige fordele ved amning bør overvejes sammen med moderens kliniske behov for Mupirocin creme og eventuelle potentielle bivirkninger på det ammede barn fra Mupirocin creme eller fra den underliggende maternelle tilstand.
kliniske overvejelser
for at minimere oral eksponering af lægemidlet for børn skal et bryst og / eller brystvorte, der behandles med Mupirocin-creme, vaskes grundigt inden amning.
pædiatrisk brug
sikkerheden og effektiviteten af mupirocin creme er blevet etableret i aldersgrupperne 3 måneder til 16 år. Anvendelse af Mupirocin creme i disse aldersgrupper understøttes af beviser fra passende og velkontrollerede forsøg med Mupirocin creme hos voksne med yderligere data fra 93 pædiatriske forsøgspersoner undersøgt som en del af de pivotale forsøg med voksne .
geriatrisk anvendelse
i 2 tilstrækkelige og velkontrollerede forsøg blev 30 personer ældre end 65 år behandlet med Mupirocin creme. Der blev ikke observeret nogen samlet forskel i effekten eller sikkerheden af Mupirocin creme i denne patientpopulation sammenlignet med den, der blev observeret hos yngre patienter.
Mupirocin creme beskrivelse
Mupirocin creme USP, 2% indeholder dihydrat krystallinsk calcium hemi-salt af RNA syntetaseinhibitor antibakteriel, mupirocin. Kemisk set er det (aE,2S,3R,4R, 5S)-5-tetrahydro-3,4-dihydroksy-l-methyl-2H-pyran-2-crotonsyre, ester med 9-hydroksynonansyre, calciumsalt (2:1), dihydrat.
molekylformlen for mupirocin-calcium er (C26H43O9 )2CA-liter 2H2O, og molekylvægten er 1075,3. Molekylvægten af mupirocinfri syre er 500,6. Strukturformlen for mupirocin calcium er:
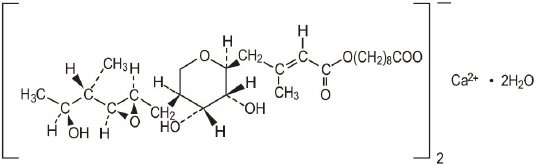
hvert gram Mupirocin creme indeholder 20 mg (2% vægt/vægt) mupirocin svarende til 21,5 mg (2,15% vægt/vægt) mupirocin calcium. The inactive ingredients are benzyl alcohol, cetomacrogol 1000, cetyl alcohol, mineral oil, phenoxyethanol, purified water, stearyl alcohol, and xanthan gum.
Mupirocin Cream – Clinical Pharmacology
Mechanism of Action
Mupirocin is an RNA synthetase inhibitor antibacterial .
Pharmacokinetics
Absorption
Systemic absorption of mupirocin through intact human skin is minimal. Den systemiske absorption af mupirocin blev undersøgt efter påføring af Mupirocin creme 3 gange dagligt i 5 dage på forskellige hudlæsioner større end 10 cm i længden eller 100 cm2 i området hos 16 voksne (i alderen 29 Til 60 år) og 10 børn (i alderen 3 til 12 år). En vis systemisk absorption blev observeret som det fremgår af påvisning af metabolitten, moninsyre, i urinen. Data fra dette forsøg indikerede hyppigere forekomst af perkutan absorption hos børn (90% af forsøgspersonerne) sammenlignet med voksne (44% af forsøgspersonerne); de observerede urinkoncentrationer hos børn (0,07 til 1.3 mcg pr. mL) ligger inden for det observerede interval (0,08 til 10,03 mcg pr.mL ) hos den voksne befolkning. Generelt synes graden af perkutan absorption efter flere doser at være minimal hos voksne og børn.
effekten af samtidig anvendelse af Mupirocin creme med andre topiske produkter er ikke undersøgt .
Elimination
i et forsøg udført med 7 raske voksne mandlige forsøgspersoner var eliminationshalveringstiden efter intravenøs administration af mupirocin 20 Til 40 minutter for mupirocin og 30 til 80 minutter for moninsyre.
metabolisme: Efter intravenøs eller oral administration metaboliseres mupirocin hurtigt. Hovedmetabolitten, moninsyre, udviser ingen antibakteriel aktivitet.
udskillelse: Moninsyre elimineres overvejende ved renal udskillelse.
Mikrobiologi
Mupirocin er et RNA-syntetaseinhibitor antibakterielt produceret ved fermentering ved anvendelse af organismen Pseudomonas fluorescens.
virkningsmekanisme
Mupirocin hæmmer bakteriel proteinsyntese ved reversibel og specifikt binding til bakteriel isoleucyl-transfer RNA (tRNA) syntetase.
Mupirocin er bakteriedræbende ved koncentrationer opnået ved topisk administration. Mupirocin er stærkt proteinbundet (større end 97%), og virkningen af sårudskillelser på mupirocins minimale hæmmende koncentrationer (MICs) er ikke bestemt.
resistens
når mupirocinresistens opstår, skyldes det produktionen af en modificeret isoleucyl-tRNA-syntetase eller erhvervelsen af ved genetisk overførsel et plasmid, der medierer en ny isoleucyl-tRNA-syntetase. Plasmidmedieret resistens på højt niveau (mic-Kurt 512 mcg/mL) er rapporteret i stigende antal isolater af S. aureus og med højere frekvens i koagulase-negative stafylokokker. Mupirocinresistens forekommer med større frekvens i methicillinresistent end methicillin-modtagelige stafylokokker.
krydsresistens
på grund af dets virkningsmåde viser mupirocin ikke krydsresistens med andre klasser af antimikrobielle midler.
antimikrobiel aktivitet
Mupirocin har vist sig at være aktiv mod følsomme isolater af S. aureus og S. pyogenes, både in vitro og i kliniske forsøg . Følgende in vitro-data er tilgængelige, men deres kliniske betydning er ukendt. Mupirocin er aktiv mod de fleste isolater af Staphylococcus epidermidis.
Følsomhedstestmetoder
mupirocinresistens på højt niveau (larg 512 mcg / mL) kan bestemmes ved hjælp af standard diskdiffusions-eller bouillonmikrofortyndingstest.1,2 på grund af forekomsten af mupirocinresistens i methicillinresistent S. aureus (MRSA), er det hensigtsmæssigt at teste MRSA-populationer for mupirocinfølsomhed inden brug af mupirocin ved hjælp af en standardiseret metode.3,4,5
ikke-klinisk Toksikologi
carcinogenese, mutagenese, nedsat fertilitet
Der er ikke udført langtidsstudier med dyr til vurdering af det karcinogene potentiale af mupirocincalcium.
resultater af følgende undersøgelser udført med mupirocin calcium eller mupirocin natrium in vitro og in vivo indikerede ikke et potentiale for genotoksicitet: rotte primær hepatocyt uplanlagt DNA-syntese, sedimentanalyse for DNA-strengbrud, Salmonella reversionstest (Ames), Escherichia coli mutationsassay, metafaseanalyse af humane lymfocytter, muselymfomassay og knoglemarvsmikronukleiassay hos mus.
i en fertilitets – / reproduktionsundersøgelse (med dosering gennem amning) resulterede mupirocin subkutant til han-og hunrotter i doser op til 100 mg pr.kg pr. dag, hvilket er 14 gange den humane topiske dosis (ca. 60 mg mupirocin pr. dag) baseret på beregninger af dosis divideret med hele kropsoverfladearealet, ikke i nedsat fertilitet eller nedsat reproduktionsevne, der kan tilskrives mupirocin.
kliniske studier
effekten af topisk Mupirocincreme til behandling af sekundært inficerede traumatiske hudlæsioner (f. eks. 10 cm i længden eller 100 cm2 i det samlede areal) blev sammenlignet med oral cephaleksin i 2 randomiserede, dobbeltblinde, dobbelt-dummy kliniske forsøg. Protokolpopulationerne (voksne og pædiatriske forsøgspersoner inkluderet) var 96,1% for mupirocin creme (n = 231) og 93,1% for oral cephaleksin (n = 219). Patogenudryddelsesgraden ved opfølgning i per-protokolpopulationerne var 100% for både Mupirocincreme og oral cephaleksin.
Pediatrics
der var 93 pædiatriske forsøgspersoner i alderen 2 uger til 16 år tilmeldt pr.protokol i de sekundært inficerede hudlæsionsforsøg, skønt kun 3 var yngre end 2 år i befolkningen behandlet med Mupirocin creme. Forsøgspersoner blev randomiseret til enten 10 dages topisk Mupirocin-creme 3 gange dagligt eller 10 dages oral cephaleksin (250 mg 4 gange dagligt for forsøgspersoner større end 40 kg eller 25 mg pr.kg pr. dag oral suspension i 4 opdelte doser for forsøgspersoner mindre end eller lig med 40 kg). Den kliniske effekt ved opfølgning (7 til 12 dage efter behandlingen) i per-protokolpopulationerne var 97,7% (43 af 44) for mupirocin creme og 93,9% (46 af 49) for Cephaleksin.
- klinisk og Laboratoriestandardinstitut (CLSI). Præstationsstandarder for antimikrobiel følsomhedstest; seksogtyvende Informationstilskud. CLSI-dokument M100-S26. Klinisk og laboratorium standarder Institut, 950 Vest Valley Rd., Suite 2500, Pa 19087, USA, 2016.
- Patel J, RJ, et al. Mupirocin Modstand. Kliniske Infektionssygdomme. 2009; 49(6):935-41.
- klinisk og Laboratoriestandardinstitut (CLSI). Metoder til fortynding antimikrobielle følsomhedstest for bakterier, der vokser aerobt; godkendt Standard-tiende udgave. CLSI-dokument M07-A10. Klinisk og laboratorium standarder Institut, 950 Vest Valley Road, Suite 2500, Pennsylvania 19087, USA, 2015.
- klinisk og Laboratoriestandardinstitut (CLSI). Ydelsesstandarder for antimikrobielle Diskdiffusions følsomhedstest; godkendt Standard – tolvte udgave. CLSI-dokument M02-A12. Klinisk og laboratorium standarder Institut, 950 Vest Valley Road, Suite 2500, Pennsylvania 19087, USA, 2015.
- Finlay JE, Miller LA, Poupard JA. Fortolkningskriterier til test af stafylokokkers følsomhed over for mupirocin. Antimicrob Agenter Chemother 1997; 41(5):1137-1139.
hvordan leveret/opbevaring og håndtering
Mupirocin Cream er en hvid creme, der indeholder 20 mg (2% vægt/vægt) mupirocin pr.gram i en olie – vandbaseret emulsion.
Mupirocin creme USP, 2% leveres i 15 gram (NDC 16714-055-01) og 30 gram (NDC 16714-055-02) rør.
opbevares ved 20 liter til 25 liter C (68 liter til 77 liter F) . Må ikke nedfryses.
Patientrådgivningsinformation
rådgive patienten om at læse FDA-godkendt patientmærkning (patientinformation).
rådgive patienten om at administrere Mupirocin creme som følger:
- Brug kun Mupirocin creme som anvist af sundhedsudbyderen. Det er kun til ekstern brug. Undgå kontakt med Mupirocin creme med øjnene. Hvis Mupirocin creme kommer i øjnene, skylles grundigt med vand.
- Brug ikke Mupirocin creme i næsen.
- vask dine hænder før og efter påføring af Mupirocin creme.
- brug en gasbind eller bomuldspindel til at påføre en lille mængde Mupirocin creme på det berørte område. Det behandlede område kan om ønsket være dækket af gasbind.
- rapporter til sundhedsudbyderen tegn på lokale bivirkninger. Mupirocin creme skal stoppes, og sundhedsudbyderen kontaktes, hvis irritation, alvorlig kløe eller udslæt opstår.
- rapporter til sundhedsudbyderen eller gå til nærmeste akutrum, hvis der opstår alvorlige allergiske reaktioner, såsom hævelse af læber, ansigt eller tunge eller hvæsende vejrtrækning .
- hvis der ikke ses nogen forbedring på 3 til 5 dage, skal du kontakte sundhedsudbyderen.
fremstillet til: Memphis, TN 38141.
fremstillet af: Taro Pharmaceuticals Inc.
Brampton, Ontario, Canada L6T 1C1.
udstedt: November 2020
5214500
54
| denne patientinformation er godkendt af US Food and Drug Administration. udgivet: November 2020 5214500 54 |
||
| patientinformation mupirocin (mue pir ‘ Oh sin) creme, til topisk brug |
||
| hvad er mupirocin creme?Mupirocin Cream er et receptpligtigt lægemiddel, der anvendes på huden (topisk anvendelse) til behandling af visse hudinfektioner forårsaget af bakterier kaldet Staphylococcus aureus og Streptococcus pyogenes. Det vides ikke, om Mupirocin creme er sikker og effektiv hos børn under 3 måneder. | ||
| Hvem bør ikke bruge Mupirocin creme? Brug ikke mupirocin Cream, hvis:
|
||
| Hvad skal jeg fortælle min sundhedsudbyder, før jeg bruger Mupirocin creme? Før du bruger Mupirocin Cream, fortæl din læge om alle dine medicinske tilstande, herunder hvis du:
Fortæl din læge om alle de lægemidler, du tager, herunder receptpligtig og over-the-counter medicin, vitaminer og naturlægemidler kosttilskud. Bland ikke Mupirocin creme med andre lotioner, cremer eller salver. |
||
hvordan skal jeg bruge mupirocin creme?
|
||
| Hvad er de mulige bivirkninger af Mupirocin creme? Mupirocin creme kan forårsage alvorlige bivirkninger, herunder:
|
||
|
|
|
de mest almindelige bivirkninger af mupirocin creme omfatter:
disse er ikke alle mulige bivirkninger af Mupirocin creme. Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088. |
||
hvordan skal jeg opbevare mupirocin creme?
|
||
| Generelle oplysninger om sikker og effektiv anvendelse af mupirocin creme. lægemidler ordineres undertiden til andre formål end dem, der er anført i en indlægsseddel. Brug ikke mupirocin creme til en tilstand, som den ikke var ordineret til. Giv ikke Mupirocin creme til andre mennesker, selvom de har de samme symptomer, som du har. Det kan skade dem. Du kan bede din apotek eller sundhedsudbyder om oplysninger om Mupirocin creme, der er skrevet til sundhedspersonale. |
||
| Hvad er ingredienserne i Mupirocin creme? aktiv ingrediens: mupirocin calcium inaktive ingredienser: cetomacrogol 1000, cetylalkohol, mineralolie, phenoksyethanol, renset vand, stearylalkohol og gum fremstillet til: Northstar Rksllc, Memphis, TN 38141. Manufactured by: Taro Pharmaceuticals Inc., Brampton, Ontario, Canada L6T 1C1. For more information, call 1-800-206-7821. |
||
PRINCIPAL DISPLAY PANEL – 30 g Tube Carton
NDC 16714-055-02
Rx only
Mupirocin Cream USP
2%
FOR DERMATOLOGIC USE ONLY.
NORTHSTARx®
30 g

| MUPIROCIN mupirocin calcium cream |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
Labeler – NORTHSTAR rk LLC (830546433)
NORTHSTAR rk LLC
ofte stillede spørgsmål
- Kan jeg bruge mupirocin salve til blæseudslæt?
- kan mupirocin helbrede eller hjælpe med eksem?
- kan mupirocin bruges til atleter fod?
- kan mupirocin creme bruges til sengesår?
mere om mupirocin aktuel
- bivirkninger
- under graviditet eller amning
- doseringsinformation
- Sammenlign alternativer
- supportgruppe
- prissætning &kuponer
- Spansk
- 38 anmeldelser
- stof klasse: aktuelle antibiotika
Forbrugerressourcer
- patientinformation
- Mupirocin Nasal (avanceret læsning)
- Mupirocin Aktuel (avanceret læsning)
professionelle ressourcer
- ordineringsinformation
- Mupirocin (professionel patientrådgivning)
- Mupirocin (FDA)
andre mærker Bactroban, Bactroban nasal, centany, centany at, pirnuo
relaterede behandlingsvejledninger
- nasal transport af Staphylococcus aureus
- hud-og strukturinfektion
- sekundære kutane bakterielle infektioner
- Impetigo
- Paronychia
medicinsk ansvarsfraskrivelse