Stor granulær Lymfocytleukæmi som en komplikation af Rheumatoid Arthritis | reumatolog Larra Cl Larsnica
introduktion
Feltys syndrom (FS) er en sjælden systemisk komplikation (mindre end 1%) af rheumatoid arthritis (RA), kendetegnet ved triaden af RA, vedvarende neutropeni (3
) og splenomegali af forskellig størrelse, som kan variere fra subklinisk splenomegali, der kun kan påvises ved billeddannelse, til massiv1 splenomegali. Det forekommer hovedsageligt i langvarige tilfælde med alvorlig ledsygdom og ekstraartikulære manifestationer og har en stærk tilknytning til HLA-DR4-haplotypen (næsten 95% af tilfældene).2 hos 30% -40% af patienterne med FS er der en udvidelse af store granulære lymfocytter (LGL).1 LGL repræsenterer 10% -15% af cirkulerende mononukleære celler og er morfologisk identificeret ved deres store størrelse (15–18 liter), deres runde eller indrykkede kerne og rigelige cytoplasma med acurofile granuler. Fænotypen af disse celler kan være cytotoksisk T-lymfocyt (CD8+, CD57+) eller natural killer (NK) (CD3−, CD8−, CD56+).3 Når ekspansion af LGL er monoklonal og er forbundet med infiltration af knoglemarv og milt af disse celler, kaldes det stor granulær lymfocytleukæmi (LGLL) og betragtes som en kronisk lavgradig lymfoproliferativ lidelse. Dens kliniske præsentation svarer til FS, hvilket fremhæver den øgede modtagelighed for bakterielle infektioner forbundet med neutropeni, anæmi og splenomegali, som også er blevet kaldt “pseudo-Felty”.3,4 klinisk præsentation
en 70-årig pensioneret arbejdstager fra et granitbrud blev diagnosticeret i en alder af 43 med seropositiv RA med involvering af hænder, fødder, knæ og hofter. Han udviklede efterfølgende pneumokoniose og pulmonale reumatoid knuder (Fig. 1), der diagnosticeres som Caplans syndrom. Under sin progression blev han behandlet med NSAID ‘ er, kortikosteroider, guldsalte, cyclosporin og methotreksat. På trods af dette udviklede patienten strukturelle skader i hænder, fødder og hofter, hvilket krævede placering af protese i begge hofter ved henholdsvis 51 og 54 år. I de senere år forblev hans sygdom stabil, behandlet med methotreksat 10 mg ugentligt og lave doser glukokortikoider uden tegn på inflammatorisk ledaktivitet. Han præsenterede’ svanehals ‘ deformiteter i alle fingre og reumatoid knuder på albuerne. For 12 måneder siden udviklede han pludselig feber og smerter i sin højre lyske med efterfølgende septisk chok, hvilket demonstrerede en infektion i højre hofte af Salmonella spp. Glucocorticoider blev suspenderet, og han blev behandlet med langvarig antibiotikabehandling og delvis udskiftning af protesen. Laboratorieundersøgelser viste vedvarende neutropeni på trods af tilbagetrækning af myelotoksiske lægemidler og forbedring af sepsis og nåede 0neutrofiler/mm3. Retrospektivt, når han gennemgik antallet af neutrofiler, havde han lave tællinger et år tidligere, mellem 1800 og 1000/mm3. Resten af blodtal og biokemi var normale. ESR var 80 mm/T og CRP 111 mg/l. han opretholdt høje niveauer af reumatoid faktor (6930u/ml) og anti-CCP (300u / ml) og havde også polyklonal hypergammaglobulinæmi. Antinukleære antistoffer og ekstraherbare nukleare antigener var negative, og komplementniveauerne var inden for normale værdier. HLA-typning viste, at han bar haplotypen DRB1*0404 (DR4), og der blev påvist mild splenomegali (13,7 cm) på abdominal computertomografi.

pneumokoniose og pulmonale rheumatoid knuder.
det perifere blodudstrygning viste lymfocytose af LGL (Fig. 2), som i immunophenotypen svarede Til 42% af de samlede leukocytter med en afvigende fænotype af cytotoksisk T− lymfocyt (CD3+, CD8+, CD5+, CD7+/−, CD4−, CD56-og DR+). Knoglemarvsbiopsien viste 20% af den totale marvcellularitet svarende til den samme klonale ekspansion (bekræftet ved omlejring af det variable område af TCR gamma). Baseret på disse fund blev der stillet en diagnose af LGLL, og behandling med 15 mg ugentlig genstartet på trods af 3 måneder med vedvarende neutropeni (3
), hvilket krævede hyppig administration af granulopoiesisstimulerende faktorer. Han blev efterfølgende behandlet med cyclophosphamid, vincristin og prednison i høje doser. Efter 6 måneders behandling fortsætter neutropeni.
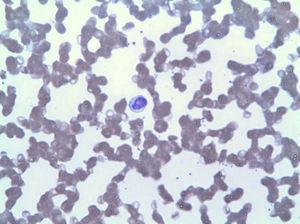
lymfocytose på grund af LGL.
Diskussion
LGLL er en kronisk leukæmi karakteriseret ved udvidelse af LGL monoklonal fænotype af aktiverede cytotoksiske T-lymfocytter eller mindre hyppigt NK-celler.5 Den gennemsnitlige diagnosealder er 60 år, og den er ofte forbundet med autoimmune sygdomme, især RA, men er også blevet beskrevet i ulcerøs colitis, Sj Lutgrens syndrom, lupus erythematosus og multiple1 sklerose. Patienter med RA, der har tilknyttet LGLL, har en klinisk præsentation svarende til FS. De er normalt patienter med langvarig RA, alvorlig ledskade og betydelige konsekvenser og øget hyppighed af ekstra-artikulære manifestationer såsom reumatoid knuder, lymfadenopati, pretibiale mavesår, pleuritis, hudpigmentering, neuropati eller episcleritis.6 patienten havde også en anden sjælden komplikation af RA, reumatoid pneumokoniose eller Caplan ‘ s syndrom, kendetegnet ved udseendet af lungeknuder med histopatologi svarende til typiske reumatoid knuder hos patienter med en historie med erhvervsmæssig eksponering for uorganisk støv, såsom silica, kul eller granit.7 så vidt vi ved, er den foreliggende sag den første, der beskriver præsentationen af Caplan ‘ s syndrom og LGLL hos den samme patient. I de fleste tilfælde er præsentationen LGLL svær neutropeni forbundet med tilbagevendende bakterielle infektioner. De mikroorganismer, der oftest er involveret, er Staphylococcus aureus, Streptococcus spp. og gram-negative baciller. Mindre almindeligt anæmi, feber, nattesved og lever og milt forstørrelse5 kan også ledsage det. Op til en tredjedel af patienterne med LLGG har ingen tilsyneladende RA klinisk aktivitet på diagnosetidspunktet, men opretholder høje niveauer af ESR.6 op til 40% af patienterne med FS har LGL-lymfocytose.7 denne kendsgerning sammen med den kliniske lighed og tilknytning til HLA-DR4 har kraftigt antydet, at FS og LGLL forbundet med RA er udtryk for den samme enhed, der er kendetegnet ved spredning af LGL.8 andre former inkluderer også mildere former såsom reaktiv lymfocytose og infektioner til mere aggressive former for NK5 LGLL. LGLL diagnose er baseret på konstateringen af en monoklonal ekspansion af LGL i perifert blod og knoglemarv med en karakteristisk immunophenotype (CD3+, CD4−, CD8 +, CD16+, CD28− og CD57+). Klonaliteten bekræftes ved at studere reTCR9-genet. Generelt har LGL en kronisk og indolent progression med en gennemsnitlig overlevelse på 10 år.1 i sjældne tilfælde, især når udvidelsen skyldes LGL med NK-fænotype, kan denne leukæmi opføre sig mere aggressivt.5 Den mest almindelige indikation for behandling er tilbagevendende infektioner og sjældnere anæmi, symptomatisk splenomegali eller udseendet af alvorlige B-symptomer B1.førstelinjebehandling i LGLL er immunsuppressive lægemidler alene, specifikt methotreksat (10 mg/uge), cyclosporin A (1-1, 5 mg/kg/2 gange dagligt) eller oral cyclophosphamid (50-100 mg/dag). 50% af patienterne og opnår korrektion af cytopenier, men ikke udrydder leukæmiske celler.1 glukokortikoider kan bruges til at fremskynde responsen, og granulopoiesis-stimulerende faktorer er nyttige i den indledende behandling af neutropeni. Hos ildfaste patienter og hos dem med meget aggressiv præsentationsbehandling med kemoterapiregimer svarende til CHOP (cyclophosphamid, vincristin, doksorubicin og prednison) og andre ordninger for lymfom er blevet forsøgt, men har ikke tydeligt vist deres effektivitet. Andre behandlinger, der er blevet testet, er purinanaloger, Alemtub, splenektomi og allogen knoglemarvstransplantation med variable resultater.3
konklusioner
både FS og LGLL er sjældne komplikationer af RA, som forekommer i langvarig sygdom med betydelig strukturel skade og ekstra-artikulære manifestationer. Hos patienter med langvarig RA og neutropeni bør tilstedeværelsen af klonal proliferation af LGL i perifert blod og/eller knoglemarv udelukkes, hvilket muliggør diagnose af LGLL. Førstelinjebehandling er brugen af immunsuppressive lægemidler, såsom lavdosis methotreksat, og glukokortikoider kan være forbundet med granulopoiesistimulerende faktorer. Andre behandlingsmetoder såsom kemoterapi eller splenektomi har vist variable resultater i nogle ildfaste tilfælde.
etiske oplysninger
beskyttelse af mennesker og dyr. Forfatterne erklærer, at der ikke blev udført forsøg på mennesker eller dyr til denne undersøgelse.
fortrolighed af Data. Forfatterne erklærer, at de har fulgt protokollerne fra deres arbejdscenter om offentliggørelse af patientdata, og at alle patienter, der er inkluderet i undersøgelsen, har modtaget tilstrækkelig information og har givet deres informerede samtykke skriftligt til at deltage i denne undersøgelse.