Homoquiralidad biológica: Uno de los Grandes Misterios

En cada forma de vida en la Tierra, los azúcares son siempre de la mano derecha, y los aminoácidos son siempre zurdo. ¿Qué significa esto y por qué sucede? Este extraño fenómeno involucra moléculas quirales y se conoce como «homoquiralidad».»
Las moléculas quirales son moléculas de la misma fórmula, pero con estructuras ligeramente diferentes. Su mano es un objeto quiral porque no es superponible en su imagen especular; cuando coloca su mano izquierda sobre su derecha, sus pulgares apuntarán en diferentes direcciones. En moléculas orgánicas, cuando cuatro grupos diferentes rodean un carbono central, la molécula tendrá dos formas quirales diferentes llamadas enantiómeros. Estas dos moléculas son imágenes especulares una de la otra, ya que los grupos alrededor del carbono están orientados en diferentes direcciones, como las manos derecha e izquierda. En química, estos compuestos se denominan enantiómeros (o isómeros) R y S. Sin embargo, cuando los aminoácidos o los azúcares son quirales, los científicos los llaman isómeros D y L (los científicos son terribles para nombrar las cosas de manera consistente). D-significa » diestro «y L-significa «zurdo».»

La D y L isómeros normalmente están presentes en una proporción de 50/50. Los químicos llaman a esto una mezcla racémica. Naturalmente, esperarías que ambos estuvieran igualmente presentes en nuestros cuerpos, ¿verdad? Mal! De hecho, todas las formas de vida solo usan L-aminoácidos y D-azúcares. La presencia de un solo isómero se denomina homoquiralidad. Desde las bacterias más pequeñas hasta los elefantes, solo los aminoácidos L componen las proteínas y solo los azúcares D componen los polisacáridos. En otras palabras, todas las proteínas son diestras y todos los polisacáridos son zurdos*. ¿Por qué es esto? Es un misterio que ha dejado perplejos a los biólogos durante años. A pesar de los mejores esfuerzos de físicos, químicos y biólogos evolutivos, todavía no lo sabemos con certeza. Aquí, echaremos un vistazo a algunas de las principales teorías actuales.
*(Debe tenerse en cuenta que algunos L-azúcares también se pueden descomponer por vías metabólicas. Los azúcares pueden formar anillos, y el azúcar-D forma un anillo más estable que el azúcar-L, pero los azúcares-L todavía pueden existir. La estabilidad del anillo puede ser el principal contribuyente a la prevalencia de azúcares D. A continuación, nos centraremos principalmente en los aminoácidos, que se adhieren estrictamente a una sola formación quiral en los sistemas biológicos.)
Enzimas y Evolución

Esto es lo que sabemos: las enzimas en las células solo pueden metabolizar un isómero, pero no el otro. Las enzimas catalizan las reacciones para descomponer y construir moléculas al unirse a ellas de maneras muy específicas. Una enzima que descompone la D-glucosa no será capaz de descomponer la L-glucosa. Si quisiéramos usar y construir ambos isómeros, tendríamos que tener dos conjuntos de enzimas. Esto requeriría más ADN, más comida y mucha más energía. Naturalmente, las células quieren ser lo más eficientes posible, por lo que tener un conjunto adicional de enzimas sería agotador.
Pero si tuviéramos esas enzimas adicionales, ¿no podríamos obtener el doble de energía del medio ambiente? Podríamos usar el otro 50% de isómeros si tuviéramos las enzimas para descomponer en lugar de perderlos. La respuesta tiene que ver con la evolución y la pirámide alimenticia.
Cuando la vida temprana estaba evolucionando, un organismo tendría enzimas que reaccionan selectivamente con un isómero. Los organismos que comieron esta primera forma de vida tendrían que tener las mismas enzimas selectivas para digerirlas. Si todos sus alimentos solo contienen azúcares D, ¡usted también lo hará! Por lo tanto, si la parte inferior de la cadena alimentaria solo utiliza L-aminoácidos, ¡la homoquiralidad se propagará a todos los organismos de la cadena alimentaria! Dado que la vida tuvo que desarrollar un conjunto de enzimas primero, terminamos atascados con esa selectividad. La presión selectiva de la evolución obligó a cada nuevo organismo a utilizar los mismos tipos de aminoácidos y azúcares que los anteriores.
Así que una vez que se elige un isómero, cada forma de vida lo usará. Pero, ¿por qué L-aminoácidos en lugar de D-aminoácidos, y por qué D-azúcares en lugar de L-azúcares? Este es el verdadero misterio. Algo al principio de la vida tenía que seleccionar uno sobre el otro. Es posible que en las primeras etapas de la vida, algunos organismos desarrollaron un conjunto de enzimas, mientras que diferentes organismos tenían el otro. Podría haber sido un evento aleatorio que eliminó una línea de enzimas, pero los científicos no están satisfechos con esta respuesta. Tiene que haber alguna razón por la que los L-aminoácidos y los D-azúcares son mejores para la supervivencia que sus contrapartes.
Enter Physics
Las mezclas racémicas son mezclas 50/50 de los dos isómeros. Pero hay razones para creer que en nuestro sistema estelar, en realidad hay una ligera preferencia de energía por un isómero sobre el otro. Para entender esta preferencia, tenemos que adentrarnos profundamente en la Vía Láctea.
Nuestra galaxia tiene un giro quiral y una orientación magnética. Esto hace que el polvo cósmico polarice circularmente la luz en una dirección. Básicamente, debido a que la luz es una onda de 2 dimensiones, se propagará en una hélice. El polvo cósmico hace que esta hélice gire preferentemente en una dirección.

Esta luz polarizada circularmente degrada los aminoácidos D más que los aminoácidos L, por lo que los aminoácidos L son más estables. Esto está respaldado por estudios de meteoros y cometas. La materia cósmica, al menos en la Vía Láctea, tiene una preferencia por los L-aminoácidos debido a la polarización circular de la luz.
Otra explicación física para la preferencia de un isómero sobre el otro tiene que ver con la fuerza electrodébil. Hay cuatro fuerzas fundamentales que gobiernan la física: la gravitación, el electromagnetismo, la fuerza nuclear fuerte y la fuerza electrodébil (también conocida como fuerza nuclear débil). Los tres primeros son aquirales: afectan a los isómeros L y D de la misma manera. La fuerza electrodébil, sin embargo, se ve afectada por la quiralidad. La fuerza electrodébil gobierna la desintegración radiactiva de átomos y moléculas. En esta decadencia, la paridad del universo no siempre se conserva. Durante la desintegración beta, los electrones emitidos favorecen un tipo de espín. El espín de los electrones degrada de nuevo los aminoácidos D más que los aminoácidos L, haciendo que el equilibrio de las moléculas cambie a favor del isómero L.
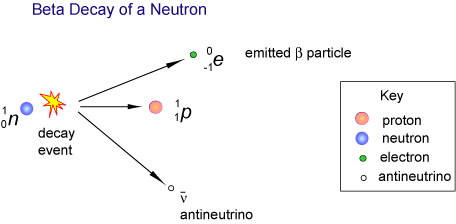
Tanto la luz polarizada y la electrodébil caries contribuir a una leve preferencia de un isómero sobre el otro en nuestra galaxia. Sin embargo, en el gran esquema de las cosas, esta discrepancia no es suficiente para explicar por qué CADA forma de vida utiliza solo azúcares D y aminoácidos L. Tiene que haber algo más. Lo que nos lleva a Autoc
Autocatálisis
Una vez que la física da una ligera ventaja a un isómero sobre el otro, hay una razón química que amplifica la diferencia. La autocatálisis significa que la presencia de un producto químico estimula su propia producción. Alrededor de 1950, F. C. Frank sugirió que los isómeros dominantes pueden activar su propia producción mientras suprimen la producción del otro isómero.

El gráfico de arriba ilustra el punto. Al comenzar con 3 isómeros L y 2 isómeros D, la relación se puede amplificar muy rápidamente, por lo que los isómeros L superan en número a los isómeros D. El isómero-L estimula su propia producción, y el isómero-L también se une al isómero-D en un proceso llamado «antagonismo mutuo».»Esto evita la formación de más isómeros D, y el isómero L se favorece rápidamente.
Esto fue solo un marco hipotético para explicar por qué solo tenemos L-aminoácidos y D-azúcares. Pero este concepto ganó apoyo cuando se descubrió la Reacción de Soai. Esta es una demostración de cómo ciertos isómeros pueden ser favorecidos sobre otros en los procesos biológicos. Aunque no hay evidencia de que la autocatulación ubicua cause homoquiralidad, ciertamente puede ser un factor de amplificación en algunos casos.
Un Modelo de trabajo
Hoy en día, la teoría más popular para la homoquiralidad biológica incluye todas estas conclusiones. Fenómenos físicos como la luz polarizada y la fuerza electrodébil crean un ligero desequilibrio de los isómeros D y L. Esta pequeña discrepancia se amplifica en un desequilibrio más desigual mediante autocatálisis. Luego, una vez que se formó la vida, un solo isómero fue seleccionado rápidamente por la cadena alimentaria y la especificidad de las enzimas. Por lo tanto, hoy solo vemos L-aminoácidos y D-azúcares.
Esta teoría todavía tiene algunos agujeros. Puede que nunca haya una explicación perfecta para un evento que comenzó hace miles de millones de años. Pero ahora tenemos al menos una solución potencial para el misterio de la homoquiralidad biológica.
» El misterio crea maravilla, y la maravilla es la base del deseo del hombre de comprender.»— Neil Armstrong