Química Introductoria-1ª Edición Canadiense
Objetivos de aprendizaje
- Definir búfer.
- Identifique correctamente los dos componentes de un búfer.
Como se indica en la Sección 12.4 «Ácidos y Bases Fuertes y Débiles y sus Sales», los ácidos débiles son relativamente comunes, incluso en los alimentos que comemos. Pero ocasionalmente encontramos un ácido o base fuerte, como el ácido estomacal, que tiene un pH fuertemente ácido de 1,7. Por definición, los ácidos y bases fuertes pueden producir una cantidad relativamente grande de iones H+ u OH− y, en consecuencia, tienen actividades químicas marcadas. Además, cantidades muy pequeñas de ácidos y bases fuertes pueden cambiar el pH de una solución muy rápidamente. Si se agregara 1 ml de ácido estomacal al torrente sanguíneo y no hubiera ningún mecanismo de corrección, el pH de la sangre disminuiría de aproximadamente 7,4 a aproximadamente 4,7, un pH que no es propicio para continuar viviendo. Afortunadamente, el cuerpo tiene un mecanismo para minimizar estos cambios dramáticos de pH.
El mecanismo implica un tampón, una solución que resiste cambios dramáticos en el pH. Los tampones lo hacen al estar compuestos de ciertos pares de solutos: un ácido débil más una sal derivada de ese ácido débil o una base débil más una sal de esa base débil. Por ejemplo, un tampón puede estar compuesto de HC2H3O2 disuelto (un ácido débil) y NaC2H3O2 (la sal derivada de ese ácido débil). Otro ejemplo de tampón es una solución que contiene NH3 (una base débil) y NH4Cl (una sal derivada de esa base débil).
Usemos un tampón HC2H3O2 / NaC2H3O2 para demostrar cómo funcionan los tampones. Si se agrega una base fuerte, una fuente de iones OH—(aq), a la solución tampón, esos iones OH− reaccionarán con el HC2H3O2 en una reacción ácido-base:
HC2H3O2(aq) + OH−(aq) → H2O(ℓ) + C2H3O2−(aq)
En lugar de cambiar el pH drásticamente haciendo que la solución sea básica, los iones OH− añadidos reaccionan para hacer H2O, por lo que el pH no cambia mucho.
Si se agrega un ácido fuerte, una fuente de iones H+, a la solución tampón, los iones H+ reaccionarán con el anión de la sal. Debido a que el HC2H3O2 es un ácido débil, no se ioniza mucho. Esto significa que si muchos iones H+ e iones C2H3O2 están presentes en la misma solución, se unirán para hacer HC2H3O2:
H+(aq) + C2H3O2−(aq) → HC2H3O2(aq)
En lugar de cambiar el pH drásticamente y hacer que la solución sea ácida, los iones H+ agregados reaccionan para hacer moléculas de un ácido débil. La Figura 12.2″ Las acciones de los Búferes » ilustra ambas acciones de un búfer.
Figura 12.2 Las acciones de los búferes
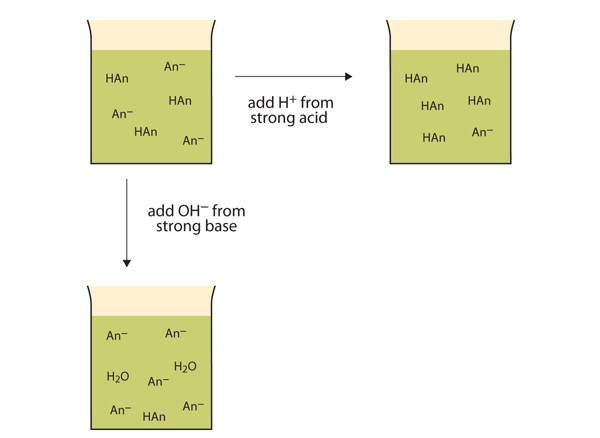
Los búferes pueden reaccionar con ácidos fuertes (superior) y bases fuertes (lateral) para minimizar grandes cambios en el pH.
Los tampones hechos de bases débiles y las sales de bases débiles actúan de manera similar. Por ejemplo, en un tampón que contiene NH3 y NH4Cl, las moléculas de NH3 pueden reaccionar con cualquier exceso de iones H+ introducidos por ácidos fuertes:
NH3(aq) + H+(aq) → NH4+(aq)
mientras que el ion NH4+(aq) puede reaccionar con cualquier ion OH− introducido por bases fuertes:
NH4+(aq) + OH−(aq) → NH3(aq) + H2O(ℓ)
Ejemplo 15
¿Qué combinaciones de compuestos pueden hacer una solución tampón?
- HCHO2 y NaCHO2
- HCl y NaCl
- CH3NH2 y CH3NH3Cl
- NH3 y NaOH
Solución
- HCHO2 es el ácido fórmico, ácido débil, mientras que NaCHO2 es la sal del anión del ácido débil (el formiato de iones ). La combinación de estos dos solutos formaría una solución tampón.
- El HCl es un ácido fuerte, no un ácido débil, por lo que la combinación de estos dos solutos no formaría una solución tampón.
- CH3NH2 es metilamina, que es como NH3 con uno de sus átomos H sustituido por un grupo CH3. Porque no figura en la Tabla 12.2 «Ácidos y bases fuertes», podemos suponer que es una base débil. El compuesto CH3NH3Cl es una sal hecha de esa base débil, por lo que la combinación de estos dos solutos formaría una solución tampón.
- NH3 es una base débil, pero NaOH es una base fuerte. La combinación de estos dos solutos no sería una solución tampón.
Pruébese a sí mismo
¿Qué combinaciones de compuestos pueden hacer una solución tampón?
- NaHCO3 y NaCl
- H3PO4 y NaH2PO4
- NH3 y (NH4)3PO4
- NaOH y NaCl
Respuestas
- no
- sí
- sí
- no
Búferes sólo cantidades limitadas de agregado de ácido fuerte o una base. Una vez que cualquiera de los dos solutos reacciona por completo, la solución ya no es un tampón, y pueden ocurrir cambios rápidos en el pH. Decimos que un búfer tiene una cierta capacidad. Los tampones que tienen más soluto disuelto en ellos, para empezar, tienen capacidades más grandes, como podría esperarse.
La sangre humana tiene un sistema de amortiguación para minimizar los cambios extremos en el pH. Un tampón en la sangre se basa en la presencia de HCO3 y H2CO3 . Con este tampón presente, incluso si un poco de ácido estomacal llegara directamente al torrente sanguíneo, el cambio en el pH de la sangre sería mínimo. Dentro de muchas de las células del cuerpo, hay un sistema de amortiguación basado en iones fosfato.
Aplicación de alimentos y bebidas: El ácido que alivia el Dolor
Aunque los medicamentos no son exactamente «alimentos y bebidas», los ingerimos, así que echemos un vistazo a un ácido que probablemente sea el medicamento más común: el ácido acetilsalicílico, también conocido como aspirina. La aspirina es bien conocida como analgésico y antipirético (reductor de fiebre).
La estructura de la aspirina se muestra en la figura adjunta. La parte ácida está rodeada; es el átomo H en esa parte que se puede donar como aspirina actúa como un ácido de Brønsted-Lowry. Debido a que no se indica en la Tabla 12.2 «Ácidos y bases fuertes», el ácido acetilsalicílico es un ácido débil. Sin embargo, sigue siendo un ácido, y dado que algunas personas consumen cantidades relativamente grandes de aspirina diariamente, su naturaleza ácida puede causar problemas en el revestimiento del estómago, a pesar de las defensas del estómago contra su propio ácido estomacal.
Figura 12.3 La estructura molecular de la Aspirina

Los átomos en círculo son la parte ácida de la molécula.
Debido a que las propiedades ácidas de la aspirina pueden ser problemáticas, muchas marcas de aspirina ofrecen una forma de «aspirina tamponada» del medicamento. En estos casos, la aspirina también contiene un agente tampón, generalmente MgO, que regula la acidez de la aspirina para minimizar sus efectos secundarios ácidos.
Tan útil y común como es la aspirina, se comercializó formalmente como medicamento a partir de 1899. La Administración de Alimentos y Medicamentos de los Estados Unidos (FDA, por sus siglas en inglés), la agencia gubernamental encargada de supervisar y aprobar medicamentos en los Estados Unidos, no se formó hasta 1906. Algunos han argumentado que si la FDA se hubiera formado antes de la introducción de la aspirina, es posible que la aspirina nunca haya obtenido la aprobación debido a su potencial de efectos secundarios: sangrado gastrointestinal, zumbido en los oídos, síndrome de Reye (un problema hepático) y algunas reacciones alérgicas. Sin embargo, recientemente se ha promocionado la aspirina por sus efectos en la reducción de ataques cardíacos y accidentes cerebrovasculares, por lo que es probable que la aspirina esté aquí para quedarse.
Conclusiones clave
- Un búfer es una solución que resiste cambios repentinos en el pH.
Ejercicios
-
Definir el búfer. ¿Qué dos componentes químicos relacionados se requieren para hacer un tampón?
-
¿un búfer se realiza mediante la combinación de un ácido fuerte con una base fuerte? Por qué o por qué no?
-
Qué combinaciones de compuestos puede hacer un tampón? Supongamos soluciones acuosas.
a) HCl y NaCl
b) HNO2 y NaNO2
c) NH4NO3 y HNO3
d) NH4NO3 y NH3
4. ¿Qué combinaciones de compuestos pueden hacer un tampón? Supongamos soluciones acuosas.
a) H3PO4 y Na3PO4
b) NaHCO3 y Na2CO3
c) NaNO3 y Ca(NO3)2
d) HN3 y NH3
5. Para cada combinación en el Ejercicio 3 que sea un tampón, escriba las ecuaciones químicas para las reacciones de los componentes del tampón cuando se agrega un ácido fuerte y una base fuerte.
6. Para cada combinación en el Ejercicio 4 que sea un tampón, escriba las ecuaciones químicas para las reacciones de los componentes del tampón cuando se agrega un ácido fuerte y una base fuerte.
7. El sistema tampón de fosfato completo se basa en cuatro sustancias: H3PO4, H2PO4 -, HPO42-y PO43 -. ¿Qué diferentes soluciones tampón se pueden hacer a partir de estas sustancias?
8. Explique por qué NaBr no puede ser un componente en un tampón ácido o básico.
9. Se elaboran dos soluciones que contienen las mismas concentraciones de solutos. Una solución está compuesta de H3PO4 y Na3PO4, mientras que la otra está compuesta de HCN y NaCN. ¿Qué solución debería tener la mayor capacidad como tampón?
10. Se elaboran dos soluciones que contienen las mismas concentraciones de solutos. Una solución está compuesta de NH3 y NH4NO3, mientras que la otra está compuesta de H2SO4 y Na2SO4. ¿Qué solución debería tener la mayor capacidad como tampón?
Respuestas
Un tampón es la combinación de un ácido o base débil y una sal de ese ácido o base débil.
a)
b) sí
c)
d) sí
3b: ácido fuerte: NO2− + H+ → HNO2; base fuerte: HNO2 + OH− → NO2− + H2O; 3d: base fuerte: NH4+ + OH− → NH3 + H2O; ácido fuerte: NH3 + H+ → NH4+7.
Los búferes se pueden hacer a partir de tres combinaciones: (1) H3PO4 y H2PO4 -, (2) H2PO4− y HPO42−, y (3) HPO42− y PO43−. (Técnicamente, un búfer se puede hacer a partir de dos componentes cualesquiera.)
El tampón de fosfato debe tener mayor capacidad.