Hva Er Radiobiologi-Strålingsbiologi-Definisjon
Strålingsbiologi (også kjent som radiobiologi) er en medisinsk vitenskap som involverer studier av biologiske effekter av ioniserende stråling på levende vev. Stråling er overalt rundt oss. I, rundt og over den verden vi lever i. Det er en naturlig energikraft som omgir oss. Det er en del av vår naturlige verden som har vært her siden vår planet ble født. Enten strålekilden er naturlig eller menneskeskapt, enten det er en stor dose stråling eller en liten dose, vil det være noen biologiske effekter. Generelt er ioniserende stråling skadelig og potensielt dødelig for levende vesener, men kan ha helsemessige fordeler i medisin, for eksempel i strålebehandling for behandling av kreft og tyrotoksikose. Dette kapitlet oppsummerer kort de kortsiktige og langsiktige konsekvensene som kan oppstå ved eksponering for stråling.
Cellulær Skade-Radiobiologi
alle biologiske skadeeffekter begynner med konsekvensen av strålingsinteraksjoner med atomene som danner cellene. Alle levende ting består av en eller flere celler. Hver del av kroppen din består av celler eller ble bygget av dem. Selv om vi har en tendens til å tenke på biologiske effekter når det gjelder effekten av stråling på levende celler, interagerer ioniserende stråling per definisjon bare med atomer ved en prosess som kalles ionisering. For ioniserende stråling, den kinetiske energien til partikler(fotoner, elektroner, etc.) av ioniserende stråling er tilstrekkelig og partikkelen kan ionisere (for å danne ion ved å miste elektroner) målatomer for å danne ioner. Bare ioniserende stråling kan slå elektroner fra et atom.
det er to mekanismer hvor stråling til slutt påvirker celler. Disse to mekanismene kalles Vanligvis:
- Direkte effekter. Direkte effekter er forårsaket av stråling, når stråling samhandler direkte med atomene I DNA-molekylet, eller en annen cellulær komponent som er kritisk for cellens overlevelse. Sannsynligheten for at strålingen interagerer MED DNA-molekylet er svært liten siden disse kritiske komponentene utgjør en så liten del av cellen.
- Indirekte effekter. Indirekte effekter skyldes interaksjon av stråling vanligvis med vannmolekyler. Hver celle, akkurat som det er tilfelle for menneskekroppen, er for det meste vann. Ioniserende stråling kan bryte bindingene som holder vannmolekylet sammen, og produsere radikaler som hydroksyl OH, superoksidanion O2-og andre– Disse radikaler kan bidra til ødeleggelsen av cellen.
et stort antall celler av en bestemt type kalles et vev. Hvis dette vevet danner en spesialisert funksjonell enhet, kalles det et organ. Type og antall berørte celler er også en viktig faktor. Noen celler og organer i kroppen er mer følsomme for ioniserende stråling enn andre.Følsomhet av ulike typer celler til ioniserende stråling er svært høy for vev som består av celler som deler seg raskt som de som finnes i beinmarg, mage, tarm, mannlige og kvinnelige reproduktive organer, og utvikler foster. Dette skyldes at delende celler krever riktig DNA-informasjon for at cellens avkom skal overleve. En direkte interaksjon av stråling med en aktiv celle kan resultere i død eller mutasjon av cellen, mens en direkte interaksjon med DNA i en sovende celle ville ha mindre effekt.som et resultat kan levende celler klassifiseres i henhold til deres reproduksjonshastighet, noe som også indikerer deres relative følsomhet overfor stråling. Som et resultat er aktivt reproduserende celler mer følsomme for ioniserende stråling enn celler som utgjør hud -, nyre – eller levervev. Nerve – og muskelceller er de tregeste å regenerere og er de minst følsomme cellene.
 følsomheten til de ulike organene i menneskekroppen korrelerer med den relative følsomheten til cellene de er sammensatt av. I praksis representeres denne følsomheten av vevsvektingsfaktoren, wT, som er den faktoren hvorved ekvivalentdosen i et vev Eller organ T veies for å representere det relative bidraget fra det vevet eller organet til den totale helseskader som følge av ensartet bestråling av kroppen (ICRP 1991B).
følsomheten til de ulike organene i menneskekroppen korrelerer med den relative følsomheten til cellene de er sammensatt av. I praksis representeres denne følsomheten av vevsvektingsfaktoren, wT, som er den faktoren hvorved ekvivalentdosen i et vev Eller organ T veies for å representere det relative bidraget fra det vevet eller organet til den totale helseskader som følge av ensartet bestråling av kroppen (ICRP 1991B).
hvis en person bestråles bare delvis, vil dosen avhenge sterkt av vevet som ble bestrålet. For eksempel er en 10 mSv gammadose til hele kroppen og en 50 mSv dose til skjoldbruskkjertelen den samme, når det gjelder risiko, som en helkroppsdose på 10 + 0,04 x 50 = 12 mSv.
Høy-LA Og Lav-La Stråling
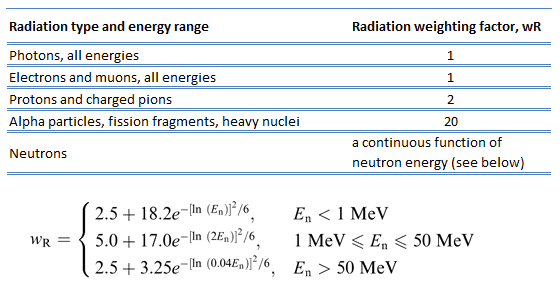
som skrevet, interagerer hver type stråling med materie på en annen måte. For eksempel ladede partikler med høye energier kan direkte ionisere atomer. Alfa partikler er ganske massiv og bære en dobbel positiv ladning, slik at de har en tendens til å reise bare en kort avstand og ikke trenge veldig langt inn i vev hvis i det hele tatt. Men alfa partikler vil deponere sin energi over et mindre volum (muligens bare noen få celler hvis de kommer inn i en kropp) og forårsake mer skade på de få cellene.
Beta partikler (elektroner) er mye mindre enn alfa partikler. De bærer en enkelt negativ ladning. De er mer gjennomtrengende enn alfa partikler. De kan reise flere meter, men legger mindre energi på et hvilket som helst punkt langs deres veier enn alfa partikler. Dette betyr at betapartikler har en tendens til å skade flere celler, men med mindre skade på hver. På den annen side samhandler elektrisk nøytrale partikler bare indirekte, men kan også overføre noen eller alle deres energier til saken.
det ville sikkert forenkle saker om biologiske effekter av stråling var direkte proporsjonal med absorbert dose. Dessverre er biologiske effekter også avhengig av hvordan den absorberte dosen fordeles langs strålingsbanen. Studier har vist at alfa-og nøytronstråling forårsaker større biologisk skade for en gitt energiavsetning per kg vev enn gammastråling gjør. Det ble oppdaget, biologiske effekter av noen stråling øker med lineær energioverføring (LET). Kort sagt, den biologiske skaden fra HØY LET stråling (alfa partikler, protoner eller nøytroner) er mye større enn den fra lav LET stråling (gammastråler). Dette skyldes at levende vev lettere kan reparere skader fra stråling som er spredt over et stort område enn det som er konsentrert i et lite område. Selvfølgelig, ved svært høye eksponeringsnivåer kan gammastråler fortsatt forårsake stor skade på vev.Fordi mer biologisk skade er forårsaket for den samme fysiske dosen (dvs.den samme energien avsatt per enhetsmasse av vev), er en grå av alfa-eller nøytronstråling mer skadelig enn en grå av gammastråling. Dette faktum at stråling av forskjellige typer (og energier) gir forskjellige biologiske effekter for den samme absorberte dosen, er beskrevet i forhold til faktorer kjent som relativ biologisk effektivitet (rbe) og strålingsvektingsfaktoren (wR).
Akutt Dose og Kronisk Dose
Biologiske effekter av stråling og deres konsekvenser avhenger sterkt av nivået av doseraten oppnådd. I radiobiologi er doseraten et mål for strålingsdoseintensitet (eller styrke). Lave doser er vanlig i hverdagen. I de følgende punktene er det noen eksempler på strålingseksponering, som kan hentes fra forskjellige kilder.
- 05 µSv – Sover ved siden av noen
- 09 µSv – som Bor innenfor 30 kilometer i et kjernekraftverk for et år
- 1 µSv – å Spise en banan
- 3 µSv – Bor innenfor 50 miles av et kullkraftverk for et år
- 10 µSv – Gjennomsnittlig daglig dose mottatt fra naturlig bakgrunn
- 20 µSv – Brystet X-ray
Fra biologiske konsekvensene synspunkt, det er veldig viktig å skille mellom doser mottatt over korte og lengre perioder. Derfor er biologiske effekter av stråling vanligvis delt inn i to kategorier.
- Akutte Doser. En «akutt dose» (kortsiktig høydose) er en som oppstår over en kort og begrenset tidsperiode, dvs. innen en dag.
- Kroniske Doser. En «kronisk dose» (langsiktig lavdose) er en dose som fortsetter i lengre tid, dvs. uker og måneder, slik at den bedre beskrives med en doserate.Høye doser har en tendens til å drepe celler, mens lave doser har en tendens til å skade eller endre dem. Høye doser kan forårsake visuelt dramatiske strålingsforbrenninger, og / eller rask dødsfall gjennom akutt strålingssyndrom. Akutte doser under 250 mGy er usannsynlig å ha noen observerbare effekter. 3 til 5 Gy har en 50% sjanse for å drepe en person noen uker etter eksponeringen, hvis en person ikke får medisinsk behandling.
Lave doser spredt over lange perioder, forårsaker ikke et øyeblikkelig problem for noen kroppsorganer. Effektene av lave doser av stråling forekommer på nivået av cellen, og resultatene kan ikke observeres i mange år. Videre viser noen studier at de fleste humane vev utviser en mer uttalt toleranse for effekten av lav-LET-stråling ved langvarig eksponering sammenlignet med en engangseksponering for en lignende dose.
Deterministiske Og Stokastiske Effekter
i radiobiologi er de fleste negative helseeffekter av strålingseksponering vanligvis delt inn i to brede klasser:
- deterministiske effekter er terskelhelseeffekter, som er relatert direkte til den absorberte strålingsdosen og alvorlighetsgraden av effekten øker etter hvert som dosen øker.
- Stokastiske effekter oppstår ved en tilfeldighet, vanligvis uten et terskelnivå av dose. Sannsynligheten for stokastiske effekter er proporsjonal med dosen, men alvorlighetsgraden av effekten er uavhengig av mottatt dose.
Deterministiske Effekter
i radiobiologi er deterministiske effekter (eller ikke-stokastiske helseeffekter) helseeffekter som er relatert direkte til den absorberte stråledosen og alvorlighetsgraden av effekten øker etter hvert som dosen øker. Deterministiske effekter har en terskel under hvilke ingen påviselige kliniske effekter oppstår. Terskelen kan være svært lav (av størrelsesorden 0,1 Gy eller høyere) og kan variere fra person til person. For doser mellom 0,25 Gy og 0,5 Gy kan små blodforandringer påvises ved medisinske vurderinger, og for doser mellom 0,5 Gy og 1,5 Gy vil blodforandringer bli notert og symptomer på kvalme, tretthet, oppkast oppstår.
når terskelen er overskredet, øker alvorlighetsgraden av en effekt med dosen. Årsaken til tilstedeværelsen av denne terskeldosen er at strålingsskader (alvorlig funksjonsfeil eller død) av en kritisk populasjon av celler (høye doser har en tendens til å drepe celler) i et gitt vev må opprettholdes før skade uttrykkes i en klinisk relevant form. Derfor kalles deterministiske effekter også vevsreaksjon. De kalles også ikke-stokastiske effekter for å kontrastere med tilfeldighetslignende stokastiske effekter (f.eks. kreftinduksjon).Deterministiske effekter er ikke nødvendigvis mer eller mindre alvorlige enn stokastiske effekter. Høye doser kan forårsake visuelt dramatiske strålingsforbrenninger, og / eller rask dødsfall gjennom akutt strålingssyndrom. Akutte doser under 250 mGy er usannsynlig å ha noen observerbare effekter. 3 til 5 Gy har en 50% sjanse for å drepe en person noen uker etter eksponeringen, hvis en person ikke får medisinsk behandling. Deterministiske effekter kan til slutt føre til en midlertidig plage eller også til dødsfall. Eksempler på deterministiske effekter:
Eksempler på deterministiske effekter er:
- Akutt strålingssyndrom, ved akutt helkroppsstråling
- strålingsforbrenninger, fra stråling til en bestemt kroppsoverflate
- Strålingsindusert tyreoiditt, en potensiell bivirkning av strålebehandling mot hypertyreose
- Kronisk strålingssyndrom, fra langvarig stråling.
- Strålingsindusert lungeskade, fra for eksempel strålebehandling til lungene
Dødelige Stråledoser
den dødelige stråledosen (LD) er en indikasjon på den dødelige mengden stråling. I strålingsbeskyttelse brukes MEDIAN dødelig dose, LDXY vanligvis. For eksempel er dosen av stråling som forventes å forårsake død til 50 % av de bestrålede personene innen 30 dager LD50 / 30. LD1 er den dosen som forventes å forårsake død hos 1% av de bestrålede personene, OG DERFOR ER LD99 dødelig for alle (99%) bestrålede personer. Det er også svært viktig, om en person får noen medisinsk behandling eller ikke. Jo større en akutt strålingsdose er, desto større er muligheten for at den dreper individet. FOR en sunn voksen anslås LD50 å være et sted mellom 3 og 5 Gy.
- 2,5 Sv-Dose som dreper et menneske med 1% risiko (LD1), hvis dosen mottas over en svært kort varighet.
- 5 Sv – Dose som dreper et menneske med 50% risiko innen 30 dager (LD50 / 30), hvis dosen mottas over en svært kort varighet. Dødsårsak vil være tap av benmargsfunksjon.
- 8 Sv-Dose som dreper et menneske med 99% risiko (LD99), hvis dosen mottas over en svært kort varighet. Ved rundt 10 Gy kan akutt betennelse i lungene oppstå og føre til døden.
de dødelige dosedataene ovenfor gjelder for akutte gammadoser levert på svært kort tid, f.eks. noen få minutter. Mer dose er nødvendig for å gi effektene nevnt ovenfor, hvis dosen mottas over en periode på timer eller lenger.
Stokastiske Effekter
i radiobiologi oppstår stokastiske effekter av ioniserende stråling ved en tilfeldighet, vanligvis uten et terskelnivå for dose. Sannsynligheten for stokastiske effekter er proporsjonal med dosen, men alvorlighetsgraden av effekten er uavhengig av mottatt dose. De biologiske effektene av stråling på mennesker kan grupperes i somatiske og arvelige effekter. Somatiske effekter er de som lider av den eksponerte personen. Arvelige effekter er de som lider av avkom av den enkelte utsatt. Kreftrisiko er vanligvis nevnt som den viktigste stokastiske effekten av ioniserende stråling, men også arvelige lidelser er stokastiske effekter.
IFØLGE ICRP:
(83) På grunnlag av disse beregningene foreslår Kommisjonen nominelle sannsynlighetskoeffisienter for skadejustert kreftrisiko som 5,5 x 10-2 Sv-1 for hele populasjonen og 4.1 x 10-2 Sv-1 for voksne arbeidere. For arvelige effekter er den negative justerte nominelle risikoen i hele populasjonen estimert til 0,2 x 10-2 Sv-1 og hos voksne arbeidstakere til 0,1 x 10-2 Sv-1 .
Spesiell Referanse: ICRP, 2007. Anbefalinger Fra Den Internasjonale Kommisjonen For Radiologisk Beskyttelse fra 2007. ICRP Publikasjon 103. Anne. ICRP 37 (2-4).si-enheten for effektiv dose, sievert, representerer den ekvivalente biologiske effekten av innskudd av en joule av gammastråler energi i et kilo humant vev. Som et resultat representerer en sievert en 5.5% sjanse for å utvikle kreft. Merk at den effektive dosen ikke er ment som et mål for deterministiske helseeffekter, som er alvorlighetsgraden av akutt vevskader som er sikker på å skje, som måles av mengden absorbert dose.Det er tre generelle kategorier av stokastiske effekter som følge av eksponering for lave doser av stråling. Disse Er:
- Genetiske effekter. Den genetiske effekten lider av avkom av den enkelte utsatt. Det innebærer mutasjon av svært spesifikke celler, nemlig sædceller eller eggceller. Stråling er et eksempel på et fysisk mutagent middel. Merk at det også er mange kjemiske midler, så vel som biologiske midler (for eksempel virus) som forårsaker mutasjoner. Et svært viktig faktum å huske er at stråling øker den spontane mutasjonsraten, men produserer ingen nye mutasjoner.
- somatiske effekter. Somatiske effekter er de som lider av den eksponerte personen. Den vanligste effekten av bestråling er stokastisk induksjon av kreft med latent periode på år eller tiår etter eksponering. Siden kreft er det primære resultatet, kalles det noen ganger kreftfremkallende effekten. Stråling er et eksempel på fysisk kreftfremkallende, mens sigaretter er et eksempel på et kjemisk kreftfremkallende middel. Virus er eksempler på biologiske kreftfremkallende stoffer.
- In-Utero effekter involverer produksjon av misdannelser i utvikling av embryoer. Dette er imidlertid faktisk et spesielt tilfelle av den somatiske effekten, siden embryoet / fosteret er det som er utsatt for strålingen.
Somatiske effekter som følge av eksponering for stråling antas av de fleste å forekomme på en stokastisk måte. Den mest aksepterte modellen antyder at forekomsten av kreft på grunn av ioniserende stråling øker lineært med effektiv strålingsdose med en hastighet på 5,5% per sievert. Denne modellen er kjent som linear no-threshold model (LNT). Denne modellen antar at det ikke er noe terskelpunkt og risikoen øker lineært med en dose. Hvis denne lineære modellen er riktig, er naturlig bakgrunnsstråling den farligste strålekilden til generell folkehelse, etterfulgt av medisinsk bildebehandling som et nært sekund. LNT er ikke universelt akseptert med noen foreslår en adaptiv dose-respons forhold der lave doser er beskyttende og høye doser er skadelig. Det må understrekes at en rekke organisasjoner er uenige i å bruke den lineære no-threshold-modellen for å estimere risiko fra miljø-og yrkesmessig lavstrålingseksponering.
Radiobiologi og Dosegrenser
i strålevern er dosegrensene satt til å begrense stokastiske effekter til et akseptabelt nivå, og for å forhindre deterministiske effekter helt. Merk at stokastiske effekter er de som oppstår fra sjanse: jo større dose, desto mer sannsynlig er effekten. Deterministiske effekter er de som normalt har en terskel: over dette øker alvorlighetsgraden av effekten med dosen. Dosegrenser er en grunnleggende komponent i strålevern, og brudd på disse grensene er mot strålingsregulering i de fleste land. Vær oppmerksom på at dosegrensene beskrevet i denne artikkelen gjelder for rutinemessige operasjoner. De gjelder ikke for en nødsituasjon når menneskelivet er truet. De gjelder ikke i nødeksponeringssituasjoner der en person forsøker å forhindre en katastrofal situasjon.
grensene er delt inn i to grupper, publikum og yrkeseksponerte arbeidstakere. I HENHOLD TIL ICRP refererer yrkeseksponering til all eksponering som arbeidstakere pådrar seg i løpet av sitt arbeid, med unntak av ekskluderte eksponeringer og eksponeringer fra fritatte aktiviteter som involverer stråling eller fritatte kilder
- enhver medisinsk eksponering
- den normale lokale naturlige bakgrunnsstrålingen.
tabellen nedenfor oppsummerer dosegrenser for yrkeseksponerte arbeidstakere og for publikum:
Kilde til data: ICRP, 2007. Anbefalinger Fra Den Internasjonale Kommisjonen For Radiologisk Beskyttelse fra 2007. ICRP Publikasjon 103. Anne. ICRP 37 (2-4).
i henhold TIL anbefaling AV ICRP i sin uttalelse om vevsreaksjoner av 21. April 2011 ble den tilsvarende dosegrensen for linsen i øyet for yrkeseksponering i planlagte eksponeringssituasjoner redusert fra 150 mSv / år til 20 mSv/år, i gjennomsnitt over definerte perioder på 5 år, uten årlig dose i et enkelt år over 50 mSv.
Grenser for effektiv dose er for summen av relevante effektive doser fra ekstern eksponering i den angitte tidsperioden og den forpliktede effektive dosen fra inntak av radionuklider i samme periode. For voksne beregnes den engasjerte effektive dosen for en periode på 50 år etter inntak, mens for barn beregnes den for perioden opp til 70 år. Den effektive helkroppsdosegrensen på 20 mSv er en gjennomsnittsverdi over fem år. Den virkelige grensen er 100 mSv i 5 år, med ikke mer enn 50 mSv i ett år.