Algorytmy leczenia wrzodziejącego zapalenia jelita grubego z lokalnego doświadczenia / klinicznego czasopisma medycznego Las Condes
wprowadzenie
wrzodziejące zapalenie jelita grubego (UC) jest częścią choroby zapalnej jelit (IBD) i charakteryzuje się przewlekłym zapaleniem o nieznanej etiologii, prawdopodobnie wynikającym z interakcji czynników środowiskowych i genetycznych1. Lokalizuje się wyłącznie w okrężnicy, trwale angażując wyściółkę odbytnicy i różne rozszerzenia okrężnicy. Jest to przewlekła choroba, która rozwija się wraz z wybuchami (kryzysami) i okresami remisji. Kryzysy charakteryzują się występowaniem rektorargii, wzrostem częstotliwości i zmniejszeniem konsystencji wypróżnień. Może również objawiać się zaburzeniami ogólnymi, pilnością i nietrzymaniem stolca, bólem brzucha, utratą masy ciała (w ciężkich przypadkach) i objawami pozakomórkowymi (między innymi stawowymi, okulistycznymi, dermatologicznymi, wątrobowo-żółciowymi i naczyniowymi).
tradycyjnie leczenie UC koncentrowało się na osiągnięciu remisji objawów, jednak obecnie wykazano, że cel ten nie jest wystarczający do zmniejszenia częstości hospitalizacji i kolektomii,chyba że towarzyszy mu gojenie śluzu2, 3. Ponadto w niedawno opublikowanym badaniu stwierdzono, że zgodność aktywności endoskopowej z aktywnością histologiczną sięga tylko 60% i że normalizacja histologiczna jest związana z mniejszą częstością ognisk4. Biorąc to pod uwagę, należy zauważyć, że cel leczenia UC powinien koncentrować się na remisji endoskopowej, a najlepiej histologicznej. Takie podejście wymaga starannego i systematycznego śledzenia klinicznych, endoskopowych i biologicznych markerów pacjentów.
w celu ujednolicenia leczenia pacjentów leczonych, w ramach interdyscyplinarnego programu dla pacjentów z IBD opracowano algorytmy leczenia z uwzględnieniem celów terapeutycznych, różnych alternatyw i proponowanych terminów oceny odpowiedzi na różne strategie. Każdy z nich powinien zostać omówiony wraz z pacjentem, wyjaśniając ich ryzyko i korzyści oraz dostosowując Plan obserwacji, który ułatwia przestrzeganie zaleceń i wczesne zajęcie się brakiem odpowiedzi na leczenie lub jego powikłaniami.
przy wstępnej ocenie, a także w przebiegu choroby, należy wziąć pod uwagę udział interdyscyplinarnego zespołu obejmującego gastroenterologów, koloproktologów, pielęgniarek, radiologów, anatomopatologów i innych specjalności, takich jak psychologowie, dietetycy i dietetycy, kinezjolodzy, reumatolodzy, dermatolodzy, zakaźnicy, Położnicy i inni. Pozwala to pacjentowi kompleksowo zarządzać swoją patologią.
w poniższych algorytmach należy wziąć pod uwagę następujące punkty:
-
prawidłowe potwierdzenie diagnostyczne. Ustal przy diagnozie stopień i nasilenie choroby. Obejmuje to wykonanie kolonoskopii z biopsją i wykluczenie diagnoz różnicowych, takich jak zakaźne lub niedokrwienne zapalenie jelita grubego. W naszym zespole wykorzystujemy kliniczny indeks majowy do diagnozy i w każdej z konsultacji kontrolnych5.
-
zidentyfikuj złe czynniki prognostyczne, takie jak: Hipoalbuminemia, podwyższone białko C-reaktywne (CRP), niedokrwistość, nasilenie endoskopowe (obecność głębokich wrzodów), skumulowana nadinfekcja, wczesny wiek manifestacji (6, umożliwiając personalizację strategii terapeutycznych poprzez zmniejszenie powikłań choroby.
-
po rozpoczęciu strategii leczenia. Rozważ czas oceny skuteczności leczenia i dokonaj korekt lub zmian w leczeniu, jeśli cele terapeutyczne nie zostały osiągnięte (ryc.1). Odpowiednie monitorowanie UC obejmuje określenie aktywności choroby za pomocą kalprotektyny kałowej (CF), badań endoskopowych, biopsji i/lub obrazowania w zależności od pierwotnie ustalonej lokalizacji i stanu ciężkości.
 Rysunek 1.
Rysunek 1.ocena leczenia według celów w zapalnej chorobie jelit
(*) aktywność zapalną należy zobiektywizować za pomocą kalprotektyny kałowej, kolonoskopii ileoskopii, biopsji, a ostatecznie badania obrazowego (najlepiej MRI) i / lub kapsułki endoskopowej.
MRI: MRI.
(0,24 MB).algorytm leczenia zapalenie odbytnicy wrzodziejące (ryc. 2)
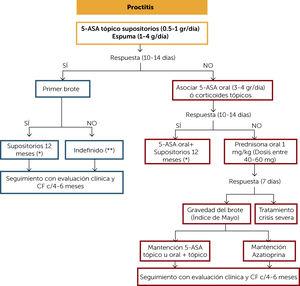
u pacjentów z wrzodziejące zapalenie odbytnicy zaleca się jako pierwszy wybór stosowania 5-aminosalicilatos (5-ASA), miejscowo. Jeśli pacjent reaguje klinicznie (10-14 dni) i jest to debiut choroby, zaleca się utrzymanie leczenia czopkami przez co najmniej 12 miesięcy. Po 8 tygodniach leczenia dawkę można zmniejszyć w zależności od odpowiedzi na noc średnio lub 3 razy w tygodniu. Jeśli pacjent miał więcej niż jeden wybuch, zaleca się utrzymywanie terapii miejscowej w nieskończoność. Monitorowanie powinno być kliniczne, a pomiar CF co 4 miesiące.
 rys. 2.
rys. 2.algorytm leczenia wrzodziejącego zapalenia odbytnicy
(*) dawki początkowej po 8 tygodniach, może być zmniejszona w zależności od odpowiedzi klinicznej i CF (mcg / G) w nocy, 3 razy w tygodniu. Rozważ przerwanie leczenia, jeśli po pierwszym roku leczenia wystąpi kliniczna, CF, kolonoskopia i odpowiedź histologiczna. Jeśli terapia zawiesza się, jeśli odpowiedź kliniczna, CF, kolonoskopia i histologiczna. Jeśli przestaniesz, będziesz potrzebować monitorowania klinicznego i CF co 4 miesiące przez co najmniej rok. Następnie co najmniej 2 razy w roku.
(**) należy rozważyć przerwanie leczenia, jeśli występuje odpowiedź kliniczna, CF, kolonoskopowa i histologiczna. Jeśli przestaniesz, będziesz potrzebować monitorowania klinicznego i CF co 4 miesiące przez co najmniej rok. Następnie co najmniej 2 razy w roku.
5-ASA: 5-amonisalicylany; CF: kalprotektyna kałowa.
(0,55 MB).jeśli pacjent nie reaguje na początkowe leczenie, doustne lub miejscowe 5-ASA kortykoidowe mogą być powiązane i klinicznie ponownie ocenione po 10-14 dniach. Jeśli pojawi się odpowiedź, utrzymuj powiązaną terapię przez co najmniej 12 miesięcy. Jeśli nie ma odpowiedzi, zaleca się rozpoczęcie doustnych kortykoidów w dawkach 1 mg / kg i ocenę kliniczną na tydzień. Jeśli wystąpi odpowiedź, a wybuch był łagodny do umiarkowanego, można go utrzymać miejscowo 5-ASA lub pokrewną terapią i stopniowo usuwać kortykoidy. Proponowany schemat wypłat przedstawiono w tabeli 1. Jeśli ognisko było umiarkowane lub ciężkie, sugeruje się utrzymanie leczenia tiopurynami (TP) (azatiopryna lub 6-merkaptopuryna). Obserwację kliniczną i pomiar CF należy wykonywać co 4 miesiące. Jeśli pacjent nie reaguje na indukcję kortykoidami, należy go uznać za ciężki kryzys („algorytm leczenia ciężkiego kryzysu”).
Tabela 1.Schemat leczenia CU z cortioides
Dawki prednizonu dziennie Schemat redukcji dawki 60 mg dziennie 1° tygodniu 50 mg dziennie 2° tygodniu 40mg dziennie 3° tygodniu 35mg w dzień 4 tygodnie 30 mg dziennie 5° tydzień 25 mg na dobę 6° tydzień 20 mg na dobę 7° tydzień 17.5 mg na dobę 8° tydzień 15 mg na dobę, 9.tydzień 12.5 mg na dobę 10° tydzień 10 mg na dobę 11. tydzień 7.5 mg na dobę 12° tydzień 5 mg dziennie 13. tydzień 2.5mg dziennie 14° tydzień algorytm leczenia zapalenia jelita grubego po lewej stronie (rys. 3)
u pacjentów z zapaleniem jelita grubego zaleca się leczenie 5-ASA lub doustnie związane z miejscowym leczeniem, szczególnie u pacjentów z obecnością objawów odbytnicy. Jeśli wystąpi odpowiedź kliniczna w ciągu 1-2 tygodni, zaleca się przestrzeganie tej samej terapii indukcyjnej i obserwacji klinicznej oraz z CF co 4 miesiące. Jeśli nie zareaguje, należy rozpocząć leczenie doustnymi kortykoidami 1mg / kg lub budezonidem MMX i ocenić odpowiedź kliniczną po 7 dniach. Ten ostatni lek może być alternatywą w niepoważnych ujęciach, z tą zaletą, że ma mniej skutków ubocznych niż prednizon. Jeśli wystąpi odpowiedź i odpowiada pierwszemu wybuchowi, wskazane jest postępujące usuwanie kortykoidów (Tabela 1) i leczenie podtrzymujące doustną terapią 5-ASA lub skojarzoną. Jeśli nie pasuje do pierwszego błysku, prezentowane są dwa scenariusze: w przypadku, gdy wybuch, poprzedni był krótszy niż 12 miesięcy temu, należy rozważyć leczenie podtrzymujące TP. Jeśli poprzedni wybuch miał miejsce ponad 12 miesięcy temu, można go podnieść jako leczenie podtrzymujące 5-ASA.
 Rysunek 3.
Rysunek 3.algorytm leczenia lewego zapalenia jelita grubego
(*) monitorowanie kliniczne i CF co 4 miesiące przez co najmniej jeden rok. Następnie co najmniej 2 razy w roku.
( * *) można rozważyć zastosowanie budezonidu MMX, który może być alternatywą w niepoważnych obrazach, z tą zaletą, że ma mniej skutków ubocznych niż prednizon.
( * * *) w przypadku, gdy poprzedni wybuch był krótszy niż 12 miesięcy temu, przy odpowiedniej terapii 5-ASA, bez rezygnacji z leczenia lub infekcji, należy rozważyć zastosowanie TP (lub w przypadku wedolizumabu). Jeśli poprzedni wybuch miał miejsce ponad 12 miesięcy temu, można go podnieść jako leczenie podtrzymujące 5-ASA.
(****) należy monitorować za pomocą badań krwi i testów wątrobowych co 3 miesiące.
(*****) pacjent wymagający hospitalizacji i endowenozowych kortykoidów rozważ w swoim utrzymaniu stosowanie TP jako monoterapii, stosowanie anty-TNF lub połączenie obu. Bądź dostępny vedolizumad. Ocena ryzyka / korzyści / kosztów i dostępu do terapii.
5-ASA: 5-amonisalicylany; CF: kalprotektyna kałowa; TP: tiopuryny.
(0,5 MB).jeśli pacjent nie reaguje na indukcję kortykosteroidów należy uznać za kryzys ciężki („algorytm przetwarzania kryzysu”).
algorytm leczenia niepoważnego rozległego zapalenia jelita grubego (1) (ryc.4)
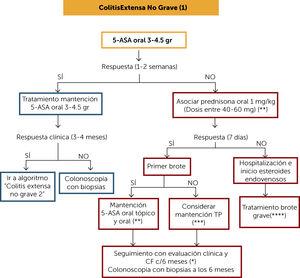
leczenie indukcyjne remisji niepoważnego rozległego zapalenia jelita grubego można rozpocząć od doustnego 5-ASA w dawkach 3-4, 5 g / dzień i ocenić odpowiedź kliniczną po 7-14 dniach. Jeśli odpowiedź jest korzystna, pozostaw leczenie podtrzymujące w równej dawce i oceń odpowiedź kliniczną po 3-4 miesiącach z klinicznym wskaźnikiem Mayo i CP. jeśli wystąpiła odpowiedź kliniczna, kontynuuj leczenie w oparciu o „niepoważny algorytm leczenia rozległego zapalenia jelita grubego 2”. Jeśli po 4 miesiącach nie ma korzystnej odpowiedzi klinicznej z doustnym 5-ASA w odpowiednich dawkach, należy wykonać kolonoskopię z biopsją w celu oceny nasilenia aktywności zapalnej.
 Rysunek 4.
Rysunek 4.algorytm leczenia rozległego, niepoważnego zapalenia jelita grubego (1)
( * ) można rozważyć zastosowanie budezonidu MMX, który może być alternatywą w niepoważnych obrazach, z korzyścią dla mniejszej liczby działań niepożądanych niż prednizon.
(**) kliniczne i CF monitorie co 4 miesiące przez co najmniej jeden rok. Następnie co najmniej 2 razy w roku.
( * * * ) w przypadku, gdy poprzednia epidemia była mniejsza niż 12 miesięcy temu, przy odpowiedniej terapii 5-ASA, bez rezygnacji z leczenia lub infekcji, należy rozważyć zastosowanie TP (lub jeśli wedolizumab jest dostępny). Jeśli poprzednia epidemia miała miejsce ponad 12 miesięcy temu, można ją uznać za leczenie podtrzymujące 5-ASA.
(****) pacjent wymagający hospitalizacji i endowenozowych kortykoidów rozważa w swoim utrzymaniu stosowanie TP jako monoterapii, stosowanie anty-TNF lub ich połączenie. być dostępnym wedolizumabem. Ocena ryzyka / korzyści / kosztów i dostępu do terapii.
5-ASA: 5-amonisalicylany; CF: kalprotektyna kałowa; TP: tiopuryny.
(0,52 MB).Jeśli pacjent nie reaguje na leczenie indukcyjne doustnie 5-ASA, należy podać kortykosteroidy doustnie (1mg / kg) i ocenę odpowiedzi klinicznej po 7 dniach. Budezonid MMX, jak wspomniano, może być alternatywą w łagodnych przypadkach, ponieważ ma mniej skutków ubocznych. Jeśli nie ma odpowiedzi, zaleca się stosowanie ogólnoustrojowych kortykoidów. Jeśli wystąpi odpowiedź i odpowiada pierwszemu wybuchowi, wskazane jest postępujące usuwanie kortykoidów (Tabela 1) i leczenie podtrzymujące doustną terapią 5-ASA lub skojarzoną. Jeśli nie jest to zgodne z pierwszą epidemią, przedstawiono dwa scenariusze: w przypadku, gdy poprzednia epidemia była mniejsza niż 12 miesięcy temu, należy rozważyć leczenie podtrzymujące TP. Jeśli poprzednia epidemia była większa niż 12 miesięcy temu, może zostać podniesiona jako terapia wspomagająca 5-ASA. Wszyscy ci pacjenci powinni mieć kolonoskopię z biopsją po 6 miesiącach, aby ocenić gojenie się błony śluzowej.
Jeśli nie zareagujesz na terapię indukcyjną kortykoidami (po 7 dniach), sugeruje się hospitalizację i rozpoczęcie leczenia zgodnie z „algorytmem leczenia ciężkiego kryzysu”.
algorytm leczenia niepoważnego rozległego zapalenia jelita grubego (2) (ryc.5)
ponieważ głównym celem leczenia UC jest osiągnięcie gojenia się błony śluzowej, ważne jest, aby wziąć pod uwagę, że ocena kliniczna może nie być wystarczająca do optymalnego leczenia tych pacjentów. Dlatego u tych pacjentów, którzy reagują klinicznie na doustne 5-ASA, powinni jednakowo towarzyszyć im CF co 4 miesięce7, 8.
Jeśli CF > 200µg / g, a pacjent utrzymuje się z pewnymi objawami, należy dostosować terapię; jeśli pacjent był leczony 5-ASA, dawkę można zwiększyć do 45 g / dzień i rozważyć dodanie miejscowego 5-ASA. Ta modyfikacja terapii powinna zostać oceniona za dwa tygodnie. Jeśli istnieje odpowiedź, kontynuuj leczenie i obserwację już opisaną. Jeśli nie ma odpowiedzi, wykonaj kolonoskopię i rozważ skalowanie do TP i/lub anty-TNF.
jeśli pacjent doświadczył TP, dawkę należy dostosować, mierząc metabolity i rozważając dodanie 5-ASA w maksymalnej dawce. Dostosowanie to należy ocenić po 4 tygodniach; jeśli wystąpi odpowiedź, utrzymuj terapię i obserwację, jeśli nie ma odpowiedzi, wykonaj kolonoskopię i zgodnie z wynikami rozważ skalowanie do anty-TNF.
jeśli pacjent był już leczony anty-TNF i miał zaostrzenie, należy wykonać kolonoskopię (z wyłączeniem nadkażenia wirusem cytomegalii ) i zmierzyć poziomy anty-TNF i przeciwciał oraz dostosować dawki zgodnie z wynikami lub ostatecznie zmienić dawki anty-TNF.
u tych pacjentów, którzy osiągnęli remisję kliniczną z 5-ASA i których CF przekraczają 200µg/g, sugeruje się wykluczenie innych czynników, takich jak: przestrzeganie leczenia, odpowiednie dawki, stosowanie środków przeciwzapalnych brak steroidy, dodane infekcje i powtórzenie nowego CF w ciągu miesiąca. Jeśli utrzymuje się wysoki poziom, rozważ wykonanie kolonoskopii, nawet jeśli pacjent jest bezobjawowy.
chociaż obecne wytyczne dotyczące leczenia są mniej rygorystyczne w odniesieniu do obserwacji za pomocą biomarkerów i optymalizacji terapii, w oparciu o aktualne dane i nowe podejście do leczenia ??treat to target?? (leczenie zgodnie z celami) powinno działać proaktywnie i wyprzedzać fakty, co pozwoli osiągnąć cel leczenia błony śluzowej i zachować go w czasie. To określi najlepszą prognozę choroby długoterminowej9.
algorytm leczenia ciężkiego kryzysu (rys.6)
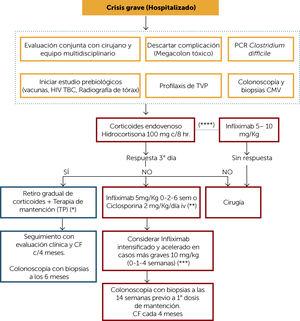
leczenie ciężkiego kryzysu UC powinno odbywać się u hospitalizowanego pacjenta i od samego początku jest oceniane przez interdyscyplinarny zespół, w tym gastroenterologa, koloproktologa, dietetyka i pielęgniarkę. Jako pierwsze przybliżenie należy wykluczyć obecność toksycznego megakolonu i zakażenia Clostridium difficile (najlepiej PCR w wypróżnieniach). Zakażenie CMV należy również rozważyć u pacjentów, którzy otrzymali sterydy przed kryzysem lub immunomodulatory (mi). Badanie to powinno odbywać się za pomocą immunohistochemii lub PCR w biopsjach endoskopowych. Należy również wziąć pod uwagę obecność jakiegoś zarodka enteropatogennego, jeśli istnieje historia epidemiologiczna wskazująca na to. Od momentu przyjęcia do szpitala, w przypadku ciężkiego zapalenia jelita grubego, należy poprosić o wstępne badanie w celu ewentualnego rozpoczęcia terapii biologicznej, która obejmuje: wyklucz przewlekłe infekcje, takie jak ludzki wirus niedoboru odporności (HIV), gruźlica z prześwietleniem klatki piersiowej, a najlepiej kwantyferon (lub w inny sposób PPD z oceną zakaźną) i przewlekłe zapalenie wątroby (wspólny środek przeciwgorączkowy dla wirusa zapalenia wątroby typu B, antygenu powierzchniowego HBV i przeciwciała przeciwwirusowego zapalenia wątroby typu C). Ponadto należy zaszczepić się co najmniej przeciwko grypie, pneumokokom i wirusowemu zapaleniu wątroby typu A i b u pacjentów, którzy wcześniej nie byli narażeni. Pacjenci z ciężkim kryzysem UC są narażeni na wysokie ryzyko zdarzeń zakrzepowych, dlatego powinni przejść profilaktykę zakrzepicy żył głębokich zgodnie z protokołem każdego centru10. ponadto część wstępnej oceny powinna obejmować kolonoskopię z biopsją w celu wykluczenia zakażenia CMV, jak już wspomniano, a także w celu oceny nasilenia endoskopowego i histologicznego. Kolonoskopię tę można wykonać bez przygotowania i najlepiej w znieczuleniu lub z odpowiednią sedacją.
 Rysunek 6.
Rysunek 6.algorytm leczenia ciężkiego kryzysu wrzodziejącego zapalenia jelita grubego
( * ) u pacjenta, który debiutuje ze swoją chorobą, może ostatecznie przejść do utrzymania 5-ASA, jeśli stwarza ryzyko TP.
( * * ) u pacjentów wcześniej nieleczonych TP należy rozważyć cyklosporynę. Rozważ w zależności od dostępności stosowanie wedolizumabu.
(***) pacjenci z hipoalbuminemią, podwyższonym CRP, niedokrwistością. Ocena odpowiedzi klinicznej po każdej dawce
( * * * * ) u zoptymalizowanego pacjenta immunorefraktycznego, 5-ASA odpowiednich dawek, u których rozwija się ciężki kryzys, infliksymab w dawkach zgodnie ze stanem klinicznym
HIV: ludzki wirus niedoboru odporności; TBC: gruźlica; DVT: zakrzepica żył głębokich; CMV: wirus cytomegalii; TP: tiopuryny; SF: kalprotektyna kałowa.
(0,75 Mb).leczenie ciężkiego kryzysu rozpoczyna się od endowenozowych kortykoidów (hydrokortyzon 100mg C / 8hrs. lub solumedrol 20mg c / 8hrs). Odpowiedź musi zostać oceniona nie później niż w dniu 3. Jeśli pojawi się odpowiedź, można ją nakładać doustnie, a następnie rozpocząć stopniowe usuwanie kortykoidów (ryc.3) Plus terapia podtrzymująca TP. U nowo zdiagnozowanych pacjentów, którzy nie byli wcześniej leczeni i zadebiutowali z ciężkim kryzysem, utrzymanie doustnego 5 – ASA można rozważyć, jeśli odpowiedź na sterydy była wczesna. Należy jednak wziąć pod uwagę, że wybór tej drugiej opcji wymaga odpowiedniego monitorowania klinicznego i CF.
Jeśli nie ma odpowiedzi na endowenozowe kortykoidy, alternatywy terapeutyczne będą zależeć od stanu pacjenta i Ośrodka. Operacja jest dobrą alternatywą u tych pacjentów, najlepiej zarządzaną przez doświadczony zespół. Medyczną alternatywą może być rozpoczęcie infliksymabu (IFX) w dawkach indukcyjnych 5 mg/kg (0-2-6 tygodni) lub endowenozowa cyklosporyna 2 mg/kg/dzień. Wybór między tymi opcjami będzie zależeć od wcześniejszego zastosowania TP w odpowiednich dawkach (w tym przypadku IFX jest opcją), doświadczenia każdego ośrodka i możliwości pomiaru poziomów cyklosporyny. U pacjentów z hipoalbuminemią, podwyższonym CRP lub niedokrwistością można rozważyć zwiększoną terapię dawkami infliksymabu 10 mg/kg po 0-1-4 tygodniu11.
u pacjentów, którzy są na odpowiednich i zoptymalizowanych dawkach (pomiar metabolitów) TP i mają poważny kryzys, sugeruje się rozpoczęcie IFX jako pierwszej terapii (z wyłączeniem długotrwałego stosowania kortykoidów w ramach programu). Dawkę if należy dostosować do stanu każdego pacjenta, jak wspomniano wcześniej.
komentarze
przedstawione tutaj algorytmy stanowią praktyczną wizję zarządzania UC przez zespół programu chorób zapalnych jelit kliniki Las Grafes, w którym uczestniczą gastroenterolodzy, koloproktolodzy i pielęgniarki, które obejmują koncepcje leczenia opartego na celach (treat to target) Moderna monitoring IBD i medycyny spersonalizowanej, które nie są przeznaczone do wytycznych klinicznych ani ogólnych wytycznych UC.
obecne leczenie UC obejmuje odpowiednią obserwację, która umożliwia wczesne wykrycie braku odpowiedzi na leczenie w sposób, który optymalizuje terapię, nawet przed epidemią kliniczną. Ta obserwacja koniecznie obejmuje interdyscyplinarną, skoordynowaną i wspieraną przez Pielęgniarstwo pracę, która ułatwia komunikację między pacjentem a zespołem opieki zdrowotnej. W ten sposób można skrócić czas reakcji i podejmowania decyzji w celu dostosowania leków, a zmiana strategii w odpowiednim czasie, poprawiając jakość życia i rokowanie pacjentów z UC.
algorytmy te będą przeprowadzane na bieżąco w zależności od nowych faktów naukowych i pojawienia się nowych alternatyw terapeutycznych.
deklaracja interesów
autorzy stwierdzają, że nie ma konfliktu interesów w tym sensie, że nie ma płatności ani finansowania dla branży i instytucji.