chimie pentru Non-majori
cum se schimbă energia acestui lucrător în timp ce urcă și coboară scara?
urcarea unei scări necesită energie. La fiecare pas, vă împingeți împotriva gravitației și acumulați energie potențială. Revenirea în jos eliberează acea energie potențială pe măsură ce coborâți pas cu pas. Dacă nu ești atent, poți elibera acea energie potențială dintr-o dată când cazi de pe scară (niciodată o idee bună). În plus, luați urcarea sau coborârea în trepte. Nu există o poziție” între ” pe scară-piciorul tău lovește o treaptă sau lovește spațiul gol și ai probleme până găsești o treaptă pe care să stai.

În urma descoperirilor spectrelor de emisie de hidrogen și a efectului fotoelectric, fizicianul danez Niels Bohr (1885-1962) a propus un nou model al atomului în 1915. Bohr a propus că electronii nu radiază energie pe măsură ce orbitează nucleul, ci există în stări de energie constantă pe care el le-a numit stări staționare. Aceasta înseamnă că electronii orbitează la distanțe fixe față de nucleu (vezi figura de mai jos). Lucrarea lui Bohr s-a bazat în primul rând pe spectrele de emisie ale hidrogenului. Acesta este denumit și modelul planetar al atomului. A explicat funcționarea interioară a atomului de hidrogen. Bohr a primit Premiul Nobel pentru Fizică în 1922 pentru munca sa.
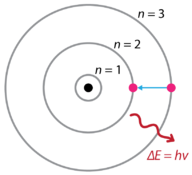
Figura 1. Modelul atomic al lui Bohr spectrele de emisie de hidrogen.
Bohr a explicat că electronii pot fi mutați în orbite diferite cu adăugarea de energie. Când energia este îndepărtată, electronii revin la starea lor de bază, emițând o cantitate corespunzătoare de energie – un cuantum de lumină sau foton. Aceasta a fost baza pentru ceea ce mai târziu a devenit cunoscut sub numele de teoria cuantică . Aceasta este o teorie bazată pe principiul că materia și energia au proprietățile atât ale particulelor, cât și ale undelor. Acesta explică o gamă largă de fenomene fizice, inclusiv existența unor pachete discrete de energie și materie, principiul incertitudinii și principiul excluderii.
conform modelului Bohr, adesea denumit model planetar, electronii înconjoară nucleul atomului în căi specifice permise numite orbite. Când electronul se află într-una din aceste orbite, energia sa este fixă. Starea de bază a atomului de hidrogen, unde energia sa este cea mai mică, este atunci când electronul se află pe orbita cea mai apropiată de nucleu. Orbitele care sunt mai departe de nucleu sunt toate cu o energie succesiv mai mare. Electronului nu i se permite să ocupe niciunul dintre spațiile dintre orbite. O analogie de zi cu zi cu modelul Bohr este treptele unei scări. Pe măsură ce vă deplasați în sus sau în jos pe o scară, puteți ocupa doar anumite trepte și nu puteți fi în spațiile dintre trepte. Urcarea scării crește energia potențială, în timp ce coborârea scării scade energia.
lucrarea lui Bohr a avut o influență puternică asupra înțelegerii noastre moderne a funcționării interioare a atomului. Cu toate acestea, modelul său a funcționat bine pentru o explicație a emisiilor atomului de hidrogen, dar a fost serios limitat atunci când a fost aplicat altor atomi. La scurt timp după ce Bohr și-a publicat modelul planetar al atomului, au fost făcute mai multe descoperiri noi, ceea ce a dus, din nou, la o viziune revizuită a atomului.
rezumat
- Modelul Bohr postulează că electronii orbitează nucleul la niveluri fixe de energie.
- orbitele mai departe de nucleu există la niveluri de energie mai ridicate.
- când electronii revin la un nivel de energie mai scăzut, ei emit energie sub formă de lumină.
practică
folosiți linkul de mai jos pentru a răspunde la următoarele întrebări:
- Cum schimbă orbitele unui electron?pe ce se baza Modelul Bohr?
- ce credea Bohr despre orbite?
- modelul lui Bohr funcționează pentru toți atomii?
recenzie
- când a propus Bohr modelul său de atom?
- ce este o stare staționară?
- care este starea de bază?
- poate electronul să ocupe orice spațiu între orbite?
Glosar
- model planetar: o modalitate de a descrie modelul atomului lui Bohr.
- teoria cuantică: Materia și energia au proprietățile particulelor și undelor.
- stare staționară: electronii orbitează la o distanță fixă de nucleu.