Homochiralitatea biologică: Unul dintre cele mai mari mistere ale vieții

în fiecare formă de viață de pe pământ, zaharurile sunt întotdeauna dreptaci, iar aminoacizii sunt întotdeauna stângaci. Ce înseamnă asta și de ce se întâmplă? Acest fenomen bizar implică molecule chirale și este cunoscut sub numele de „homochiralitate”.”
moleculele chirale sunt molecule cu aceeași formulă, dar cu structuri ușor diferite. Mâna ta este un obiect chiral, deoarece nu se suprapune pe imaginea sa în oglindă; când așezați mâna stângă peste dreapta, degetele mari vor indica în direcții diferite. În moleculele organice, atunci când patru grupuri diferite înconjoară un carbon central, molecula va avea două forme chirale diferite numite enantiomeri. Aceste două molecule sunt imagini în oglindă una cu cealaltă, deoarece grupurile din jurul carbonului sunt orientate în direcții diferite, cum ar fi mâinile drepte și stângi. În chimie, acești compuși sunt numiți enantiomeri R și s (sau izomeri). Cu toate acestea, atunci când aminoacizii sau zaharurile sunt chirale, oamenii de știință le numesc izomeri D și L (oamenii de știință sunt teribili în a numi lucrurile în mod consecvent). D-înseamnă ” dreptaci „și L – înseamnă” stângaci.”

izomerii D și L sunt prezenți în mod normal într-un raport 50/50. Chimiștii numesc acest amestec racemic. Desigur, te-ai aștepta ca amândoi să fie la fel de prezenți în corpul nostru, nu? Greșit! De fapt, toate formele de viață folosesc doar l-aminoacizi și D-zaharuri. Prezența unui singur izomer se numește homochiralitate. De la cele mai mici bacterii la elefanți, numai l-aminoacizii alcătuiesc proteine și numai d-zaharurile alcătuiesc polizaharide. Cu alte cuvinte, toate proteinele sunt dreptaci și toate polizaharidele sunt stângaci*. De ce este asta? Este un mister care i-a nedumerit pe biologi de ani de zile. În ciuda eforturilor depuse de fizicieni, chimiști și biologi evoluționiști, încă nu știm sigur. Aici, vom arunca o privire la unele dintre cele mai importante teorii actuale.
*(trebuie remarcat faptul că unele zaharuri L pot fi, de asemenea, defalcate pe căi metabolice. Zaharurile pot forma inele, iar zahărul D formează un inel mai stabil decât zahărul L, dar zaharurile L pot exista în continuare. Stabilitatea inelului poate fi principalul factor care contribuie la prevalența zaharurilor D. Mai jos, ne vom concentra în principal pe aminoacizi, care aderă strict la o singură formare chirală în sistemele biologice.)
enzime și Evoluție

Iată ce știm: enzimele din celule pot metaboliza doar un izomer, dar nu și celălalt. Enzimele catalizează reacțiile pentru a descompune și construi molecule prin legarea lor în moduri foarte specifice. O enzimă care descompune D-glucoza nu va putea descompune L-glucoza. Dacă am dori să folosim și să construim ambii izomeri, ar trebui să avem două seturi de enzime. Acest lucru ar necesita mai mult ADN, mai multă hrană și mult mai multă energie. În mod natural, celulele doresc să fie cât mai eficiente posibil, astfel încât să aibă un set suplimentar de enzime ar fi impozitarea.
dar dacă am avea acele enzime suplimentare, nu am putea obține de asemenea de două ori mai multă energie din mediu? Am putea folosi celelalte 50% din izomeri dacă am avea enzimele pentru a le descompune în loc să le irosim. Răspunsul are legătură cu evoluția și piramida alimentară.
când viața timpurie evolua, un organism ar avea enzime care reacționează selectiv cu un izomer. Organismele care au mâncat această primă formă de viață ar trebui să aibă aceleași enzime selective pentru a le digera. Dacă toate alimentele dvs. conțin doar zaharuri D, la fel veți face și voi! Deci, dacă partea de jos a lanțului alimentar folosește doar l-aminoacizi, homochiralitatea se va răspândi la fiecare organism din lanțul alimentar! Deoarece viața a trebuit să dezvolte mai întâi un set de enzime, am ajuns să fim blocați cu acea selectivitate. Presiunea selectivă din evoluție a forțat fiecare nou organism să utilizeze aceleași tipuri de aminoacizi și zahăr ca și cele anterioare.
Deci, odată ce un izomer este ales, fiecare formă de viață îl va folosi. Dar de ce L-aminoacizi în loc de D-aminoacizi și de ce d-zaharuri în loc de l-zaharuri? Acesta este adevăratul mister. Ceva la începutul vieții a trebuit să aleagă unul peste celălalt. Este posibil ca în primele etape ale vieții, unele organisme să dezvolte un set de enzime, în timp ce diferite organisme au avut celălalt. Ar fi putut fi un eveniment aleatoriu care a distrus o linie de enzime, dar oamenii de știință nu sunt mulțumiți de acest răspuns. Trebuie să existe un motiv pentru care L-aminoacizii și D-zaharurile sunt mai bune pentru supraviețuire decât omologii lor.
Enter Physics
amestecurile racemice sunt 50/50 amestecuri ale celor doi izomeri. Dar există motive să credem că în sistemul nostru stelar, există de fapt o ușoară preferință energetică pentru un izomer față de celălalt. Pentru a înțelege această preferință, trebuie să călătorim adânc în Calea Lactee.
galaxia noastră are un spin chiral și o orientare magnetică. Acest lucru face ca praful cosmic să polarizeze circular lumina într-o singură direcție. Practic, deoarece lumina este o undă 2-dimensională, se va propaga într-o helix. Praful cosmic face ca această helix să se rotească preferențial într-o direcție.

lumină polarizată. Polarizarea opusă se învârte în cealaltă direcție.
această lumină polarizată circular degradează d-aminoacizii mai mult decât l-aminoacizii, deci l-aminoacizii sunt mai stabili. Acest lucru este susținut de studiile meteorilor și cometelor. Materia cosmică, cel puțin în Calea Lactee, are o preferință pentru L-aminoacizi datorită polarizării circulare a luminii.
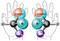
o altă explicație fizică pentru preferința unui izomer față de celălalt are legătură cu forța electroslabă. Există patru forțe fundamentale care guvernează fizica: gravitația, electromagnetismul, forța nucleară puternică și forța electroweak (alias forța nucleară slabă). Primele trei sunt achirale: afectează izomerii L și D în același mod. Cu toate acestea, forța electroslabă este afectată de Chiralitate. Forța electroslabă guvernează dezintegrarea radioactivă a atomilor și moleculelor. În această decădere, paritatea universului nu este întotdeauna păstrată. În timpul dezintegrării beta, electronii emiși favorizează un tip de rotire. Spinul electronilor degradează din nou D-aminoacizii mai mult decât l-aminoacizii, determinând schimbarea echilibrului moleculelor în favoarea izomerului L.
Autocataliză
odată ce fizica dă o ușoară margine unui izomer față de celălalt, există un motiv chimic care amplifică diferența. Autocataliza înseamnă că prezența unei substanțe chimice stimulează propria producție. În jurul anului 1950, F. C. Frank a sugerat că izomerii dominanți își pot activa propria producție în timp ce suprimă producția celuilalt izomer.

din „originea Homochiralității biologice” de Donna blackmond
graficul de mai sus ilustrează punctul. Când începeți cu 3 izomeri L și 2 izomeri D,raportul poate fi amplificat foarte rapid, astfel încât izomerii L depășesc cu mult izomerii D. Izomerul L stimulează propria producție, iar izomerul L se leagă și de izomerul D într-un proces numit „antagonism reciproc.”Acest lucru previne formarea mai multor izomeri D, iar izomerul L este favorizat rapid.acesta a fost doar un cadru ipotetic pentru a explica de ce avem doar L-aminoacizi și D-zaharuri. Dar acest concept a câștigat sprijin atunci când a fost descoperită reacția Soai. Aceasta este o demonstrație a modului în care anumiți izomeri pot fi favorizați față de alții în procesele biologice. Deși nu există dovezi că autocatliza omniprezentă provoacă homochiralitate, poate fi cu siguranță un factor de amplificare în unele cazuri.
un Model de lucru
astăzi, cea mai populară teorie pentru homochiralitatea biologică include toate aceste concluzii. Fenomenele fizice, cum ar fi lumina polarizată și forța electroslabă, creează un ușor dezechilibru al izomerilor D și L. Această mică discrepanță este amplificată într-un dezechilibru mai inegal prin autocataliză. Apoi, odată ce viața a fost formată, un singur izomer a fost selectat rapid de lanțul alimentar și de specificitatea enzimelor. Astfel, astăzi vedem doar l-aminoacizi și D-zaharuri.
această teorie are încă câteva găuri. S-ar putea să nu existe niciodată o explicație perfectă pentru un eveniment care a început cu miliarde de ani în urmă. Dar acum avem cel puțin o soluție potențială pentru misterul homochiralității biolgice.
„misterul creează uimire, iar minunea este baza dorinței omului de a înțelege.”—Neil Armstrong