8.3: Orbital magnetiskt dipolmoment för elektronen
inlärningsmål
i slutet av detta avsnitt kommer du att kunna:
- förklara varför väteatomen har magnetiska egenskaper
- förklara varför energinivåerna för en väteatom associerad med orbital vinkelmoment delas av ett yttre magnetfält
- använd kvantnummer för att beräkna storleken och riktningen för det orbitala magnetiska dipolmomentet för en väteatom
i Bohrs modell av väteatomen rör sig elektronen i en cirkulär bana runt protonen. Elektronen passerar en viss punkt på slingan under en viss tid, så vi kan beräkna en ström \(i = Q/t\). En elektron som kretsar kring en proton i en väteatom är därför analog med ström som strömmar genom en cirkulär tråd (figur \(\PageIndex{1}\)). I studien av magnetism såg vi att en strömbärande tråd producerar magnetfält. Det är därför rimligt att dra slutsatsen att väteatomen producerar ett magnetfält och interagerar med andra magnetfält.
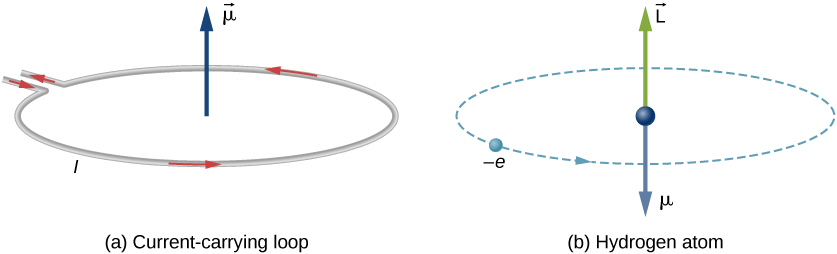
det orbitala magnetiska dipolmomentet är ett mått på styrkan hos magnetfältet som produceras av en elektrons orbitala vinkelmoment. Från Kraft och vridmoment på en strömslinga är storleken på det orbitala magnetiska dipolmomentet för en strömslinga
\
där \(i\) är strömmen och \(A\) är slingans område. (För korthet hänvisar vi till detta som det magnetiska ögonblicket.) Strömmen\ (I\) associerad med en elektron i omlopp kring en proton i en väteatom är
\
där e är storleken på elektronladdningen och\ (T\) är dess omloppsperiod. Om vi antar att elektronen färdas i en perfekt cirkulär bana, är omloppsperioden
\
där r är omloppets radie och v är elektronens hastighet i sin omlopp. Med tanke på att området för en cirkel är \(\pi r^2\), är det absoluta magnetiska momentet
\
det är bra att uttrycka det magnetiska momentumetcr i termer av Orbital vinkelmoment (\(\vec{L} = \vec{r} \times\vec{p}\)). Eftersom elektronen kretsar i en cirkel bildar positionsvektorn \(\vec{r}\) och momentumvektorn \(\vec{p}\) en rätt vinkel. Således är storleken på orbital vinkelmomentet
\
genom att kombinera dessa två ekvationer har vi
\
i full vektorform skrivs detta uttryck som
\
det negativa tecknet visas eftersom elektronen har en negativ laddning. Lägg märke till att riktningen för elektronens magnetiska moment är antiparallell mot orbitalvinkelmomentet, som visas i Figur \(\PageIndex{1b}\). I atomens Bohr-modell är förhållandet mellan \(\vec{\mu}\) och \(\vec{l}\) i ekvation \ref{BIG} oberoende av omloppets radie.
det magnetiska momentet \(XHamster\) kan också uttryckas i termer av det orbitala vinkelkvantumtalet \(l\). Kombinera ekvation \ref{eq2} och ekvation \ref{eq1}, storleken på det magnetiska ögonblicket är
\
z-komponenten i det magnetiska ögonblicket är
\ &= – \left(\dfrac{e}{2m_e}\right) \, m \hbar \\ &= – \mu_b m. \label{EQ6} \end{align}\]
kvantiteten \(\mu_b\) är en grundläggande magnetismenhet som kallas Bohr Magneton, som har värdet \(9,3 \gånger 10^{-24} \, joule/Tesla\) (j/t) eller \(5,8 \gånger 10^{-5} ev/t\). Kvantisering av det magnetiska ögonblicket är resultatet av kvantisering av orbitalvinkelmomentet.
som vi kommer att se i nästa avsnitt beror det totala magnetiska dipolmomentet för väteatomen på både elektronens orbitalrörelse och dess inneboende snurrning. För närvarande ignorerar vi effekten av elektronspinn.
exempel \(\PageIndex{1}\): orbitalt magnetiskt dipolmoment
vad är storleken på det orbitala dipolmagnetmomentet för en elektron i väteatomen i (a) S-tillståndet, (b) p-tillståndet och (c) D-tillståndet? (Antag att elektronens rotation är noll.)
strategi
elektronens magnetiska momentum är relaterad till dess orbitala vinkelmoment L. för väteatomen är denna kvantitet relaterad till orbitalvinkelkvantumtalet l. tillstånden ges i spektroskopisk notation, som relaterar en bokstav (s, p, d, etc.) till ett kvantnummer.
lösning
storleken på det magnetiska momentet anges i ekvation \ref{eq5}:
\&= \vänster(\dfrac{e}{2m_e}\höger) \, \sqrt{l(L + 1)} \hbar \nonumber \ \ &= \mu_b\sqrt{L(L + 1)}. \ end{align}\]
- för S-tillståndet, \(l = 0\) så vi har \(\mu = 0\) och \(\mu_z = 0\).
- för p-tillståndet, \(l = 0\) och vi har \ \ var \(m = (-1, 0, 1)\) Så \
- för D-tillståndet, \(l = 2\) och vi får \ \ var \(m = (-2, -1, 0, 1, 2)\) Så \
betydelse
I s-tillståndet finns det ingen orbital vinkelmoment och därför inget magnetiskt ögonblick. Detta betyder inte att elektronen är i vila, bara att elektronens totala rörelse inte producerar ett magnetfält. I P-tillståndet har elektronen ett magnetiskt ögonblick med tre möjliga värden för z-komponenten i detta magnetiska ögonblick; detta innebär att magnetiskt ögonblick kan peka i tre olika polära riktningar—var och en antiparallell mot orbital vinkelmomentvektorn. I d-tillståndet har elektronen ett magnetiskt ögonblick med fem möjliga värden för z-komponenten i detta magnetiska ögonblick. I detta fall kan det magnetiska ögonblicket peka i fem olika polära riktningar.
en väteatom har ett magnetfält, så vi förväntar oss att väteatomen ska interagera med ett externt magnetfält—som att trycka och dra mellan två stångmagneter. Från Kraft och vridmoment på en strömslinga vet vi att när en strömslinga interagerar med ett externt magnetfält \(\vec{b}\), upplever det ett vridmoment som ges av
\
Där jag är strömmen, \(\vec{a}\) är slingans område, \(\vec{\mu}\) är det magnetiska ögonblicket och \(\vec{B}\) är det externa magnetfältet. Detta vridmoment verkar för att rotera väteatomens magnetiska momentvektor för att anpassa sig till det yttre magnetfältet. Eftersom mekaniskt arbete utförs av det yttre magnetfältet på väteatomen kan vi prata om energitransformationer i atomen. Den potentiella energin hos väteatomen associerad med denna magnetiska interaktion ges av ekvation \ref{eq30}:
\
om det magnetiska ögonblicket är antiparallellt med det yttre magnetfältet är den potentiella energin stor, men om det magnetiska ögonblicket är parallellt med fältet är den potentiella energin liten. Arbete som utförs på väteatomen för att rotera atomens magnetiska momentvektor i riktning mot det yttre magnetfältet är därför förknippat med en minskning av potentiell energi. Systemets energi bevaras dock eftersom en minskning av potentiell energi producerar strålning (utsläpp av en foton). Dessa energiövergångar kvantiseras eftersom det magnetiska ögonblicket endast kan peka i vissa riktningar.
om det externa magnetfältet pekar i den positiva z-riktningen är den potentiella energin associerad med det orbitala magnetiska dipolmomentet
\
där \(\mu_B\) är Bohr magneton och m är vinkelmomentprojektionskvanttal (eller magnetiskt orbitalkvantumtal), som har värdena
\
till exempel i \(l = 1\) elektrontillstånd delas elektronens totala energi i tre distinkta energinivåer motsvarar \(u = -\mu_b B, 0, \mu_b b\).
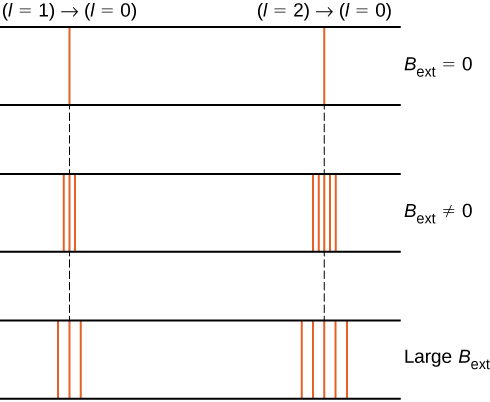
uppdelningen av energinivåer med ett externt magnetfält kallas Zeeman-effekten. Ignorera effekterna av elektronspinn, övergångar från \(l = 1\) till ett gemensamt lägre energitillstånd producerar tre nära åtskilda spektrallinjer (figur \(\PageIndex{2}\), vänster kolumn). På samma sätt producerar övergångar från \(l = 2\) staten fem nära åtskilda spektrallinjer (höger kolumn). Separationen av dessa linjer är proportionell mot styrkan hos det yttre magnetfältet. Denna effekt har många tillämpningar. Till exempel används splittringen av linjer i solens vätespektrum för att bestämma styrkan hos solens magnetfält. Många sådana magnetfältmätningar kan användas för att göra en karta över den magnetiska aktiviteten vid solens yta som kallas ett magnetogram (figur \(\PageIndex{3}\)).

bidragsgivare och attribut
Samuel J. Ling (Truman State University), Jeff Sanny (Loyola Marymount University) och Bill Moebs med många bidragande författare. Detta verk är licensierat av OpenStax University Physics under en Creative Commons Attribution License (av 4.0).