5.3: Lewisin diagrammit
Lewis käytti yksinkertaisia diagrammeja (joita nykyään kutsutaan Lewisin diagrammeiksi) pitääkseen kirjaa siitä, kuinka monta elektronia oli tietyn atomin uloimmassa eli valenssikuoressa. Atomin ydin eli ydin yhdessä sisempien elektronien kanssa esitetään kemiallisella symbolilla, ja vain valenssielektronit piirretään kemiallisen symbolin ympärillä olevina pisteinä. Näin kuvan 1 kolme atomia elektroneista ja Valenssista voidaan esittää seuraavilla Lewisin diagrammeilla:
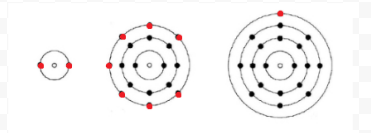

Jos atomi on jalokaasuatomi, on kaksi vaihtoehtoista menetelmää mahdollista. Joko voimme katsoa, että atomilla on nolla valenssielektronia tai voimme pitää ulointa täytettyä kuorta valenssikuorena. Kolme ensimmäistä jalokaasua voidaan siis kirjoittaa seuraavasti:
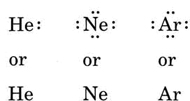
esimerkki \(\PageIndex{1}\): Lewis-rakenteet
Piirrä Lewis-diagrammit atomille jokaisesta seuraavista alkuaineista: Li, N, F, Na
ratkaisu
huomaamme etukannen sisällä olevasta jaksollisesta järjestelmästä, että Li: n järjestysluku on 3. Siinä on siis kolme elektronia, yksi enemmän kuin jalokaasussa He. Tällöin uloimmassa eli valenssikuoressa on vain yksi elektroni, ja Lewisin Diagrammi on
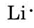
saman päättelyn mukaan N:llä on seitsemän elektronia, viisi enemmän kuin hänellä, kun taas F: llä on yhdeksän elektronia, seitsemän enemmän kuin hänellä, jolloin
![]()
Na: lla on yhdeksän elektronia enemmän kuin hänellä, mutta niistä kahdeksan on ytimessä, mikä vastaa Ne: n uloimman kuoren kahdeksaa elektronia. Koska Na: ssa on vain 1 elektroni enemmän kuin Ne:ssä, sen Lewisin Diagrammi on
![]()
huomaa edellisestä esimerkistä, että alkalimetallien Lewis-diagrammit ovat identtisiä lukuun ottamatta niiden kemiallisia symboleja. Tämä sopii hyvin yhteen alkalimetallien hyvin samankaltaisen kemiallisen käyttäytymisen kanssa. Samoin Lewisin diagrammit muiden ryhmien kaikille alkuaineille, kuten emäksisille maametalleille tai halogeeneille, näyttävät samoilta.
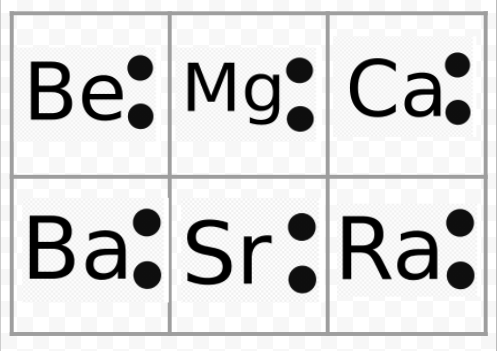
Lewisin diagrammeja voidaan käyttää myös alkuaineiden valenssien ennustamiseen. Lewis esitti, että atomin valenssien määrä oli yhtä suuri kuin sen valenssikuoressa olevien elektronien lukumäärä tai niiden elektronien lukumäärä, jotka olisi lisättävä valenssikuoreen saavuttaakseen seuraavan jalokaasun elektronikuorirakenteen. Esimerkkinä tästä ajatuksesta pidetään alkuaineita Be ja O. niiden Lewis-diagrammit sekä jalokaasujen He ja Ne

vertaamalla olla hän, näemme, että ensin mainitulla on kaksi elektronia enemmän ja siksi sen valenssi olisi 2. Alkuaineen O voidaan olettaa olevan valenssi 6 tai valenssi 2, koska sillä on kuusi valenssielektronia-kaksi vähemmän kuin Ne. Näin kehitettyjen valenssisääntöjen avulla Lewis pystyi selittämään valenssiosasta löydetyn taulukon yhdisteiden alaindeksien säännöllisen kasvun ja vähenemisen, ja toistamaan sen tässä. Lisäksi hänen osuutensa taulukossa olevista formuloista oli yli 50 prosenttia. (Ne, jotka ovat samaa mieltä hänen ajatuksensa ovat tummennetut väri taulukossa. Saatat haluta viitata tähän taulukkoon nyt ja tarkistaa, että jotkut ilmoitetut kaavat noudattavat Lewisin sääntöjä.) Lewisin menestys tässä yhteydessä osoitti selvästi, että elektronit olivat tärkein tekijä atomien pitämisessä koossa molekyylien muodostuessa.
näistä menestyksistä huolimatta Lewisin teorioissa on myös vaikeuksia, erityisesti jaksollisen järjestelmän kalsiumin ulkopuolisille alkuaineille. Esimerkiksi alkuaineella Br (Z = 35) on 17 elektronia enemmän kuin jalokaasulla Ar (Z = 18). Tästä voidaan päätellä, että Br: llä on 17 valenssielektronia, minkä vuoksi on kiusallista selittää, miksi Br muistuttaa Cl: ää ja F: ää niin läheisesti, vaikka näillä kahdella atomilla on vain seitsemän valenssielektronia.
| Element | Atomic Weight | Hydrogen Compounds | Oxygen Compounds | Chlorine Compounds |
|---|---|---|---|---|
| Hydrogen | 1.01 | H2 | H2O, H2O2 | HCl |
| Helium | 4.00 | None formed | None formed | None formed |
| Lithium | 6.94 | LiH | Li2O, Li2O2 | LiCl |
| Beryllium | 9.01 | BeH2 | BeO | BeCl2 |
| Boron | 10.81 | B2H6 | B2O3 | BCl3 |
| Carbon | 12.01 | CH4, C2H6, C3H8 | CO2, CO, C2O3 | CCl4, C2Cl6 |
| Nitrogen | 14.01 | NH3, N2H4, HN3 | N2O, NO, NO2, N2O5 | NCl3 |
| Oxygen | 16.00 | H2O, H2O2 | O2, O3 | <Cl2O, ClO2, Cl2O7 |
| Fluorine | 19.00 | HF | OF2, O2F2 | ClF, ClF3, ClF5 |
| Neon | 20.18 | None formed | None formed | None formed |
| Sodium | 22.99 | NaH | Na2O, Na2O2 | NaCl |
| Magnesium | 24.31 | MgH2 | MgO | MgCl2 |
| Aluminum | 26.98 | AlH3 | Al2O3 | AlCl3 |
| Silicon | 28.09 | SiH4, Si2H6 | SiO2 | SiCl4, Si2Cl6 |
| Phosphorus | 30.97 | PH3, P2H4 | P4O10, P4O6 | PCl3, PCl5, P2Cl4 |
| Sulfur | 32.06 | H2S, H2S2 | SO2, SO3 | S2Cl2, SCl2, SCl4 |
| Chlorine | 35.45 | HCl | Cl2O, ClO2, Cl2O7 | Cl2 |
| Potassium | 39.10 | KH | K2, K2O2, KO2 | KCl |
| Argon | 39.95 | None formed | None formed | None formed |
| Calcium | 40.08 | CaH2 | CaO, CaO2 | CaCl2 |
| Scandium | 44.96 | Relatively Unstable | Sc2O3 | ScCl3 |
| Titanium | 47.90 | TiH2 | TiO2, Ti2O3, TiO | TiCl4, TiCl3, TiCl2 |
| Vanadium | 50.94 | VH2 | V2O5, V2O3, VO2, VO | VCl4, VCl3, VCl2 |
| Chromium | 52.00 | CrH2 | Cr2O3, CrO2, CrO3 | CrCl3, CrCl2 |
Contributors
-
Ed Vitz (Kutztown University), John W. Moore (UW-Madison), Justin Shorb (Hope College), Xavier Prat-Resina (Minnesotan Rochesterin yliopisto), Tim Wendorff ja Adam Hahn.