biologinen Homokiraalisuus: Yksi elämän suurimmista mysteereistä
div>heinä 13, 2016 · 7 min read

jokaisessa maapallon eliömuodossa sokerit ovat aina oikeakätisiä ja aminohapot aina vasenkätisiä. Mitä tämä merkitsee ja miksi se tapahtuu? Tämä omituinen ilmiö liittyy kiraalisiin molekyyleihin ja sitä kutsutaan ”homokiraalisuudeksi.”
Kiraaliset molekyylit ovat molekyylejä, joilla on sama kaava, mutta hieman erilaiset rakenteet. Kätesi on kiraalinen esine, koska se ei ole päällekkäin peilikuvansa kanssa; kun asetat vasemman kätesi oikean päälle, peukalosi osoittavat eri suuntiin. Orgaanisissa molekyyleissä, kun neljä eri ryhmää ympäröi keskushiiltä, molekyylillä on kaksi eri kiraalista muotoa, joita kutsutaan enantiomeereiksi. Nämä kaksi molekyyliä ovat toistensa peilikuvia, sillä hiiltä ympäröivät ryhmät suuntautuvat eri suuntiin, kuten oikea ja vasen käsi. Kemiassa näitä yhdisteitä kutsutaan R-ja S-enantiomeereiksi (tai isomeereiksi). Kuitenkin, kun aminohapot tai sokerit ovat kiraalisia, tutkijat kutsuvat niitä D-ja L-isomeereiksi (tutkijat ovat huonoja nimeämään asioita johdonmukaisesti). D tarkoittaa oikeakätistä ja L vasenkätistä.”

d-ja L-isomeerien suhde on yleensä 50/50. Kemistit kutsuvat tätä raseemiseksi seokseksi. Luonnollisesti heidän molempien pitäisi olla yhtä läsnä kehossamme, eikö niin? Väärin! Itse asiassa kaikki elämänmuodot käyttävät vain L-aminohappoja ja D-sokereita. Vain yhden isomeerin esiintymistä kutsutaan homokiraliteetiksi. Pienimmistä bakteereista norsuihin vain L-aminohapot muodostavat proteiineja ja vain D-sokerit muodostavat polysakkarideja. Toisin sanoen kaikki proteiinit ovat oikeakätisiä ja kaikki polysakkaridit vasenkätisiä*. Mistä tämä johtuu? Se on mysteeri, joka on hämmentänyt biologeja vuosia. Fyysikoiden, kemistien ja evoluutiobiologien parhaista ponnisteluista huolimatta emme vieläkään tiedä varmasti. Tässä, tarkastelemme joitakin johtavia nykyisiä teorioita.
*(on huomattava, että jotkut L-sokerit voivat myös hajota aineenvaihduntareittien mukaan. Sokerit voivat muodostaa renkaita, ja D-sokeri muodostaa vakaamman renkaan kuin L-sokeri, mutta L-sokereita voi silti olla olemassa. Renkaan stabiilisuus voi olla tärkein tekijä D-sokerien yleisyydessä. Alla keskitymme pääasiassa aminohappoihin, jotka noudattavat tiukasti yhtä kiraalista muodostumista biologisissa järjestelmissä.)
entsyymit ja evoluutio

div>
Here ’ s what we do know: solujen entsyymit voivat metaboloida vain toista isomeeria, mutta eivät toista. Entsyymit katalysoivat reaktioita, jotka hajottavat ja rakentavat molekyylejä sitoutumalla niihin hyvin spesifisillä tavoilla. D-glukoosia hajottava entsyymi ei kykene hajottamaan L-glukoosia. Jos haluaisimme käyttää ja rakentaa molempia isomeerejä, meillä pitäisi olla Kahdet entsyymit. Tämä vaatisi enemmän DNA: ta, enemmän ruokaa ja paljon enemmän energiaa. Solut haluavat luonnollisesti olla mahdollisimman tehokkaita, joten ylimääräisten entsyymien saaminen olisi verottavaa.
mutta jos meillä olisi niitä ylimääräisiä entsyymejä, emmekö voisi saada myös kaksi kertaa enemmän energiaa ympäristöstä? Voisimme käyttää loput 50% isomeereistä, jos meillä olisi entsyymit hajottamaan ne tuhlaamisen sijaan. Vastaus liittyy evoluutioon ja ruokapyramidiin.
varhaisiän kehittyessä eliöllä olisi entsyymejä, jotka selektiivisesti reagoivat yhden isomeerin kanssa. Eliöillä, jotka söivät tätä ensimmäistä elämänmuotoa, pitäisi olla samat selektiiviset entsyymit sulattaakseen ne. Jos kaikki ruokasi sisältää vain D-sokereita, niin sinäkin! Jos siis ravintoketjun pohja käyttää vain L-aminohappoja, homokiraalisuus leviää ravintoketjun jokaiseen eliöön! Koska elämän piti ensin kehittää yhdet entsyymit, päädyimme siihen valikoivuuteen. Evoluution aiheuttama selektiivinen paine pakotti jokaisen uuden eliön käyttämään samoja aminohappo-ja sokerityyppejä kuin edeltäjänsä.
joten kun yksi isomeeri on poimittu, jokainen elämänmuoto käyttää sitä. Mutta miksi L-aminohappoja d-aminohappojen sijaan ja miksi D-sokereita L-sokerien sijaan? Tämä on todellinen mysteeri. Jokin aivan elämän alussa oli valita yksi yli muiden. On mahdollista, että elämän alkuvaiheissa joillekin eliöille kehittyi yksi entsyymijoukko, kun taas eri eliöillä oli toinen. Se saattoi olla satunnainen tapahtuma, joka tuhosi yhden entsyymilinjan, mutta tutkijat eivät ole tyytyväisiä tähän vastaukseen. Täytyy olla jokin syy, että L-aminohapot ja D-sokerit ovat selviytymisen kannalta parempia kuin vastineensa.
Enter fysiikka
Raseemiset seokset ovat 50/50 kahden isomeerin seoksia. On kuitenkin syytä uskoa, että tähtijärjestelmässämme on itse asiassa jonkin verran energiaa, joka suosii yhtä isomeeriä toiseen nähden. Ymmärtääksemme tämän mieltymyksen meidän on matkattava syvälle Linnunrataan.
galaksissamme on kiraalinen spin ja magneettinen orientaatio. Tämä saa kosmisen pölyn kiertämään valoa yhteen suuntaan. Koska valo on 2-ulotteinen aalto, se etenee kierteellä. Kosminen pöly saa tämän kierteen kiertymään mieluiten yhteen suuntaan.

tämä ympyräpolarisoitunut valo hajottaa D-aminohappoja enemmän kuin L-aminohappoja, joten L-aminohapot ovat stabiilimpia. Tätä tukevat meteoreja ja komeettoja koskevat tutkimukset. Kosminen aine suosii ainakin Linnunradassa L-aminohappoja valon ympyräpolarisaation vuoksi.
toinen fysikaalinen selitys yhden isomeerin suosimiselle toiseen nähden liittyy sähkövoimaan. Fysiikkaa hallitsevat neljä perusvoimaa: gravitaatio, sähkömagnetismi, vahva ydinvoima ja sähköheikko voima (alias heikko ydinvoima). Kolme ensimmäistä ovat akiraalisia: ne vaikuttavat L – ja D-isomeereihin samalla tavalla. Sähkövoimaan vaikuttaa kuitenkin siraalisuus. Sähköheikkous hallitsee atomien ja molekyylien radioaktiivista hajoamista. Tässä rappeutumisessa kaikkeuden pariteetti ei aina säily. Beetahajoamisen aikana emittoituneet elektronit suosivat yhtä spin-tyyppiä. Elektronien spin hajottaa jälleen D-aminohappoja enemmän kuin L-aminohappoja, jolloin molekyylien tasapaino muuttuu L-isomeerin hyväksi.
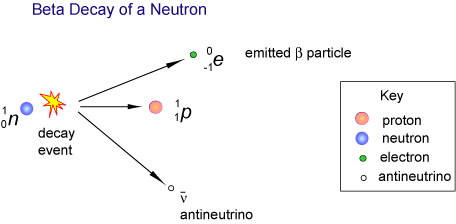
sekä polarisoitunut valo että sähköheikko hajoaminen vaikuttavat siihen, että yksi isomeeri suosii hieman toista galaksissamme. Tämä ristiriita ei kuitenkaan riitä selittämään, miksi kaikki elämänmuodot käyttävät vain D-sokereita ja L-aminohappoja. Täytyy olla jotain muutakin. Mikä johtaa …
Autokatalyysi
kun fysiikka antaa hieman särmää yhdelle isomeerille yli muiden, on olemassa kemiallinen syy, joka vahvistaa eroa. Autokatalyysi tarkoittaa, että läsnäolo kemikaali stimuloi omaa tuotantoa. Vuoden 1950 tienoilla F. C. Frank esitti, että dominoivat isomeerit voivat aktivoida oman tuotantonsa samalla kun ne tukahduttavat toisen isomeerin tuotannon.

yllä oleva grafiikka havainnollistaa asiaa. Aloitettaessa 3 L-isomeerillä ja 2 D-isomeerillä suhde voi monistua hyvin nopeasti, jolloin L-isomeerejä on huomattavasti enemmän kuin D-isomeerejä. L-isomeeri stimuloi omaa tuotantoaan, ja L-isomeeri sitoutuu myös D-isomeeriin prosessissa, jota kutsutaan ”keskinäiseksi antagonismiksi.”Tämä estää useampien D-isomeerien muodostumisen, ja L-isomeeri suositaan nopeasti.
Tämä oli vain hypoteettinen kehys selittämään, miksi meillä on vain L-aminohappoja ja D-sokereita. Käsite sai kuitenkin kannatusta, kun soai-reaktio löydettiin. Tämä on yksi osoitus siitä, miten tietyt isomeerit voivat suosia toista biologisissa prosesseissa. Vaikka ei ole näyttöä ubiquitous autocatlysis aiheuttaa homokiraalisuutta, se voi varmasti olla tekijä vahvistus joissakin tapauksissa.
toimintamalli
nykyään suosituin biologisen homokiraalisuuden teoria sisältää kaikki nämä johtopäätökset. Fysikaaliset ilmiöt, kuten polarisoitunut valo ja sähköheikkous, aiheuttavat D – ja L-isomeerien lievää epätasapainoa. Tämä pieni ristiriita monistetaan epätasaisemmaksi epätasapainoksi autokatalyysin avulla. Sitten, kun elämä oli muodostunut, ravintoketju ja entsyymien spesifisyys valitsivat nopeasti yhden isomeerin. Nykyään näemme siis vain L-aminohappoja ja D-sokereita.
tässä teoriassa on vielä joitakin aukkoja. Miljardeja vuosia sitten alkaneelle tapahtumalle ei ehkä koskaan löydy täydellistä selitystä. Mutta nyt meillä on ainakin mahdollinen ratkaisu biolgisen homokiraalisuuden mysteeriin.
”mysteeri luo ihmetystä, ja ihmeellisyys on ihmisen ymmärtämisen halun perusta.”— Neil Armstrong
/div>