Focalin XR – Pharmacology dexmethylphenidate hydrochloride
Clinical Pharmacology
mechanism of action
Dexmethylphenidate hydrochloride is a CNS stimulant. The mode of therapeutic action in ADHD is not known.
pharmacodynamics
Dexmethylphenidate is the more pharmacologically active d-enantiomer of racemic methylphenidate. Metyylifenidaatti estää noradrenaliinin ja dopamiinin takaisinoton presynaptiseen hermosoluun ja lisää näiden monoamiinien vapautumista ekstraneuronaaliseen tilaan.
sydämen Elektrofysiologia
suositellulla enimmäisvuorokausiannoksella 40 mg Focalin XR ei pidennä QTc-aikaa kliinisesti merkittävässä määrin.
farmakokinetiikka
imeytyminen
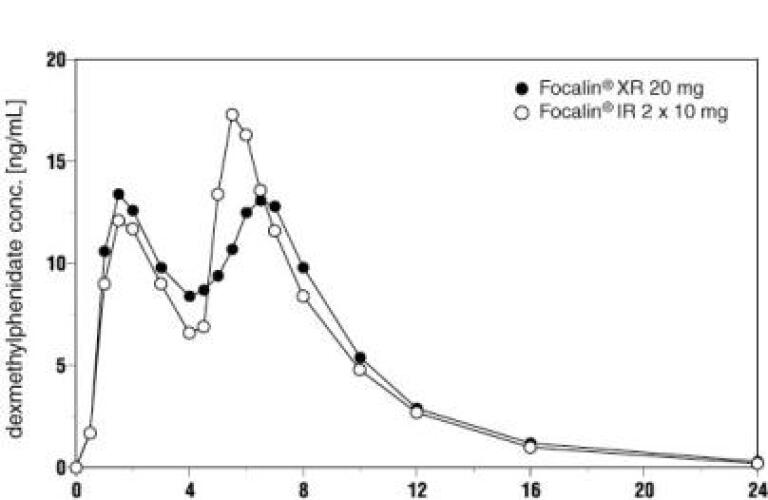
Focalin XR aiheuttaa kaksimodaalisen plasmapitoisuus-aikaprofiilin (ts.2 erillistä piikkiä noin 4 tunnin välein), kun sitä annetaan suun kautta terveille aikuisille. Focalin XR: n alkuperäinen imeytymisnopeus on sama kuin Focalin-tablettien, minkä osoittavat samanlaiset nopeusparametrit kahden eri lääkemuodon välillä, ts.ensimmäinen huippupitoisuus (Cmax1) ja aika ensimmäiseen huippupitoisuuteen (Tmax1), joka saavutetaan 1, 5 tunnissa (tyypillinen vaihteluväli 1-4 tuntia). Interpeak-minimin (tminip) keskimääräinen aika on hieman lyhyempi ja toisen huippupitoisuuden (tmax2) saavuttamiseen hieman pidempi, kun Focalin XR otetaan kerran vuorokaudessa (noin 6, 5 tuntia; vaihteluväli 4.5-7 tuntia) verrattuna Focalin-tabletteihin, jotka annetaan 2 annoksena 4 tunnin välein (KS.Kuva 1), joskin havaitut vaihteluvälit ovat suuremmat Focalin XR: llä.
Focalin XR-valmisteen toinen huippupitoisuus on pienempi (Cmax2), interpeakin vähimmäispitoisuudet ovat suuremmat (Cminip) ja huippupitoisuudet ja aallonpohjat vaihtelevat vähemmän kuin Focalin-tablettien 2 annosta 4 tunnin välein. Tämä johtuu siitä, että imeytyminen viivästyneesti vapautuvista helmistä alkaa aikaisemmin ja pitenee (KS.Kuva 1).
AUC: n(0-inf) ja Cmax: n geometrisen keskiarvon suhde kerran vuorokaudessa annetun Focalin XR: n annon jälkeen on 1, 02 ja 0, 86 samaan Focalin-tablettien kokonaisannokseen 2 annoksena 4 tunnin välein. Cmax -, Cmin-ja AUC-arvojen vaihtelu on samaa luokkaa Focalin XR-ja Focalin välittömästi vapautuvien tablettien välillä.
noin 90% annoksesta imeytyy radioaktiivisesti merkityn raseemisen metyylifenidaatin oraalisen annon jälkeen. Ensikierron metaboliasta johtuen deksmetyylifenidaatin keskimääräinen absoluuttinen hyötyosuus oli eri lääkemuodoissa annettuna 22-25%.
kerta-annoksen jälkeen Focalin XR: n farmakokinetiikka oli suhteessa annokseen välillä 5-40 mg.
potilaille, jotka eivät kykene nielemään kapselia, sisältö voidaan sirotella omenasoseeseen ja annostella .
jakautuminen
deksmetyylifenidaatin sitoutuminen plasman proteiineihin ei ole tiedossa; raseeminen metyylifenidaatti sitoutuu plasman proteiineihin 12-15% pitoisuudesta riippumatta. Deksmetyylifenidaatin jakautumistilavuus on 2, 65 ± 1, 11 L/kg.
eliminaatio
plasman Deksmetyylifenidaattipitoisuudet pienenevät monofaasisesti Focalin XR: n oraalisen annon jälkeen. Deksmetyylifenidaatin terminaalisen eliminaation puoliintumisajan keskiarvo terveillä aikuisilla oli noin 3 tuntia. Lapsipotilaiden puoliintumisaika on yleensä hieman lyhyempi 2-3 tuntia. Deksmetyylifenidaatti eliminoitui keskimääräisellä puhdistumalla 0, 40 ± 0.12 L/h/kg laskimonsisäisen annostelun jälkeen.
metabolia
ihmisillä deksmetyylifenidaatti metaboloituu pääasiassa de-esteröinnin kautta d-α-fenyylipiperidiinietikkahapoksi (tunnetaan myös nimellä d-ritaliinihappo). Tällä metaboliitilla on vain vähän tai ei lainkaan farmakologista vaikutusta. L-Treo-enantiomeerille ei ole in vivo-transkonversiota.
erittyminen
kun radioaktiivisesti merkittyä raseemista metyylifenidaattia annettiin ihmisille suun kautta, noin 90% radioaktiivisuudesta erittyi virtsaan. Raseemisen (d,l-) metyylifenidaatin päämetaboliitti virtsassa oli d,l-ritaliinihappo, joka vastasi noin 80% annoksesta. 0, 5% laskimoon annetusta annoksesta erittyi virtsaan.
tutkimukset erityisryhmissä
mies-ja naispotilaat
Focalin XR-hoidon jälkeen ensimmäinen huippupitoisuus (Cmax1) oli naisilla keskimäärin 45% korkeampi. Myös interpeakin minimi ja toinen huippu olivat naisilla hieman korkeampia, vaikka ero ei ollut tilastollisesti merkitsevä, ja nämä kuviot säilyivät vielä painon normalisoinnin jälkeenkin.
rodulliset tai etniset ryhmät
Focalin XR-valmisteen käytöstä ei ole riittävästi kokemusta farmakokinetiikan etnisten vaihtelujen havaitsemiseksi.
lapsipotilaat
Deksmetyylifenidaatin farmakokinetiikkaa Focalin XR-annoksen jälkeen ei ole tutkittu alle 18-vuotiailla pediatrisilla potilailla. Kun samanlainen raseemisen metyylifenidaatin koostumus tutkittiin 15: llä 10-12-vuotiaalla potilaalla ja 3: lla ADHD-potilaalla 7-9-vuotiaalla, ensimmäisen huippuajan aika oli samanlainen, vaikka aika piikin minimin ja toisen huippuajan välillä viivästyi ja vaihteli enemmän lapsipotilailla kuin aikuisilla. Kun sama annos annettiin lapsipotilaille ja aikuisille, lapsipotilaiden pitoisuudet olivat noin kaksinkertaiset aikuisilla todettuihin pitoisuuksiin verrattuna. Suurempi altistus johtuu lähes täysin kehon pienemmästä koosta, sillä deksmetyylifenidaatin farmakokineettisissä parametreissa (puhdistuma ja jakautumistilavuus) ei ole merkittäviä ikään liittyviä eroja annoksen ja painon normalisoitumisen jälkeen.
potilaat, joilla on munuaisten vajaatoiminta
kokemusta Focalin XR: n käytöstä munuaisten vajaatoimintaa sairastavilla potilailla ei ole. Koska munuaispuhdistuma ei ole tärkeä metyylifenidaatin eliminaatioreitti, munuaisten vajaatoiminnalla odotetaan olevan vain vähän vaikutusta Focalin XR: n farmakokinetiikkaan.
potilaat, joilla on maksan vajaatoiminta
kokemusta Focalin XR: n käytöstä maksan vajaatoimintaa sairastavilla potilailla ei ole.
Lääkeinteraktiotutkimukset
metyylifenidaatti ei metaboloidu sytokromi P450 (CYP) – isoentsyymien kautta kliinisesti merkittävässä määrin. Syps: n induktoreilla tai estäjillä ei odoteta olevan merkittävää vaikutusta metyylifenidaatin farmakokinetiikkaan. Sitä vastoin metyylifenidaatin d-ja l-enantiomeerit eivät estäneet relevantisti CYP1A2: ta, 2C8: aa, 2C9: ää, 2C19: ää, 2D6: ta, 2E1: tä tai 3a: ta. Kliinisesti metyylifenidaatin samanaikainen anto ei suurentanut CYP2D6-substraatin desipramiinin pitoisuuksia plasmassa.