8.3: Momento di dipolo magnetico orbitale dell’elettrone
Obiettivi formativi
Alla fine di questa sezione, sarete in grado di:
- Spiegare perché l’atomo di idrogeno ha proprietà magnetiche
- Spiegare perché i livelli di energia di un atomo di idrogeno associati con momento angolare orbitale, sono divisi da un campo magnetico esterno
- Utilizzare i numeri quantici per calcolare la grandezza e la direzione del raccordo anulare momento di dipolo magnetico di un atomo di idrogeno
Bohr il modello dell’atomo di idrogeno, l’elettrone si muove in un’orbita circolare intorno al protone. L’elettrone passa da un particolare punto sul ciclo in un certo tempo, quindi possiamo calcolare una corrente \(I = Q/t\). Un elettrone che orbita attorno a un protone in un atomo di idrogeno è quindi analogo alla corrente che scorre attraverso un filo circolare (Figura \ (\PageIndex{1}\)). Nello studio del magnetismo, abbiamo visto che un filo che trasporta corrente produce campi magnetici. È quindi ragionevole concludere che l’atomo di idrogeno produce un campo magnetico e interagisce con altri campi magnetici.
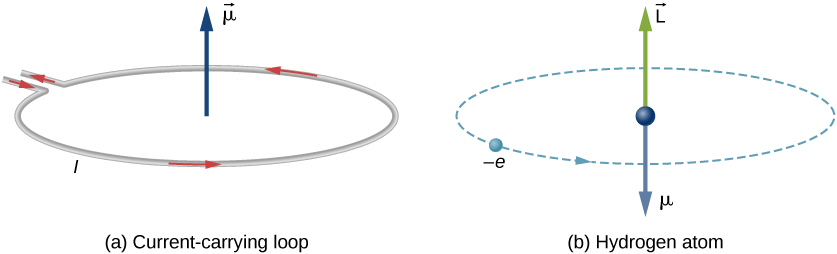
Il momento di dipolo magnetico orbitale è una misura della forza del campo magnetico prodotto dal momento angolare orbitale di un elettrone. Da Forza e Coppia su un ciclo di corrente, la grandezza del momento di dipolo magnetico orbitale per un ciclo di corrente è
\
dove \(I\) è la corrente e \(A\) è l’area del ciclo. (Per brevità, ci riferiamo a questo come il momento magnetico.) La corrente\ (I\) associata ad un elettrone in orbita attorno a un protone in un atomo di idrogeno è
\
dove e è la grandezza della carica dell’elettrone e \(T\) è il suo periodo orbitale. Se assumiamo che l’elettrone viaggi in un’orbita perfettamente circolare, il periodo orbitale è
\
dove r è il raggio dell’orbita e v è la velocità dell’elettrone nella sua orbita. Dato che l’area di un cerchio è \(\pi r^2\), il momento magnetico assoluto è
\
È utile esprimere il momento magnetico μμ in termini di momento angolare orbitale (\(\vec{L} = \vec{r} \times \vec{p}\)). Poiché l’elettrone orbita in un cerchio, il vettore di posizione \(\vec {r}\) e il vettore di momento \(\vec{p}\) formano un angolo retto. Quindi, la grandezza del momento angolare orbitale è
\
Combinando queste due equazioni, abbiamo
\
In forma vettoriale completa, questa espressione è scritta come
\
Il segno negativo appare perché l’elettrone ha una carica negativa. Si noti che la direzione del momento magnetico dell’elettrone è antiparallela al momento angolare orbitale, come mostrato in Figura \(\PageIndex{1b}\). Nel modello di Bohr dell’atomo, la relazione tra \(\vec{\mu}\) e \(\vec{L}\) nell’equazione \ref{BIG} è indipendente dal raggio dell’orbita.
Il momento magnetico \(μ\) può anche essere espresso in termini di numero quantico angolare orbitale \(l\). Combinando l’Equazione \ref{eq2} e l’Equazione \ref{eq1}, magnitudo di momento magnetico è
\
La componente z del momento magnetico è
\ &= – \left(\dfrac{e}{2m_e}\right) \, m \editormaniglie \\ &= – \mu_B m. \label{eq6} \end{align}\]
La quantità di \(\mu_B\) è un elemento fondamentale di magnetismo chiamato Bohr magneton, che ha il valore di \(9.3 \times 10^{-24} \, Joule/Tesla\) (J/T) o \(5.8 \times 10^{-5} eV/T\). La quantizzazione del momento magnetico è il risultato della quantizzazione del momento angolare orbitale.
Come vedremo nella prossima sezione, il momento di dipolo magnetico totale dell’atomo di idrogeno è dovuto sia al moto orbitale dell’elettrone che al suo spin intrinseco. Per ora, ignoriamo l’effetto dello spin degli elettroni.
Esempio \(\PageIndex{1}\): Momento di dipolo magnetico orbitale
Qual è la grandezza del momento magnetico dipolo orbitale μ di un elettrone nell’atomo di idrogeno nello stato (a) s, (b) p e (c) d? (Supponiamo che lo spin dell’elettrone sia zero.)
Strategia
Il momento magnetico dell’elettrone è correlato al suo momento angolare orbitale L. Per l’atomo di idrogeno, questa quantità è correlata al numero quantico angolare orbitale l. Gli stati sono dati in notazione spettroscopica, che mette in relazione una lettera (s, p, d, ecc.) ad un numero quantico.
Soluzione
La grandezza del momento magnetico è dato nell’Equazione \ref{eq5}:
\ &= \left(\dfrac{e}{2m_e}\right) \, \sqrt{l(l + 1)} \editormaniglie \nonumber \\ &= \mu_B\sqrt{l(l + 1)}. \end{align}\]
- Per lo stato s, \(l = 0\) quindi abbiamo \(\mu = 0\) e \(\mu_z = 0\).
- Per il p, \(l = 0\) e \ \ dove \(m = (-1, 0, 1)\) quindi, \
- Per la d stato, \(l = 2\) e otteniamo \ \ dove \(m = (-2, -1, 0, 1, 2)\) quindi, \
Significato
In s stato, non c’è momento angolare orbitale e quindi nessun momento magnetico. Ciò non significa che l’elettrone sia a riposo, solo che il movimento complessivo dell’elettrone non produce un campo magnetico. Nello stato p, l’elettrone ha un momento magnetico con tre possibili valori per la componente z di questo momento magnetico; ciò significa che il momento magnetico può puntare in tre diverse direzioni polari-ciascuna antiparallela al vettore del momento angolare orbitale. Nello stato d, l’elettrone ha un momento magnetico con cinque possibili valori per la componente z di questo momento magnetico. In questo caso, il momento magnetico può puntare in cinque diverse direzioni polari.
Un atomo di idrogeno ha un campo magnetico, quindi ci aspettiamo che l’atomo di idrogeno interagisca con un campo magnetico esterno, come il push e pull tra due magneti a barra. Da Forza e di Coppia su un Loop di Corrente, sappiamo che quando un loop di corrente interagisce con un campo magnetico esterno \(\vec{B}\), esperienze di una coppia data da
\
dove i è la corrente, \(\vec{A}\) è l’area del ciclo, \(\vec{\mu}\) è il momento magnetico, e \(\vec{B}\) è il campo magnetico esterno. Questa coppia agisce per ruotare il vettore momento magnetico dell’atomo di idrogeno per allinearsi con il campo magnetico esterno. Poiché il lavoro meccanico è svolto dal campo magnetico esterno sull’atomo di idrogeno, possiamo parlare di trasformazioni energetiche nell’atomo. Il potenziale di energia dell’atomo di idrogeno associati con questo l’interazione magnetica è dato dall’Equazione \ref{eq30}:
\
Se il momento magnetico è antiparallelo al campo magnetico esterno, l’energia potenziale è grande, ma se il momento magnetico è parallelo al campo, l’energia potenziale è di piccole dimensioni. Il lavoro svolto sull’atomo di idrogeno per ruotare il vettore del momento magnetico dell’atomo nella direzione del campo magnetico esterno è quindi associato a una caduta di energia potenziale. L’energia del sistema è conservata, tuttavia, perché un calo di energia potenziale produce radiazioni (l’emissione di un fotone). Queste transizioni di energia sono quantizzate perché il momento magnetico può puntare solo in determinate direzioni.
Se il campo magnetico esterno punti nella direzione z positiva, l’energia potenziale associata con l’orbitale magnetico di momento di dipolo è
\
dove \(\mu_B\) è il Bohr magneton e m è il momento angolare di proiezione numero quantico (o magnetico orbitale numero quantico), che ha i valori di
\
Per esempio, in \(l = 1\) di elettroni di stato, l’energia totale dell’elettrone è suddiviso in tre distinti livelli di energia corrispondente a \(U = -\mu_B B, 0, \mu_B B\).
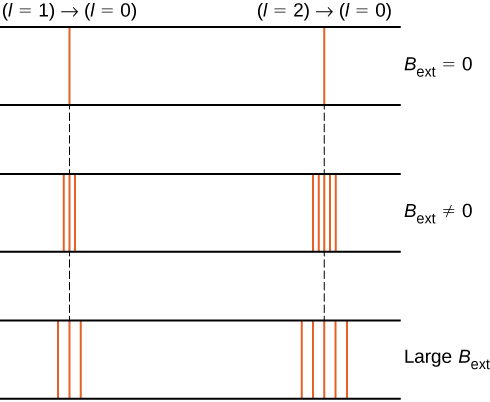
La divisione dei livelli di energia da un campo magnetico esterno è chiamata effetto Zeeman. Ignorando gli effetti dello spin degli elettroni, le transizioni dallo stato \(l = 1\) a uno stato di energia inferiore comune producono tre linee spettrali ravvicinate (Figura \ (\PageIndex{2}\), colonna di sinistra). Allo stesso modo, le transizioni dallo stato \(l = 2\) producono cinque linee spettrali ravvicinate (colonna di destra). La separazione di queste linee è proporzionale alla forza del campo magnetico esterno. Questo effetto ha molte applicazioni. Ad esempio, la divisione delle linee nello spettro dell’idrogeno del Sole viene utilizzata per determinare la forza del campo magnetico del Sole. Molte di queste misurazioni del campo magnetico possono essere utilizzate per creare una mappa dell’attività magnetica sulla superficie del Sole chiamata magnetogramma (Figura \(\PageIndex{3}\)).

Contributori e attribuzioni
Samuel J. Il film è stato prodotto da Ling (Truman State University), Jeff Sanny (Loyola Marymount University) e Bill Moebs con molti autori. Questo lavoro è concesso in licenza da OpenStax University Physics sotto una licenza Creative Commons Attribution (by 4.0).