biologische Homochiraliteit: Een van het Leven van de Grootste Mysteries

In elke levensvorm op Aarde, suikers zijn altijd rechtshandig, en de aminozuren zijn altijd linkshandig. Wat betekent dit en waarom gebeurt het? Dit bizarre fenomeen gaat om chirale moleculen en staat bekend als “homochiraliteit.”
chirale moleculen zijn moleculen met dezelfde formule, maar met iets verschillende structuren. Je hand is een chiraal object omdat het niet superponeerbaar is op zijn spiegelbeeld; wanneer je je linkerhand over je rechter plaatst, zullen je duimen in verschillende richtingen wijzen. In organische moleculen, wanneer vier verschillende groepen een centrale koolstof omringen, zal het molecuul twee verschillende chirale vormen hebben genoemd enantiomeren. Deze twee moleculen zijn spiegelbeelden van elkaar, omdat de groepen rond de koolstof in verschillende richtingen zijn georiënteerd, zoals de rechter-en linkerhand. In de chemie worden deze verbindingen R en S enantiomeren (of isomeren) genoemd. Echter, wanneer aminozuren of suikers chiral, wetenschappers noemen ze D en L isomeren (wetenschappers zijn verschrikkelijk in het benoemen van dingen consequent). D betekent ‘rechtshandig’ en L betekent ‘linkshandig’.”

The D-en l-isomeren zijn gewoonlijk aanwezig in een 50/50-verhouding. Chemici noemen dit een racemisch mengsel. Natuurlijk zou je verwachten dat ze allebei even aanwezig zijn in ons lichaam, toch? Fout! In feite gebruiken alle levensvormen alleen L-aminozuren en D-suikers. De aanwezigheid van slechts één isomeer wordt homochiraliteit genoemd. Van de kleinste bacteriën tot olifanten, alleen L-aminozuren vormen eiwitten en alleen d-suikers vormen polysachariden. Met andere woorden, alle eiwitten zijn rechtshandig en alle polysachariden zijn linkshandig*. Waarom is dit? Het is een mysterie dat biologen al jaren in de war brengt. Ondanks de inspanningen van natuurkundigen, scheikundigen en evolutionaire biologen, weten we het nog steeds niet zeker. Hier zullen we een kijkje nemen op enkele van de toonaangevende huidige theorieën.
*(opgemerkt moet worden dat sommige l-suikers ook via metabole routes kunnen worden afgebroken. Suikers kunnen ringen vormen, en de D-suiker vormt een stabielere ring dan de L-suiker, maar L-suikers kunnen nog steeds bestaan. De stabiliteit van de ring kan de belangrijkste bijdrage aan de prevalentie van D-suikers. Hieronder zullen we ons voornamelijk richten op aminozuren, die zich strikt houden aan een enkele chirale vorming in biologische systemen.)
Enzymen en Evolution

Dit is wat we wel weten: de enzymen in cellen kunnen slechts één isomeer metaboliseren, maar niet de andere. De enzymen katalyseren reacties om molecules af te breken en te bouwen door aan hen op zeer specifieke manieren te binden. Een enzym dat D-glucose afbreekt zal niet in staat zijn L-glucose af te breken. Als we beide isomeren willen gebruiken en bouwen, moeten we twee sets enzymen hebben. Dit vereist meer DNA, meer voedsel en veel meer energie. Natuurlijk willen cellen zo efficiënt mogelijk zijn, dus het hebben van een extra set enzymen zou belastend zijn.
maar als we die extra enzymen hadden, zouden we dan niet ook twee keer zoveel energie uit de omgeving kunnen halen? We zouden de andere 50% van de isomeren kunnen gebruiken als we de enzymen hadden om ze af te breken in plaats van ze te verspillen. Het antwoord heeft te maken met evolutie en de voedselpiramide.
wanneer het vroege leven evolueerde, zou een organisme enzymen hebben die selectief reageren met één isomeer. De organismen die deze eerste levensvorm aten zouden dezelfde selectieve enzymen moeten hebben om ze te verteren. Als al uw voedsel alleen d-suikers bevat, dan zult u dat ook! Dus als de bodem van de voedselketen alleen L-aminozuren gebruikt, zal homochiraliteit zich verspreiden naar elk organisme in de voedselketen! Omdat het leven eerst een stel enzymen moest ontwikkelen, kwamen we terecht bij die selectiviteit. Selectieve druk van de evolutie dwong elk nieuw organisme om dezelfde aminozuur – en suikersoorten te gebruiken als degene ervoor.
dus zodra een isomeer is gekozen, zal elke vorm van leven het gebruiken. Maar waarom L-aminozuren in plaats van D-aminozuren, en waarom d-suikers in plaats van L-suikers? Dit is het echte mysterie. Iets aan het begin van het leven moest het ene boven het andere kiezen. Het is mogelijk dat in de vroege stadia van het leven, sommige organismen ontwikkelden een set van enzymen, terwijl verschillende organismen de andere hadden. Het had een willekeurige gebeurtenis kunnen zijn die één lijn enzymen wegvaagde, maar wetenschappers zijn niet tevreden met dit antwoord. Er moet een reden zijn dat L-aminozuren en D-suikers beter zijn om te overleven dan hun tegenhangers.
Enter Physics
racemische mengsels zijn 50/50 mengsels van de twee isomeren. Maar er is reden om aan te nemen dat er in ons sterrenstelsel een lichte energievoorkeur is voor de ene isomeer boven de andere. Om deze voorkeur te begrijpen, moeten we diep in de Melkweg reizen.
ons sterrenstelsel heeft een chirale spin en een magnetische oriëntatie. Dit zorgt ervoor dat kosmisch stof licht in één richting circulair polariseert. Omdat licht een 2-dimensionale Golf is, zal het zich verspreiden in een helix. Het kosmische stof zorgt ervoor dat deze helix bij voorkeur in één richting draait.

Dit circulair gepolariseerd licht degradeert D-aminozuren meer dan L-aminozuren, zodat L-aminozuren stabieler zijn. Dit wordt ondersteund door studies van meteoren en kometen. Kosmische materie, althans in de Melkweg, heeft een voorkeur voor L-aminozuren vanwege de cirkelvormige polarisatie van licht.
een andere fysische verklaring voor de voorkeur van de ene isomeer boven de andere heeft te maken met de elektrozwakke kracht. Er zijn vier fundamentele krachten die de fysica regeren: zwaartekracht, elektromagnetisme, sterke nucleaire kracht, en de elektrozwakke kracht (ook bekend als zwakke Nucleaire kracht). De eerste drie zijn achiraal: ze beïnvloeden L – en D-isomeren op dezelfde manier. De elektrozwakke kracht wordt echter beïnvloed door chiraliteit. De elektrozwakke kracht regelt het radioactieve verval van atomen en moleculen. In dit verval wordt de pariteit van het universum niet altijd bewaard. Tijdens beta verval, geëmitteerde elektronen begunstigen een type spin. De spin van de elektronen degradeert opnieuw D-aminozuren meer dan L-aminozuren, veroorzakend het saldo van molecules om ten gunste van L-isomeer te verschuiven.
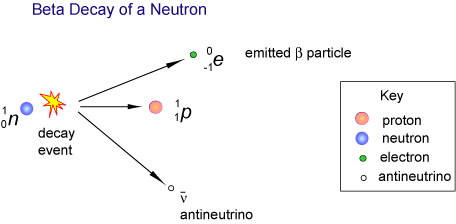
zowel gepolariseerd licht als elektrozwak verval dragen bij aan een lichte voorkeur van de ene isomeer boven de andere in ons melkwegstelsel. Echter, in het grote schema van de dingen, is deze discrepantie niet genoeg om te verklaren waarom elke levensvorm alleen d-suikers en L-aminozuren gebruikt. Er moet meer zijn. Dit leidt tot …
Autokatalyse
zodra de fysica een lichte rand geeft aan de ene isomeer over de andere, is er een chemische reden die het verschil versterkt. Autokatalyse betekent dat de aanwezigheid van een chemische stof zijn eigen productie stimuleert. Rond 1950 stelde F. C. Frank voor dat de dominante isomeren hun eigen productie kunnen activeren terwijl ze de productie van de andere isomeer onderdrukken.

bovenstaande grafiek illustreert het punt. Bij het beginnen met 3 L-isomeren en 2 D-isomeren, kan de verhouding zeer snel worden vergroot zodat de L-isomeren zeer overtreffen de D-isomeren. L-isomeer stimuleert zijn eigen productie, en L-isomeer bindt ook aan D-isomeer in een proces genoemd “wederzijds antagonisme.”Dit voorkomt de vorming van meer D-isomeren, en de L-isomeer is snel favoriet.
Dit was slechts een hypothetisch kader om te verklaren waarom we alleen L-aminozuren en D-suikers hebben. Maar dit concept kreeg steun toen de Soai-reactie werd ontdekt. Dit is één demonstratie van hoe bepaalde isomeren over een andere in biologische processen kunnen worden begunstigd. Hoewel er geen bewijs is voor alomtegenwoordige autocatlysis die homochiraliteit veroorzaakt, kan het zeker een factor voor versterking in sommige gevallen zijn.
een werkmodel
vandaag de dag bevat de meest populaire theorie voor biologische homochiraliteit al deze conclusies. Fysische verschijnselen zoals gepolariseerd licht en elektrozwakke kracht creëren een lichte onbalans van D-en L-isomeren. Deze kleine discrepantie wordt versterkt in een meer ongelijke onbalans door autokatalyse. Dan, zodra het leven werd gevormd, werd één enkele isomeer voor snel geselecteerd door de voedselketen en de specificiteit van enzymen. Zo zien we vandaag alleen L-aminozuren en D-suikers.
Deze theorie heeft nog enkele gaten. Er is misschien nooit een perfecte verklaring voor een gebeurtenis die miljarden jaren geleden begon. Maar we hebben nu tenminste een mogelijke oplossing voor het mysterie van de biolgische homochiraliteit.
“Mystery creates wonder, and wonder is the basis of man’ s desire to understand.”— Neil Armstrong