Concepts of Biology-1st Canadian Edition
virussen werden voor het eerst ontdekt na de ontwikkeling van een porseleinen filter, het Chamberland-Pasteur filter genaamd, dat alle bacteriën die onder de microscoop zichtbaar zijn uit een vloeibaar monster kon verwijderen. In 1886 toonde Adolph Meyer aan dat een ziekte van tabaksplanten, tobacco mosaic disease, kon worden overgedragen van een zieke plant naar een gezonde door middel van vloeibare plantenextracten. In 1892 toonde Dmitri Ivanowski aan dat deze ziekte op deze manier kon worden overgedragen, zelfs nadat het Chamberland-Pasteurfilter alle levensvatbare bacteriën uit het extract had verwijderd. Toch duurde het vele jaren voordat bewezen werd dat deze “filtreerbare” infectieuze agentia niet slechts zeer kleine bacteriën waren, maar een nieuw type van klein, ziekte veroorzakend deeltje.
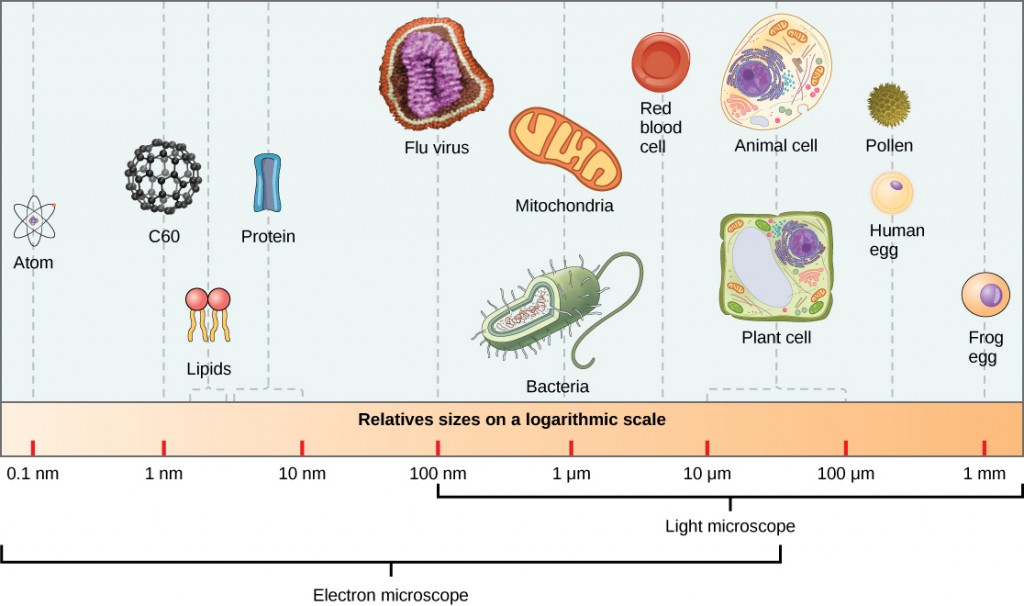
virionen, enkelvoudige virusdeeltjes, zijn zeer klein, ongeveer 20-250 nanometer (1 nanometer = 1/1.000. 000 mm). Deze individuele virusdeeltjes zijn de infectieuze vorm van een virus buiten de gastheercel. In tegenstelling tot bacteriën (die ongeveer 100 keer groter zijn), kunnen we geen virussen zien met een lichtmicroscoop, met uitzondering van enkele grote virionen van de poxvirus familie (figuur 12.3).
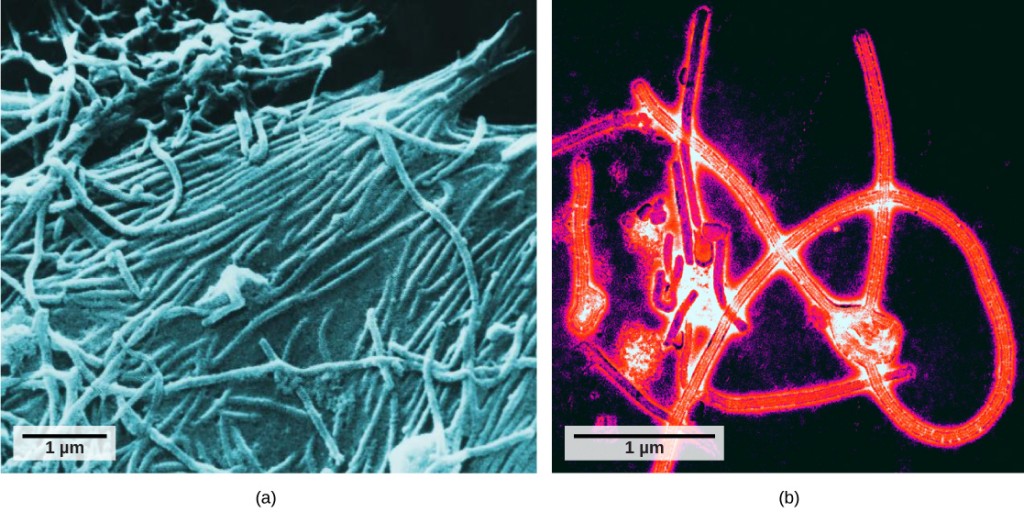
pas na de ontwikkeling van de elektronenmicroscoop in de jaren veertig kregen wetenschappers voor het eerst een goed beeld van de structuur van het tabaksmozaïekvirus (figuur 12.2) en anderen. De oppervlaktestructuur van virionen kan worden waargenomen door zowel scanning als transmissie-elektronenmicroscopie, terwijl de interne structuren van het virus alleen kunnen worden waargenomen in beelden van een transmissie-elektronenmicroscoop (figuur 12.4).
het gebruik van deze technologie heeft de ontdekking van vele virussen van alle soorten levende organismen mogelijk gemaakt. Ze werden aanvankelijk gegroepeerd door gedeelde morfologie, wat betekent dat hun grootte, vorm en onderscheidende structuren. Later, werden de groepen virussen geclassificeerd door het type van nucleic zuur zij bevatten, DNA of RNA, en of hun nucleic zuur enkel-of dubbel-strandde was. Recenter heeft de moleculaire analyse van virale replicatiecycli hun classificatie verder verfijnd.
een virion bestaat uit een nucleïnezuurkern, een buitenste eiwitcoating en soms een buitenste omhulsel gemaakt van eiwit-en fosfolipidemembranen afkomstig van de gastheercel. Het meest zichtbare verschil tussen leden van virale families is hun morfologie, die vrij divers is. Een interessant kenmerk van virale complexiteit is dat de complexiteit van de gastheer niet correleert met de complexiteit van het virion. Enkele van de meest complexe virion structuren worden waargenomen in bacteriofagen, virussen die de eenvoudigste levende organismen, bacteriën infecteren.
virussen zijn er in vele vormen en maten, maar deze zijn consistent en verschillend voor elke virale familie (figuur 12.5). Alle virionen hebben een nucleic-zuur genoom dat door een beschermende laag van proteã ne wordt behandeld, genoemd capside. De capside wordt gemaakt van eiwit subeenheden genoemd capsomeren. Sommige virale kapsels zijn eenvoudige veelvlakken “bollen”, terwijl andere vrij complex van structuur zijn. De buitenste structuur die de capside van sommige virussen omringt wordt genoemd de virale envelop. Alle virussen gebruiken een soort glycoproteïne om zich aan hun gastheercellen te hechten bij moleculen op de cel die virale receptoren worden genoemd. Het virus exploiteert deze cel-oppervlakte moleculen, die de cel gebruikt voor een ander doel, als een manier om specifieke celtypes te herkennen en te infecteren. Bijvoorbeeld, gebruikt het mazelenvirus een cel-oppervlakte glycoproteïne in mensen die normaal in immune reacties en mogelijk in de sperma-ei interactie bij bevruchting functioneert. De gehechtheid is een vereiste voor virussen om later het celmembraan te doordringen, het virale genoom in te spuiten, en hun replicatie binnen de cel te voltooien.
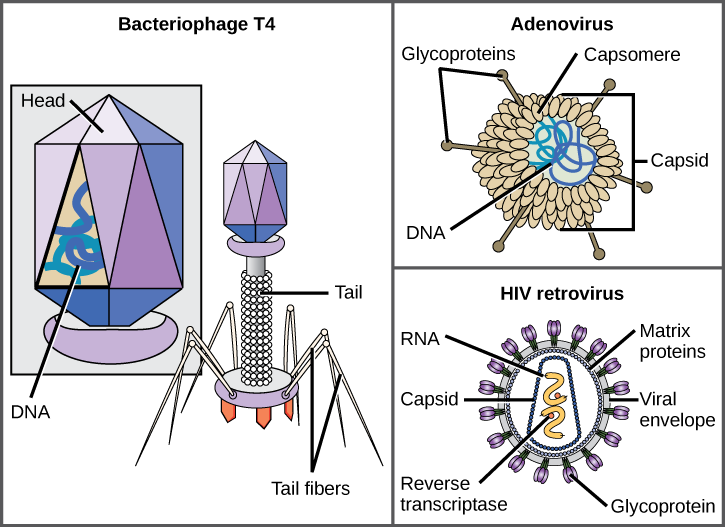
de T4-bacteriofaag, die de E. coli-bacterie infecteert, behoort tot het meest complexe virion dat bekend is; T4 heeft een eiwitstaartstructuur die het virus gebruikt om zich aan de gastheercel te hechten en een kopstructuur die zijn DNA herbergt.
Adenovirus, een niet-ontwikkeld diervirus dat aandoeningen aan de luchtwegen bij mensen veroorzaakt, gebruikt eiwitpieken die uit zijn capsomeren steken om zich aan de gastheercel te hechten. Niet-ontwikkelde virussen omvatten ook die polio (poliovirus), plantaire wratten (papillomavirus), en hepatitis A (hepatitis A virus) veroorzaken. De niet ontwikkelde virussen neigen om robuuster te zijn en waarschijnlijker om onder ruwe voorwaarden, zoals de darm te overleven.
omhulde virionen zoals HIV( humaan immunodeficiëntievirus), de veroorzaker van AIDS (verworven immunodeficiëntiesyndroom), bestaan uit nucleïnezuur (RNA in het geval van HIV) en capside-eiwitten omgeven door een fosfolipide bilaag envelop en de bijbehorende eiwitten (figuur 12.5). Waterpokken, influenza en bof zijn voorbeelden van ziekten veroorzaakt door virussen met enveloppen. Wegens de kwetsbaarheid van de envelop, zijn de niet ontwikkelde virussen beter bestand tegen veranderingen in temperatuur, pH, en sommige desinfectantia dan omhulde virussen.
over het algemeen vertelt de vorm van het virion en de aanwezigheid of afwezigheid van een omhulsel weinig over welke ziekten de virussen kunnen veroorzaken of welke soorten ze kunnen infecteren, maar het is nog steeds een nuttig middel om te beginnen met virale classificatie.
welke van de volgende beweringen over virusstructuur is waar?
A) alle virussen zijn ingekapseld in een viraal membraan.
B) de capsomere bestaat uit kleine eiwitsubeenheden die capsiden worden genoemd.
C) DNA is het genetische materiaal in alle virussen.
D) glycoproteïnen helpen het virus zich aan de gastheercel te hechten.
<!–D – >
In tegenstelling tot alle levende organismen die DNA als hun genetisch materiaal gebruiken, kunnen virussen DNA of RNA als hun genetisch materiaal gebruiken. De viruskern bevat het genoom of de totale genetische inhoud van het virus. De virale genomen neigen om klein te zijn in vergelijking met bacteriën of eukaryotes, die slechts die genen bevatten die voor proteã nen coderen het virus niet van de gastheercel kan krijgen. Dit genetisch materiaal kan single-stranded of double-stranded zijn. Het kan ook lineair of cirkelvormig zijn. Terwijl de meeste virussen één enkel segment van nucleic zuur bevatten, hebben anderen genomen die uit verscheidene segmenten bestaan.
DNA-virussen hebben een DNA-kern. Het virale DNA leidt de replicatieproteã nen van de gastheercel om nieuwe exemplaren van het virale genoom samen te stellen en om dat genoom in virale proteã nen te transcriberen en te vertalen. De virussen van DNA veroorzaken menselijke ziekten zoals waterpokken, hepatitis B, en sommige geslachtsziekten zoals herpes en genitale wratten.
RNA-virussen bevatten alleen RNA in hun kern. Om hun genomen in de gastheercel te herhalen, coderen de genomen van de virussen van RNA enzymen die niet in gastheercellen worden gevonden. De polymerase enzymen van RNA zijn niet zo stabiel zoals polymerases van DNA en maken vaak fouten tijdens transcriptie. Om deze reden, komen de veranderingen, veranderingen in de nucleotideopeenvolging, in virussen van RNA vaker voor dan in virussen van DNA. Dit leidt tot snellere evolutie en verandering in de virussen van RNA. Bijvoorbeeld, het feit dat influenza een RNA-virus is, is een van de redenen dat elk jaar een nieuw griepvaccin nodig is. Menselijke ziekten veroorzaakt door RNA virussen omvatten hepatitis C, mazelen, en hondsdolheid.
virussen kunnen worden gezien als verplichte intracellulaire parasieten. Het virus moet zich aan een levende cel hechten, naar binnen worden genomen, zijn eiwitten produceren en zijn genoom kopiëren, en een manier vinden om uit de cel te ontsnappen zodat het virus andere cellen en uiteindelijk andere individuen kan infecteren. Virussen kunnen slechts bepaalde soorten gastheren en slechts bepaalde cellen binnen die gastheer infecteren. De moleculaire basis voor deze specificiteit is dat een bepaalde oppervlaktemolecule, bekend als de virale receptor, op de oppervlakte van de gastheercel moet worden gevonden om het virus te binden. Ook, zijn de metabolische verschillen die in verschillende celtypes worden gezien die op differentiële genuitdrukking worden gebaseerd een waarschijnlijke factor waarin cellen een virus kan gebruiken om zich te herhalen. De cel moet de stoffen maken die het virus nodig heeft, zoals enzymen waarvoor het virusgenoom zelf geen genen heeft, anders kan het virus zich niet vermenigvuldigen met die cel.
stappen van virusinfecties
een virus moet een cel “overnemen” om zich te vermenigvuldigen. De virale replicatiecyclus kan dramatische biochemische en structurele veranderingen in de gastheercel veroorzaken, die celschade kunnen veroorzaken. Deze veranderingen, genoemd cytopathische gevolgen, kunnen celfuncties veranderen of zelfs de cel vernietigen. Sommige geïnfecteerde cellen, zoals die met het verkoudheidsvirus (rhinovirus), sterven door lysis (barsten) of apoptose (geprogrammeerde celdood of “celzelfmoord”), waardoor alle nieuwe virionen in één keer vrijkomen. De symptomen van virale ziekten zijn het gevolg van de immuunrespons op het virus, dat probeert het virus uit het lichaam te controleren en te elimineren, en van celschade veroorzaakt door het virus. Veel dierlijke virussen, zoals HIV (humaan immunodeficiëntievirus), verlaten de geïnfecteerde cellen van het immuunsysteem door een proces dat bekend staat als ontluikende, waarbij virionen individueel de cel verlaten. Tijdens het ontluikingsproces ondergaat de cel geen lysis en wordt deze niet onmiddellijk gedood. Echter, de schade aan de cellen die HIV infecteert kan het onmogelijk maken voor de cellen om te functioneren als bemiddelaars van immuniteit, hoewel de cellen blijven leven voor een periode van tijd. De meeste productieve virale infecties volgen vergelijkbare stappen in de virusreplicatie cyclus: bevestiging, penetratie, uncoating, replicatie, assemblage en release.
een virus hecht zich aan een specifieke receptorplaats op het gastheercelmembraan door aanhechtingseiwitten in de capside of in zijn omhulsel ingebedde eiwitten. De gehechtheid is specifiek, en typisch zal een virus zich slechts aan cellen van één of enkele species en slechts bepaalde celtypes binnen die species met de geschikte receptoren hechten.
Concept in Actie

bekijk deze video voor een visuele uitleg van hoe HIV en influenza het lichaam aanvallen.
In tegenstelling tot dierlijke virussen wordt het nucleïnezuur van bacteriofagen naakt in de gastheercel geïnjecteerd, waarbij de capside buiten de cel blijft. De plantaardige en dierlijke virussen kunnen hun cellen door endocytose ingaan, waarin het celmembraan omringt en het volledige virus overspoelt. Sommige omhulde virussen gaan de cel in wanneer de virale envelop direct met het celmembraan smelt. Eenmaal binnen de cel, wordt de virale capside gedegradeerd en wordt het virale nucleic zuur vrijgegeven, dat dan Beschikbaar voor replicatie en transcriptie wordt.
het replicatiemechanisme is afhankelijk van het virale genoom. De virussen van DNA gebruiken gewoonlijk de proteã nen en enzymen van de gastheercel om extra DNA te maken dat aan exemplaar het genoom wordt gebruikt of aan boodschappersRNA (mRNA) wordt getranscribeerd, dat dan in eiwitsynthese wordt gebruikt. De virussen van RNA, zoals het griepvirus, gebruiken gewoonlijk de kern van RNA als malplaatje voor synthese van viraal genomic RNA en mRNA. Het virale mRNA wordt vertaald in virale enzymen en capside proteã nen om nieuwe virionen te assembleren (figuur 12.6). Natuurlijk zijn er uitzonderingen op dit patroon. Als een gastheercel niet de enzymen verstrekt die nodig zijn voor virale replicatie, leveren de virale genen de informatie aan directe synthese van de ontbrekende proteã nen. Retroviruses, zoals HIV, hebben een genoom van RNA dat omgekeerd moet worden getranscribeerd om DNA te maken, dat dan in DNA van de gastheer wordt ingevoegd. Om RNA in DNA om te zetten, bevatten retroviruses genen die het virus-specifieke enzym reverse transcriptase coderen dat een RNA-malplaatje aan DNA transcribeert. Het feit dat HIV enkele van zijn eigen enzymen produceert, die niet in de gastheer worden gevonden, heeft onderzoekers toegestaan om geneesmiddelen te ontwikkelen die deze enzymen remmen. Deze geneesmiddelen, met inbegrip van de reverse transcriptase inhibitor AZT, remmen HIV-replicatie door de activiteit van het enzym te verminderen zonder het metabolisme van de gastheer te beïnvloeden.
het laatste stadium van virusreplicatie is het vrijkomen van de nieuwe virionen in het gastorganisme, waar zij aangrenzende cellen kunnen infecteren en de replicatiecyclus kunnen herhalen. Sommige virussen worden vrijgegeven wanneer de gastheercel sterft en andere virussen kunnen besmette cellen verlaten door te ontluiken door het membraan zonder de cel direct te doden.
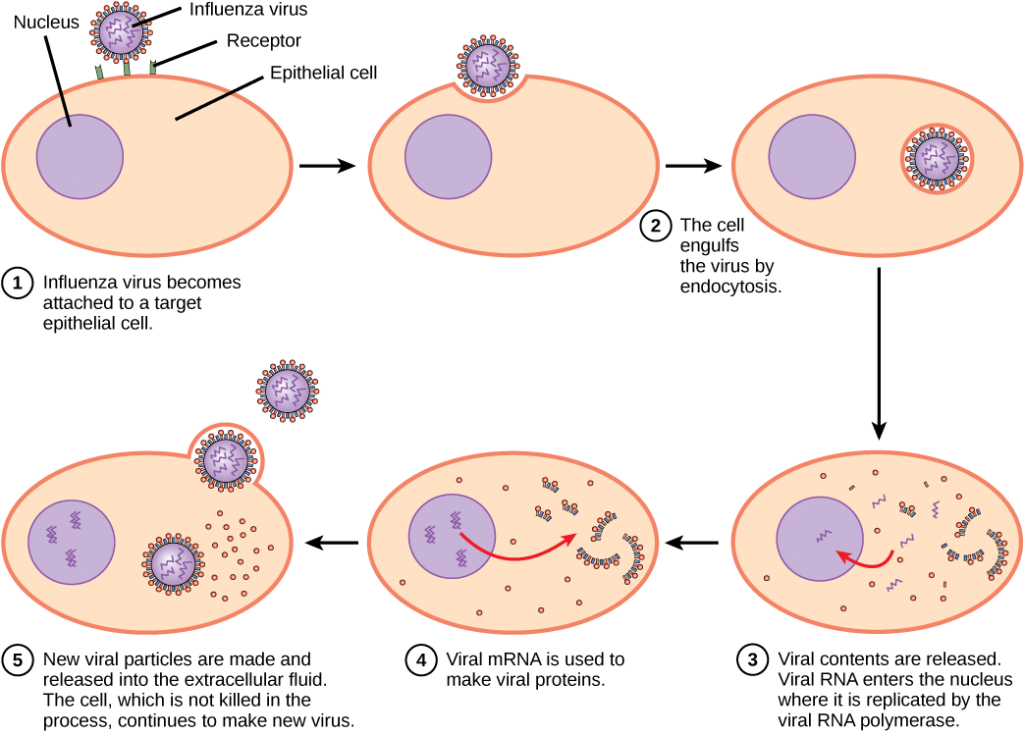
het influenzavirus is verpakt in een virale envelop, die smelt met het plasmamembraan. Op deze manier kan het virus de gastcel verlaten zonder het te doden. Welk voordeel heeft het virus te winnen door de gastheercel in leven te houden?
<!- De gastcel kan nieuwe virusdeeltjes blijven aanmaken.–>
Concept in Actie

klik door deze handleiding over virussen om structuren, wijzen van transmissie, replicatie en meer te identificeren.