Wat is radiobiologie-Stralingsbiologie-definitie
Stralingsbiologie (ook bekend als radiobiologie) is een medische wetenschap die de studie van de biologische effecten van ioniserende straling op levende weefsels omvat. Straling is overal om ons heen. In, rond en boven de wereld waarin we leven. Het is een natuurlijke energiekracht die ons omringt. Het is een deel van onze natuurlijke wereld die hier al is sinds de geboorte van onze planeet. Of de bron van de straling is natuurlijk of door de mens gemaakt,of het nu een grote dosis straling of een kleine dosis, zal er een aantal biologische effecten. In het algemeen is ioniserende straling schadelijk en potentieel dodelijk voor levende wezens, maar kan gezondheidsvoordelen hebben in de geneeskunde, bijvoorbeeld bij radiotherapie voor de behandeling van kanker en thyreotoxicose. In dit hoofdstuk worden de gevolgen van blootstelling aan straling op korte en lange termijn kort samengevat.
cellulaire schade-radiobiologie
alle effecten van biologische schade beginnen met het gevolg van stralingsinteracties met de atomen die de cellen vormen. Alle levende dingen zijn samengesteld uit één of meer cellen. Elk deel van je lichaam bestaat uit cellen of is door hen gebouwd. Hoewel we de neiging hebben om te denken van biologische effecten in termen van het effect van straling op levende cellen, in werkelijkheid, ioniserende straling, per definitie, interageert alleen met atomen door een proces genaamd ionisatie. Voor ioniserende straling, de kinetische energie van deeltjes (fotonen, elektronen, enz.) van ioniserende straling is voldoende en het deeltje kan ioniseren (om ion te vormen door elektronen te verliezen) doelatomen om ionen te vormen. Alleen ioniserende straling kan elektronen uit een atoom slaan.
Er zijn twee mechanismen waardoor straling uiteindelijk cellen beïnvloedt. Deze twee mechanismen worden gewoonlijk genoemd:
- directe effecten. De directe gevolgen worden veroorzaakt door straling, wanneer de straling rechtstreeks met de atomen van het molecuul van DNA, of een andere cellulaire component van kritiek aan de overleving van de cel interageert. De kans dat de straling interageert met het DNA-molecuul is zeer klein omdat deze kritische componenten zo ‘ n klein deel van de cel uitmaken.
- indirecte effecten. Indirecte effecten worden veroorzaakt door interactie van straling meestal met watermoleculen. Elke cel, net als het geval is voor het menselijk lichaam, is meestal water. Ioniserende straling kan breken de bindingen die het water molecuul bij elkaar te houden, het produceren van radicalen zoals hydroxyl OH, superoxide anion O2–en anderen. Deze radicalen kunnen bijdragen aan de vernietiging van de cel.
een groot aantal cellen van een bepaald type wordt een weefsel genoemd. Als dit weefsel een gespecialiseerde functionele eenheid vormt, wordt het een orgaan genoemd. Het type en het aantal cellen dat wordt beïnvloed is ook een belangrijke factor. Sommige cellen en organen in het lichaam zijn gevoeliger voor ioniserende straling dan andere.
gevoeligheid van verschillende soorten cellen voor ioniserende straling is zeer hoog voor weefsels die bestaan uit cellen die zich snel delen, zoals die in beenmerg, Maag, Darmen, mannelijke en vrouwelijke voortplantingsorganen en foetussen in ontwikkeling. Dit is omdat het verdelen van cellen correcte DNA-informatie vereist om de nakomelingen van de cel te overleven. Een directe interactie van straling met een actieve cel kan resulteren in de dood of mutatie van de cel, terwijl een directe interactie met het DNA van een slapende cel minder effect zou hebben.
hierdoor kunnen levende cellen worden geclassificeerd op basis van hun voortplantingssnelheid, wat ook hun relatieve gevoeligheid voor straling aangeeft. Als gevolg daarvan zijn actief reproducerende cellen gevoeliger voor ioniserende straling dan cellen die huid -, nier-of leverweefsel vormen. De zenuw – en spiercellen regenereren het langst en zijn de minst gevoelige cellen.
 de gevoeligheid van de verschillende organen van het menselijk lichaam correleert met de relatieve gevoeligheid van de cellen waaruit zij zijn samengesteld. In de praktijk wordt deze gevoeligheid weergegeven door de weefselweegfactor wT, die de factor is waarmee de equivalente dosis in een weefsel of orgaan T wordt gewogen om de relatieve bijdrage van dat weefsel of orgaan aan de totale schade voor de gezondheid als gevolg van uniforme bestraling van het lichaam weer te geven (ICRP 1991b).
de gevoeligheid van de verschillende organen van het menselijk lichaam correleert met de relatieve gevoeligheid van de cellen waaruit zij zijn samengesteld. In de praktijk wordt deze gevoeligheid weergegeven door de weefselweegfactor wT, die de factor is waarmee de equivalente dosis in een weefsel of orgaan T wordt gewogen om de relatieve bijdrage van dat weefsel of orgaan aan de totale schade voor de gezondheid als gevolg van uniforme bestraling van het lichaam weer te geven (ICRP 1991b).
indien een persoon slechts gedeeltelijk wordt bestraald, is de dosis sterk afhankelijk van het weefsel dat werd bestraald. Bijvoorbeeld, een gammadosis van 10 mSv voor het hele lichaam en een dosis van 50 MSV voor de schildklier is, in termen van risico, hetzelfde als een dosis van 10 + 0,04 x 50 = 12 mSv voor het hele lichaam.
High-LET and Low-LET Radiation
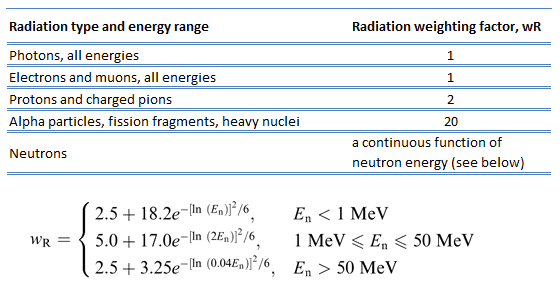
zoals geschreven, interageert elk type straling op een andere manier met materie. Bijvoorbeeld geladen deeltjes met hoge energieën kunnen atomen direct ioniseren. Alfadeeltjes zijn vrij massief en dragen een dubbele positieve lading, dus ze hebben de neiging om slechts een korte afstand te reizen en dringen niet erg ver in het weefsel of helemaal niet. Maar alfadeeltjes zullen hun energie over een kleiner volume (mogelijk slechts een paar cellen als ze in een lichaam) en veroorzaken meer schade aan die paar cellen.
bètadeeltjes (elektronen) zijn veel kleiner dan alfadeeltjes. Ze dragen een enkele negatieve lading. Ze zijn indringender dan alfadeeltjes. Ze kunnen meerdere meters reizen, maar op elk punt op hun pad minder energie deponeren dan alfadeeltjes. Dit betekent dat bètadeeltjes de neiging hebben om meer cellen te beschadigen, maar met minder schade aan elk. Aan de andere kant interageert elektrisch neutrale deeltjes slechts indirect, maar kunnen ook een deel of al hun energieën naar de materie overbrengen.
Het zou de zaken zeker vereenvoudigen indien de biologische effecten van straling recht evenredig zouden zijn met de geabsorbeerde dosis. Helaas hangen biologische effecten ook af van de manier waarop de geabsorbeerde dosis wordt verdeeld langs de weg van de straling. Studies hebben aangetoond dat alfa-en neutronenstraling grotere biologische schade veroorzaken voor een bepaalde energiedepositie per kg weefsel dan gammastraling. Het werd ontdekt, biologische effecten van elke straling neemt toe met de lineaire energieoverdracht (LET). Kortom, de biologische schade van hoge-LETSTRALING (alfadeeltjes, protonen of neutronen) is veel groter dan die van lage-LETSTRALING (gammastraling). Dit komt omdat het levende weefsel gemakkelijker schade van straling kan herstellen die over een groot gebied wordt verspreid dan die welke in een klein gebied wordt geconcentreerd. Natuurlijk, bij zeer hoge niveaus van blootstelling gammastraling kan nog steeds veel schade aan weefsels veroorzaken.
omdat meer biologische schade wordt veroorzaakt bij dezelfde fysische dosis (d.w.z. dezelfde energie die wordt afgezet per massa-eenheid weefsel), is één grijs alfa-of neutronenstraling schadelijker dan één grijs gammastraling. Dit feit dat straling van verschillende typen (en energieën) verschillende biologische effecten geeft voor dezelfde geabsorbeerde dosis wordt beschreven in termen van factoren die bekend staan als de relatieve biologische effectiviteit (RBE) en de stralingsweegfactor (WR).
Acute dosis en chronische dosis
biologische effecten van straling en de gevolgen daarvan hangen sterk af van het niveau van het verkregen dosistempo. In de radiobiologie is het dosistempo een maat voor de intensiteit (of sterkte) van de stralingsdosis. Lage doses zijn gebruikelijk voor het dagelijks leven. In de volgende punten zijn er enkele voorbeelden van blootstelling aan straling, die uit verschillende bronnen kan worden verkregen.
- 05 µSv – Slapen naast iemand
- 09 µSv – Woonachtig binnen 30 km van een kerncentrale voor een jaar
- 1 µSv – het Eten van een banaan
- 3 µSv – Woonachtig binnen een straal van 50 km van een kolencentrale voor een jaar
- 10 µSv – Gemiddelde dagelijkse dosis ontvangen van natuurlijke achtergrond
- 20 µSv – röntgenfoto van de Borst
Van biologische gevolgen oogpunt, is het zeer belangrijk om onderscheid te maken tussen de doses ontvangen over korte en langere periodes. Daarom zijn de biologische effecten van straling meestal verdeeld in twee categorieën.
- Acute Doses. Een” acute dosis ” (kortdurende hoge dosis) is een dosis die optreedt over een korte en eindige periode, d.w.z. binnen een dag.
- chronische Doses. Een “chronische dosis” (lage dosis op lange termijn) is een dosis die gedurende een langere periode, d.w.z. weken en maanden, wordt voortgezet, zodat het beter door een dosistempo wordt beschreven.
hoge doses hebben de neiging cellen te doden, terwijl lage doses de neiging hebben cellen te beschadigen of te veranderen. Hoge doses kunnen visueel dramatische stralingsbrandwonden veroorzaken, en/of een snel sterftecijfer door acuut stralingssyndroom. Acute doses lager dan 250 mGy hebben waarschijnlijk geen waarneembare effecten. Acute doses van ongeveer 3 tot 5 Gy hebben een 50% kans op het doden van een persoon enkele weken na de blootstelling, als een persoon geen medische behandeling krijgt.
lage doses verspreid over lange tijd veroorzaken geen onmiddellijk probleem voor enig orgaan. De effecten van lage stralingsdoses treden op op het niveau van de cel en de resultaten kunnen gedurende vele jaren niet worden waargenomen. Bovendien tonen sommige studies aan dat de meeste menselijke weefsels een meer uitgesproken tolerantie vertonen voor de effecten van lage-LETSTRALING bij een langdurige blootstelling in vergelijking met een eenmalige blootstelling aan een vergelijkbare dosis.
deterministische en stochastische Effecten
in de radiobiologie worden de meeste nadelige gezondheidseffecten van blootstelling aan straling gewoonlijk onderverdeeld in twee grote klassen:
- deterministische effecten zijn drempeleffecten op de gezondheid, die direct verband houden met de geabsorbeerde stralingsdosis en de ernst van het effect neemt toe naarmate de dosis toeneemt.
- stochastische effecten treden bij toeval op, meestal zonder een drempelwaarde voor de dosis. De kans op het optreden van stochastische effecten is evenredig met de dosis, maar de ernst van het effect is onafhankelijk van de ontvangen dosis.deterministische Effecten
deterministische Effecten
in de radiobiologie zijn deterministische effecten (of niet-stochastische gezondheidseffecten) gezondheidseffecten, die direct verband houden met de geabsorbeerde stralingsdosis en de ernst van het effect neemt toe naarmate de dosis toeneemt. Deterministische effecten hebben een drempelwaarde waaronder geen detecteerbare klinische effecten optreden. De drempel kan zeer laag zijn (in de Orde van grootte van 0,1 Gy of hoger) en kan van persoon tot persoon verschillen. Voor doses tussen 0,25 Gy en 0,5 Gy kunnen lichte bloedveranderingen worden gedetecteerd door medische evaluaties en voor doses tussen 0,5 Gy en 1,5 Gy zullen bloedveranderingen worden opgemerkt en symptomen van misselijkheid, vermoeidheid, braken optreden.
zodra de drempelwaarde is overschreden, neemt de ernst van een effect toe met de dosis. De reden voor de aanwezigheid van deze drempeldosis is dat stralingsschade (ernstig defect of overlijden) van een kritische celpopulatie (hoge doses hebben de neiging cellen te doden) in een bepaald weefsel moet worden opgelopen voordat het letsel in een klinisch relevante vorm wordt uitgedrukt. Daarom worden deterministische effecten ook weefselreactie genoemd. Ze worden ook niet-stochastische effecten genoemd om te contrasteren met toeval-achtige stochastische effecten (bijvoorbeeld kankerinductie).
deterministische effecten zijn niet noodzakelijk meer of minder ernstig dan stochastische effecten. Hoge doses kunnen visueel dramatische stralingsbrandwonden veroorzaken, en/of een snel sterftecijfer door acuut stralingssyndroom. Acute doses lager dan 250 mGy hebben waarschijnlijk geen waarneembare effecten. Acute doses van ongeveer 3 tot 5 Gy hebben een 50% kans op het doden van een persoon enkele weken na de blootstelling, als een persoon geen medische behandeling krijgt. Deterministische effecten kunnen uiteindelijk leiden tot een tijdelijke overlast of ook tot een fatale afloop. Voorbeelden van deterministische effecten:
voorbeelden van deterministische effecten zijn::
- acuut stralingssyndroom, door acute straling van het hele lichaam
- Stralingsbrandwonden, van straling naar een bepaald lichaamsoppervlak
- stralingsgeïnduceerde thyroïditis, een mogelijke bijwerking van bestralingsbehandeling tegen hyperthyreoïdie
- chronisch stralingssyndroom, van langdurige straling.
- Stralingsgeïnduceerd longletsel, van bijvoorbeeld bestralingstherapie naar de longen
letale stralingsdoses
de letale stralingsdosis (LD) is een indicatie van de letale hoeveelheid straling. In stralingsbescherming, de mediane letale dosis, wordt LDXY meestal gebruikt. De stralingsdosis die naar verwachting binnen 30 dagen de dood van 50% van de bestraalde personen zal veroorzaken, is bijvoorbeeld LD50/30. LD1 is de dosis die naar verwachting de dood zal veroorzaken bij 1% van de doorstraalde personen, bijgevolg is LD99 dodelijk voor alle (99%) doorstraalde personen. Het is ook erg belangrijk, of iemand een medische behandeling krijgt of niet. Hoe groter een acute stralingsdosis is, des te groter is de kans dat het individu wordt gedood. Voor een gezonde volwassene, de LD50 wordt geschat op ergens tussen de 3 en 5 Gy.
- 2,5 Sv-dosis die een mens doodt met een risico van 1% (LD1), indien de dosis gedurende een zeer korte periode wordt toegediend.
- 5 Sv-dosis die een mens doodt met een risico van 50% binnen 30 dagen (LD50/30), indien de dosis gedurende een zeer korte periode wordt toegediend. Doodsoorzaak is verlies van beenmergfunctie.
- 8 Sv-dosis die een mens doodt met een risico van 99% (LD99), indien de dosis gedurende een zeer korte periode wordt toegediend. Bij ongeveer 10 Gy, acute ontsteking van de longen kan optreden en leiden tot de dood.
de letale dosisgegevens hierboven zijn van toepassing op acute gammadoses die in een zeer korte tijd, bijvoorbeeld enkele minuten, worden toegediend. Er is meer dosis nodig om de hierboven genoemde effecten te veroorzaken, als de dosis gedurende een periode van uren of langer wordt toegediend.
stochastische Effecten
in de radiobiologie komen stochastische effecten van ioniserende straling bij toeval voor, meestal zonder drempelwaarde voor de dosis. De kans op het optreden van stochastische effecten is evenredig met de dosis, maar de ernst van het effect is onafhankelijk van de ontvangen dosis. De biologische effecten van straling op mensen kunnen worden gegroepeerd in somatische en erfelijke effecten. Somatische effecten zijn die van de blootgestelde persoon. Erfelijke effecten zijn die van de nakomelingen van de blootgestelde persoon. Kanker risico wordt meestal genoemd als de belangrijkste stochastische effect van ioniserende straling, maar ook erfelijke aandoeningen zijn stochastische effecten.
volgens de ICRP:
(83) op basis van deze berekeningen stelt de Commissie nominale waarschijnlijkheidscoëfficiënten voor schadegecorrigeerd kankerrisico voor als 5,5 x 10-2 Sv-1 voor de gehele populatie en 4.1 x 10-2 Sv – 1 voor volwassen werknemers. Voor erfelijke effecten wordt het voor schade gecorrigeerde nominale risico voor de gehele bevolking geschat op 0,2 x 10-2 Sv-1 en voor volwassen werknemers op 0,1 x 10-2 Sv-1 .
speciale referentie: ICRP, 2007. De aanbevelingen van 2007 van de Internationale Commissie voor Stralingsbescherming. ICRP-publicatie 103. Anne. ICRP 37 (2-4).
de SI-eenheid voor effectieve dosis, de sievert, vertegenwoordigt het gelijkwaardige biologische effect van de afzetting van een joule gammastraling-energie in een kilogram menselijk weefsel. Een sievert staat dus voor een 5.5% kans op kanker. Merk op dat de effectieve dosis niet bedoeld is als maat voor deterministische gezondheidseffecten, dat is de ernst van acute weefselschade die zeker zal gebeuren, die wordt gemeten door de geabsorbeerde dosis.
Er zijn drie algemene categorieën stochastische effecten als gevolg van blootstelling aan lage stralingsdoses. Dit zijn:
- genetische effecten. Het genetische effect wordt geleden door de nakomelingen van het blootgestelde individu. Het gaat om de mutatie van zeer specifieke cellen, namelijk het sperma of de eicellen. Straling is een voorbeeld van een fysisch mutageen agens. Merk op dat er ook veel chemische en biologische agentia (zoals virussen) zijn die mutaties veroorzaken. Een belangrijk feit om te onthouden is dat straling het spontane mutatiepercentage verhoogt, maar geen nieuwe mutaties veroorzaakt.
- somatische effecten. Somatische effecten zijn die van de blootgestelde persoon. Het meest voorkomende effect van bestraling is de stochastische inductie van kanker met een latente periode van jaren of decennia na blootstelling. Aangezien kanker het primaire resultaat is, wordt het soms het carcinogene effect genoemd. Straling is een voorbeeld van een fysische kankerverwekkende, terwijl sigaretten zijn een voorbeeld van een chemische kanker veroorzakende agent. Virussen zijn voorbeelden van biologische carcinogene agentia.
- In-Utero effecten omvatten de productie van misvormingen bij zich ontwikkelende embryo ‘ s. Dit is echter eigenlijk een speciaal geval van het somatische effect, aangezien het embryo/de foetus degene is die aan de straling wordt blootgesteld.
somatische effecten ten gevolge van blootstelling aan straling worden door de meeste mensen als stochastisch beschouwd. Het meest algemeen aanvaarde model stelt dat de incidentie van kanker als gevolg van ioniserende straling lineair toeneemt met een effectieve stralingsdosis van 5,5% per sievert. Dit model staat bekend als het linear no-threshold model (LNT). Dit model gaat ervan uit dat er geen drempelpunt is en dat het risico lineair toeneemt met een dosis. Als dit lineaire model correct is, dan is natuurlijke achtergrondstraling de meest gevaarlijke bron van straling voor de Algemene volksgezondheid, gevolgd door medische beeldvorming als een nauwe tweede. De LNT wordt niet algemeen aanvaard, aangezien sommigen een adaptieve dosis-respons relatie voorstellen waar lage doses beschermend zijn en hoge doses schadelijk zijn. Er zij op gewezen dat een aantal organisaties het niet eens is met het gebruik van het lineaire no-threshold-model om de risico ‘ s van blootstelling aan straling op laag niveau in het milieu en op het werk te schatten.
radiobiologie en dosislimieten
bij stralingsbescherming worden dosislimieten ingesteld om de stochastische effecten tot een aanvaardbaar niveau te beperken en deterministische effecten volledig te voorkomen. Merk op dat, stochastische effecten zijn die voortvloeien uit toeval: hoe hoger de dosis, hoe waarschijnlijker het effect is. Deterministische effecten zijn die welke normaal een drempelwaarde hebben: daarboven neemt de ernst van het effect toe met de dosis. Dosislimieten zijn een fundamenteel onderdeel van stralingsbescherming, en het overschrijden van deze limieten is in de meeste landen tegen stralingsregulering. Merk op dat de in dit artikel beschreven dosislimieten van toepassing zijn op routineoperaties. Ze zijn niet van toepassing op een noodsituatie waarin het menselijk leven in gevaar wordt gebracht. Zij zijn niet van toepassing in noodsituaties waarbij een individu een catastrofale situatie probeert te voorkomen.
de grenswaarden zijn verdeeld in twee groepen, de bevolking en de werknemers die beroepsmatig aan blootstelling zijn blootgesteld. Volgens de ICRP heeft beroepsmatige blootstelling betrekking op alle blootstelling van werknemers tijdens hun werk, met uitzondering van
- uitgesloten blootstellingen en blootstellingen uit vrijgestelde activiteiten waarbij straling of vrijgestelde bronnen betrokken zijn
- elke medische blootstelling
- de normale lokale natuurlijke achtergrondstraling.
de volgende tabel geeft een samenvatting van de dosislimieten voor werknemers die beroepsmatig aan blootstelling zijn blootgesteld en voor het publiek:
bron van gegevens: ICRP, 2007. De aanbevelingen van 2007 van de Internationale Commissie voor Stralingsbescherming. ICRP-publicatie 103. Anne. ICRP 37 (2-4).
volgens de aanbeveling van de ICRP in zijn verklaring over weefselreacties van 21. In April 2011 werd de equivalente dosislimiet voor de ooglens voor beroepsmatige blootstelling in geplande blootstellingssituaties verlaagd van 150 mSv/jaar tot 20 mSv/jaar, gemiddeld over gedefinieerde perioden van 5 jaar, waarbij geen jaarlijkse dosis in één jaar meer dan 50 mSv bedroeg.
limieten voor de effectieve dosis zijn voor de som van de relevante effectieve doses uit uitwendige blootstelling in de gespecificeerde periode en de vastgelegde effectieve dosis uit opnamen van radionucliden in dezelfde periode. Voor volwassenen wordt de vastgelegde effectieve dosis berekend voor een periode van 50 jaar na inname, terwijl voor kinderen wordt berekend voor de periode tot de leeftijd van 70 jaar. De effectieve dosislimiet voor het hele lichaam van 20 mSv is een gemiddelde waarde over vijf jaar. De werkelijke limiet is 100 mSv in 5 jaar, met niet meer dan 50 mSv in een jaar.