Dove sono finite tutte le impalcature vascolari?
INTRODUZIONE
La vascolarizzazione arteriosa infrainguinale rappresenta un sottoinsieme impegnativo per il trattamento endovascolare a causa di forze complesse sulle arterie che si verificano con il movimento degli arti inferiori. Torsione arteriosa, flessione, estensione e compressione sono esempi di queste forze, che possono portare alla frattura dello stent e tassi di restenosi più elevati dopo il trattamento.1 Mentre il bypass vascolare del condotto venoso dei segmenti femoropopliteo (FP) rimane un’opzione praticabile con circa il 75% di pervietà a 5 anni, viene spesso utilizzato solo dopo che un approccio endovascolare ha fallito. Se un condotto venoso non è disponibile, gli innesti bioprotetici devono essere utilizzati con una pervietà di 5 anni molto più bassa (meno del 50%).2
Studi multipli hanno mostrato una pervietà superiore con stent rispetto all’angioplastica transluminale percutanea (PTA) da sola nel trattamento dei segmenti FP.1,3,4 Questo beneficio è in qualche modo mitigato dalla maggiore complessità del trattamento quando questi stent falliscono. L’introduzione della tecnologia DES (Drug eluting stent) ha ulteriormente migliorato la pervietà dello stent primario; tuttavia, il loro uso è stato mitigato da recenti avvertimenti della Food and Drug Administration (FDA) che associano i dispositivi a una maggiore mortalità.5 Queste preoccupazioni sono state sollevate dopo la pubblicazione di una meta-analisi di studi randomizzati controllati su dispositivi rivestiti con paclitaxel che hanno mostrato un aumento della mortalità a partire da 2 anni. Mentre più studi successivi, inclusa un’ampia analisi di >16.000 pazienti Medicare, non sono riusciti a confermare questo associato, l’uso dei dispositivi è temporaneamente rallentato.6-9
Ciò lascia un grande ruolo potenziale alle nuove tecnologie quali gli scaffold vascolari bioassorbibili (BVS) che possono fornire la pervietà iniziale migliorata mentre attenuano i problemi a valle quale la restenosi in-stent. In questa recensione, discuteremo i vari trattamenti disponibili della malattia arteriosa periferica infrainguinale e valuteremo il futuro degli stent/scaffold vascolari sia nei vasi femoropoplitei che sotto il ginocchio.
STENTING PER LA MALATTIA FEMOROPOPLITEA
Stent in metallo nudo
Mentre l’attuale pratica vascolare endovascolare favorisce il tentativo di evitare il posizionamento dello stent come trattamento di prima linea a causa di problemi sopra descritti, rimangono importanti indicazioni per lo stenting, come la stenosi residua dopo PTA e la dissezione limitante il flusso.1 I ” Criteri di utilizzo appropriati “combinati ACC/AHA/SCAI/SIR/SVM affermano che nei pazienti in terapia medica ottimale, lo stenting endovascolare della malattia stenotica FP è appropriato per la claudicazione e l’ischemia critica degli arti (Figure 1a-c).10
Figura 1a. Criteri di utilizzo appropriati per la claudicazione intermittente nonostante la terapia medica orientata alle linee guida.
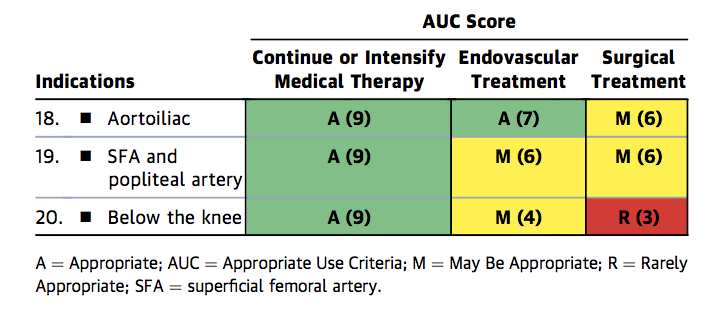
Figura 1a

Figura 1b. Appropriate Use Criteria for Critical Limb Ischemia
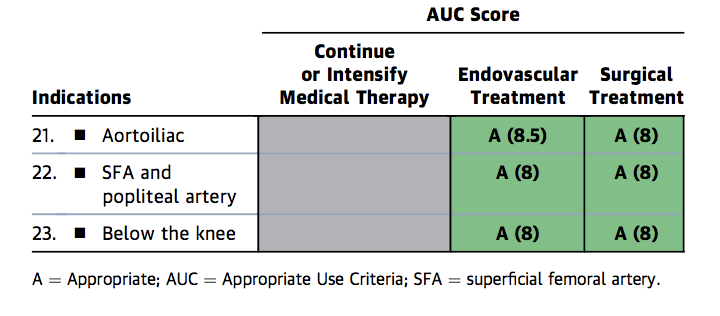
Figure 1b

Figure 1c. Appropriate Use Criteria Device Selection for FP disease
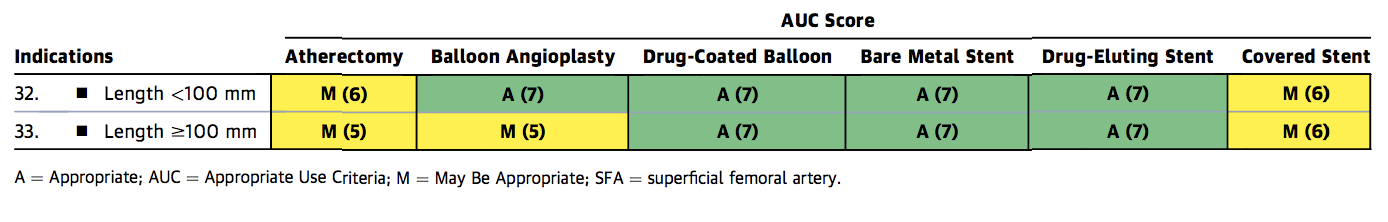
Figure 1c

FP = Femoropoplitea, A= Appropriato, AUC = Criteri di utilizzo appropriati, M = Può essere appropriato, R = Raramente appropriato, SFA = Arteria femorale superficiale.
FP = Femoropoplitea, A= Appropriato, AUC = Criteri di utilizzo appropriati, M = Può essere appropriato, R = Raramente appropriato, SFA = Arteria femorale superficiale.
La Society for Cardiovascular Angiography and Guidelines categorizza gli stent in metallo nudo come IIA e DES come raccomandazione IA per la malattia FP.11 La society of vascular surgery guidelines12, 13 on critical limb ischemia (CLI) raccomanda contro l’uso di stent sotto il ginocchio (BTK).
Il primo studio importante che ha confrontato lo stent vascolare con il solo PTA è stato condotto da Schillinger et al nel 2006.3 Nell’analisi “come trattato”, la pervietà primaria a 12 mesi era marcatamente più alta con stent di metallo nudo (63% vs. 37% p=0.001). Questo è stato seguito dallo studio di controllo randomizzato resiliente che ha confrontato lo stenting bare metal con Lifestent® a PTA. Lo studio ha mostrato nuovamente una pervietà primaria migliorata a 3 anni (75,5% vs. 41,1% p< 0,001).4
Il successivo registro SUPERB ha valutato lo stent di nitinol tessuto Supera, dimostrando una pervietà primaria dell ‘ 86,3% e zero fratture dello stent.14 I dati di follow-up a più lungo termine hanno mostrato una sopravvivenza libera da rivascolarizzazione della lesione target a 36 mesi dell ‘ 82%.1 In seguito al rilascio dello stent Supera, diverse aziende hanno introdotto stent nitinol bare metal che presentavano anche un basso tasso di frattura dello stent e una buona pervietà primaria. Ad esempio, lo stent Full® self expanding (Medtronic, Minneapolis, MN) ha mostrato una pervietà primaria di 1 anno di quasi il 75% e zero fratture di stent nei segmenti femoropopliteo (nota: le lesioni poplitee distali sono state escluse).15
Stent di eluizione del farmaco
La tecnologia di eluizione del farmaco è stata un importante progresso nel trattamento endovascolare della malattia arteriosa periferica. Lo stent eluente Zilver® paclitaxel (Cook Medical, Bloomington, IN) è stato studiato testa a testa rispetto allo stent PTA ottimale e allo stent bare metal secondo necessità. Lo studio ha mostrato che lo Zilver ® DES aveva una pervietà primaria superiore a 5 anni (66,4% contro 43,4% p <0,001). Questo studio è stato seguito dal processo IMPERIALE che ha esaminato Eluvia™ DES (Boston Scientific, Marlborough, MA) rispetto a Zilver®.16 Eluvia™ ha soddisfatto i criteri di non inferiorità prespecificati a 1 anno con un 88,5% rispetto al 79,5%, p per la non inferiorità < 0,01. Eluvia™ ha anche avuto un’incidenza numericamente inferiore di eventi avversi maggiori 4,9% contro 9,0%, p = 0,098.17
NUOVI DISPOSITIVI
Un’ampia gamma di dispositivi è in fase di sviluppo e alcuni sono sottoposti a prove in fase iniziale per soddisfare le restanti esigenze sul campo. Di seguito descriviamo alcuni esempi di importazione di tecnologie nuove o in evoluzione.
Scaffold vascolari bioassorbibili
Le scaffold vascolari bioassorbibili di dissoluzione (BVS) sono state inizialmente introdotte nelle arterie coronarie. L’eccitazione iniziale che circonda questi dispositivi è stata mitigata con la pubblicazione degli studi randomizzati ABSORB, che hanno confrontato l’ABSORB BVS (Abbott Vascular, Chicago, IL) con il DES coronarico standard (Figura 2a).18-20
Figura 2a. ASSORBIRE Bioabsorbable Stent (per gentile Concessione Abbott Vascular)

Figura 2a

Una meta-analisi di ASSORBIRE con 3,389 i pazienti hanno mostrato un dispositivo correlato trombosi del 2,3% per il BVS versus 0% per il DES a 3 anni [HR 3.79 IC 95% 1.72-8.36, p = 0.002).21
Nonostante le preoccupazioni relative alla prima generazione BVS nelle coronarie, BVS nella periferia sembra essere guadagnando slancio con la recente presentazione del singolo braccio ASSORBIRE BTK studio pilota 5 anni risultati. Lo studio è stato presentato all’incontro Vascular InterVentional Advance (VIVA) 201922 e ha riportato i risultati di 55 arti trattati con BVS dimostrando un tasso di guarigione completa della ferita del 90%. C’era un tasso di amputazione dello 0% e una pervietà primaria della nave di 5 anni che si avvicinava al 75%. Due prove imminenti si prevede di aggiungere ulteriormente al campo: lo studio randomizzato LIFE-BTK che valuterà Esprit BVS (Abbott Vascular) versus PTA da solo e lo studio Credence BTK-1 che è uno studio pilota a braccio singolo del dispositivo Credence BTK (Meril, Gujarat, India).
Sistema di virata vascolare
Il sistema endovascolare di virata (InTack Vascular, Wayne, PA) sono piccoli impianti di nitinol lunghi 6 mm che vengono utilizzati per riapplicare i lembi di dissezione prevenendo la propagazione e la perdita di lumen (Figura 2b).
Figura 2b. Tack Endovascolare di Sistema (per gentile concessione di Virata Vascolare)
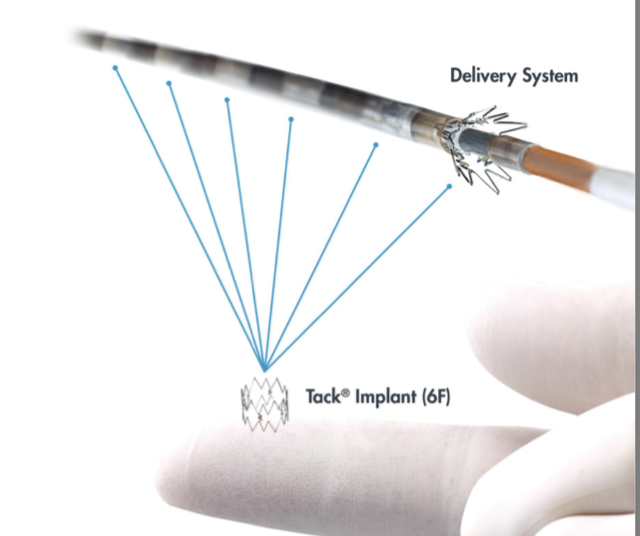
Figura 2b

Questi dispositivi sono stati valutati in recente pubblicazione, a singolo braccio, TOBA II studio, che ha valutato 213 pazienti che hanno ricevuto trattamenti con Chiodini dopo PTA. Lo studio ha mostrato un tasso di pervietà primaria di 1 anno 79,3% con 92,1% di lesioni con risoluzione completa della dissezione vascolare.23 Lo studio multicentrico a braccio singolo TOBA III ha esaminato le puntine nelle lesioni lunghe abbinate al trattamento definitivo con palloncini rivestiti di farmaci è stato recentemente riportato alla Transcatheter Cardiovascular Therapeutics Conference (TCT) in 2019. Lo studio ha mostrato una pervietà primaria del 95% a 12 mesi. Inoltre, lo studio TOBA II BTK, che ha esaminato il dispositivo nei vasi tibiali, è stato presentato a Vascular InterVentional Advances (VIVA) 2019. La presentazione ha riportato un tasso di guarigione delle ferite a 6 mesi del 73,8% e una pervietà della lesione target dell ‘ 87,3%.
BioMimics 3D Swirling Flow Stent
Lo stent 3D swirling flow (Veryan Medical) è uno stent elicoidale che opera sulla base dell’ipotesi che lo stress da taglio a bassa parete creato da stent dritti standard possa aumentare il rischio di restenosi vascolare. Modelli animali che valutano lo stent a flusso vorticoso hanno mostrato una significativa riduzione dello spessore neointimale (p <0,001). Lo studio IMITA 2 che esamina il dispositivo è in fase di completamento e dovrebbe essere presentato nel prossimo futuro. I risultati preliminari (con il 10% dei pazienti che necessitano ancora di follow-up finale) hanno mostrato una libertà di 2 anni dalla rivascolarizzazione della lesione target dell ‘ 84%.24
ChampioNIR®
Lo stent ChampioNIR® (Medinol Vascolare, Tel Aviv, Israele, Figura 2c) è uno stent ibrido autoespandibile composto da telaio radiale nitinol con una rete di fibre polimeriche longitudinali per consentire una flessibilità “infinita” e una maggiore resistenza alla fatica. Il dispositivo sta attualmente iscrivendosi al suo primo studio sull’uomo con un follow-up di 3 anni previsto.
2c. ChampioNIR® (Per Gentile Concessione Medinol Vascolare)

Figura 2c

CONCLUSIONE
Stent vascolari e ponteggi hanno un ruolo essenziale nel trattamento endovascolare algoritmo di malattia arteriosa periferica. I nuovi dispositivi in tecnologie sia durevoli che bioassorbibili hanno dimostrato promesse significative e molti sono attivamente studiati in studi clinici. Mentre le tecnologie bioassorbibili nelle coronarie hanno avuto esiti clinici peggiori, l’iterazione del dispositivo e le prove nel sistema vascolare periferico consentiranno l’opportunità di una continua crescita tecnologica.
- Garcia LA, Rosenfield KR, Metzger CD, et al. SUPERB risultati finali di 3 anni utilizzando stent nitinol biomimetic supera intrecciato. Catetere Cardiovasc Interv 2017;89: 1259-67.
- AbuRahma AF. Quando sono i trattamenti endovascolari e di bypass aperto preferiti per la malattia occlusiva femoropoplitea? Ann Vasc Dis 2018;11:25-40.
- Schillinger M, Sabeti S, Loewe C, et al. Angioplastica con palloncino contro impianto di stent nitinol nell’arteria femorale superficiale. N Engl J Med 2006;354: 1879-88.
- Laird JR, Katzen BT, Scheinert D, et al. Impianto di stent Nitinol vs. angioplastica con palloncino per lesioni nelle arterie poplitee femorali e prossimali superficiali di pazienti con claudicatio: follow – up di tre anni dallo studio randomizzato RESILIENTE. J Endovasc Ther 2012;19: 1-9.
- Katsanos K, Spiliopoulos S, Kitrou P, Krokidis M, Karnabatidis D. Rischio di morte in seguito all’applicazione di palloncini e stent rivestiti di paclitaxel nell’arteria femoropoplitea della gamba: una revisione sistematica e meta-analisi di studi randomizzati controllati. J Am Cuore Assoc 2018;7: e011245.
- Schneider PA, Laird JR, Doros G, et al. Mortalità non correlata con l’esposizione a paclitaxel: una meta-analisi indipendente a livello di paziente di un palloncino rivestito con farmaco. J Am Coll Cardiol 2019;73: 2550-63.
- Ouriel K, Adelman MA, Rosenfield K, et al. Sicurezza dell’angioplastica con palloncino rivestito con paclitaxel per la malattia dell’arteria periferica femoropoplitea. JACC Cardiovasc Interv 2019;12:2515-24.
- Gray WA, Jaff MR, Parikh SA, et al. Valutazione della mortalità dei palloni rivestiti con paclitaxel: meta-analisi a livello di paziente del programma clinico ILLUMENATE a 3 anni. Circolazione 2019;140: 1145-55.
- Secemsky EA, Kundi H, Weinberg I, et al. Associazione di sopravvivenza con rivascolarizzazione dell’arteria femoropoplitea con dispositivi rivestiti con farmaci. JAMA Cardiol 2019;4: 332-40.
- Bailey SR, Beckman JA, Dao TD, et al. ACC/AHA/SCAI / SIR / SVM 2018 Criteri di utilizzo appropriati per l’intervento dell’arteria periferica. J Am Coll Cardiol 2019;73: 214-37.
- Feldman DN, Armstrong EJ, Aronow HD, et al. SCAI consensus guidelines for device selection in femore-popliteal arterial interventions. Catetere Cardiovasc Interv 2018;92: 124-40.
- Lawrence PF, Gloviczki P. Linee guida vascolari globali per i pazienti con ischemia cronica pericolosa per gli arti. J Vasc Surg 2019; 69: 1S-2S.
- Conte MS, Bradbury AW, Kolh P, et al. Linee guida vascolari globali sulla gestione dell’ischemia cronica pericolosa per gli arti. Eur J Vasc Endovasc Surg 2019;58:S1-109.
- Garcia L, Jaff MR, Metzger C, et al. Risultato dello stent di nitinol intrecciato a filo nelle arterie poplitee femorali e prossimali superficiali: risultati di dodici mesi del SUPERB trial. Circ Cardiovasc Interv 2015; 8: e000937.
- Laird JR, Jain A, Zeller T, et al. Impianto di stent di Nitinol nell’arteria femorale superficiale e nell’arteria poplitea prossimale: risultati di dodici mesi dallo studio multicentrico SE completo. J Endovasc Ther 2014;21: 202-12.
- Dake MD, Ansel GM, Lottes AE. Zilver PTX RCT mortality analysis: nessuna differenza nel tasso di mortalità a lungo termine per lo stent a rilascio di farmaci Zilver PTX rispetto al PTA/BMS. CVIR Endovasc 2019;2:25.
- Gray WA, Keirse K, Soga Y, et al. Uno stent polimerico rivestito con paclitaxel (Eluvia) contro uno stent polimerico rivestito con paclitaxel (Zilver PTX) per intervento femoropopliteo endovascolare (IMPERIAL): uno studio randomizzato di non inferiorità. Lancetta 2018; 392: 1541-51.
- Pietra GW, Ellis SG, Gori T, et al. Risultati in cieco e angina valutazione degli scaffold coronarici bioresorbibili: risultati di 30 giorni e 1 anno dallo studio randomizzato ABSORB IV. Lancetta 2018; 392: 1530-40.
- Ali ZA, Serruys PW, Kimura T, et al. risultati a 2 anni con lo scaffold bioresorbibile Absorb per il trattamento della malattia coronarica: una revisione sistematica e meta-analisi di sette studi randomizzati con un substudy dei dati di un singolo paziente. Lancetta 2017; 390:760-72.
- Pietra GW, Ellis S, Simonton C, et al. Risultati dello scaffold vascolare bioresorbibile Absorb in arterie coronarie molto piccole e non molto piccole: lo studio randomizzato ABSORB III. J Am Coll Cardiol 2016;67:35.
- Ali ZA, Gao R, Kimura T, et al. Risultati triennali con lo scaffold bioresorbibile Absorb: meta-analisi dei dati individuali del paziente dagli studi randomizzati ABSORB. Circolazione 2018;137: 474-79.
- Presentati i risultati quinquennali dello studio ABSORB BTK (Endovascular Today website). 2019. Disponibile all’indirizzo: https://evtoday.com/news/five-year-results-from-absorb-btk-trial-presented . Accesso 02/25/20.
- Gray WA, Cardenas JA, Brodmann M, et al. Trattamento della dissezione post-angioplastica nelle arterie femoropoplitee utilizzando il sistema endovascolare Tack: risultati a 12 mesi dallo studio TOBA II. JACC Cardiovasc Interv 2019;12:2375-84.
- Swirling Flow®: l’alternativa ideale della natura all’eluizione dei farmaci (sito web Endovascolare Today). 2019. Available at: https://evtoday.com/articles/2019-sept/swirling-flow-natures-ideal-alternative-to-drug-elution. Accessed 02/25/20.
Clinical Topics: Invasive Cardiovascular Angiography and Intervention, Stable Ischemic Heart Disease, Vascular Medicine, Atherosclerotic Disease (CAD/PAD), Interventions and Vascular Medicine, Chronic Angina
Keywords: Malattie vascolari, Aneurisma, Arteriopatia periferica, Claudicatio intermittente, Stent medicamentosi, Costrizione, Patologica, Paclitaxel, Arteria femorale, United States Food and Drug Administration, Vasi coronarici, Medicare, Incidenza, Progetti pilota, Restenosi coronarica, Studi di follow-Up
< Torna agli elenchi