Mihin Verisuonitelineet ovat kadonneet?
INTRODUCTION
infrainguinal arterial verisuonitus on haastava osa endovaskulaarista hoitoa, koska valtimoihin kohdistuu monimutkaisia voimia, joita esiintyy alaraajaliikkeissä. Arteriaalinen vääntö, taipuma, laajennus ja puristus ovat esimerkkejä näistä voimista, jotka voivat johtaa stenttimurtumaan ja korkeampiin restenoosilukuihin hoidon jälkeen.1 vaikka femoropopliteal (FP) – segmenttien laskimojohdin on edelleen toteuttamiskelpoinen vaihtoehto noin 75%: n avoimuudella 5 vuoden kohdalla, sitä käytetään usein vasta, kun endovaskulaarinen lähestymistapa on epäonnistunut. Jos laskimokanavaa ei ole saatavilla, bioprosteettisia siirteitä on käytettävä paljon pienemmällä 5 vuoden avoimuudella (Alle 50%).2
useissa tutkimuksissa on todettu stenttien parempi avoimuus PALLOLAAJENNUSTEN hoidossa pelkkään pallolaajennukseen verrattuna.1,3,4 tätä hyötyä lieventää jonkin verran hoidon monimutkaistuminen, kun nämä stentit epäonnistuvat. Drug eluting stent (DES) – tekniikan käyttöönotto on edelleen parantanut primaarista stentti-avoimuutta; niiden käyttöä on kuitenkin lievennetty viimeaikaisilla elintarvike-ja lääkeviraston (FDA) varoituksilla, jotka yhdistävät laitteet korkeampaan kuolleisuuteen.5 nämä huolenaiheet tulivat esiin sen jälkeen, kun paklitakselilla päällystetyillä laitteilla tehdyistä satunnaistetuista kontrolloiduista tutkimuksista tehty meta-analyysi osoitti kuolleisuuden lisääntyneen 2 vuoden kohdalla. Vaikka useat myöhemmät tutkimukset, mukaan lukien laaja analyysi >16 000 Medicare-potilasta, eivät pystyneet vahvistamaan tätä yhteyttä, laitteiden käyttö on tilapäisesti hidastunut.6-9
Tämä jättää suuren potentiaalin uusille tekniikoille, kuten bioabsorboituville verisuonitelineille (BVS), jotka voivat parantaa varhaista avoimuutta ja samalla lieventää loppupään ongelmia, kuten stentin restenoosia. Tässä tarkastelussa keskustelemme infrainguinaalisen perifeerisen valtimosairauden erilaisista saatavilla olevista hoidoista ja arvioimme verisuonten stenttien/telineiden tulevaisuutta sekä femoropoplitealissa että polven aluksissa.
STENTING for FEMOROPOPLITEAL DISEASE
Bare Metal Stents
vaikka nykyinen endovaskulaarinen verisuonikäytäntö suosii stentin sijoittamisen välttämistä ensilinjan hoitona edellä kuvattujen seikkojen vuoksi, stentille on edelleen tärkeitä käyttöaiheita, kuten PTA: n jälkeinen jäännösstenoosi ja virtauksen rajoittava dissektio.1 yhdistetyssä ACC / AHA / SCAI / SIR / SVM: ssä ”asianmukaiset Käyttökriteerit” todetaan, että optimaalisessa lääkehoidossa olevilla potilailla stenoottisen FP-taudin endovaskulaarinen stentti sopii claudikaatioon ja kriittiseen raajaiskemiaan (luvut 1a-c).10
kuva 1a. jaksottaisen Claudication-hoidon asianmukaiset käyttöperusteet ohjeellisesta lääketieteellisestä hoidosta huolimatta.
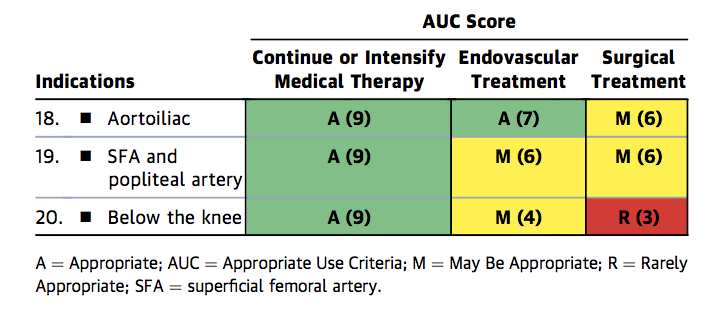
Kuva 1a

kuva 1 b. Appropriate Use Criteria for Critical Limb Ischemia
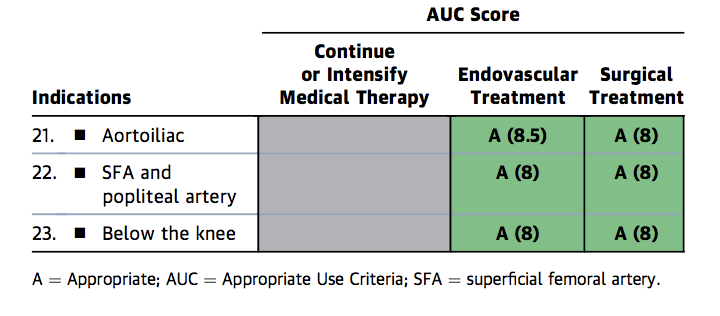
Figure 1b

Figure 1c. Appropriate Use Criteria Device Selection for FP disease
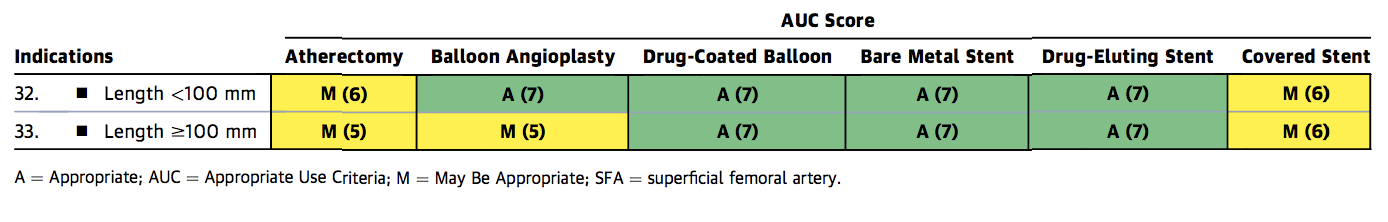
Figure 1c

FP= Femoropopliteal, a = asianmukainen, AUC = asianmukaiset Käyttökriteerit, M = voi olla sopiva, R = harvoin sopiva, SFA = pinnallinen reisivaltimo.
FP= Femoropopliteal, a = asianmukainen, AUC = asianmukaiset Käyttökriteerit, M = voi olla sopiva, R = harvoin sopiva, SFA = pinnallinen reisivaltimo.
the Society for Cardiovascular Angiography and Guidelines luokittelee paljaat metalliset stentit IIA: ksi ja DES: n IA: n suositukseksi FP-taudille.11 the society of vascular surgery guidelines12, 13 on critical limb iskemia (CLI) suosittelee stenttien käyttöä polven alapuolella (BTK).
ensimmäinen laaja tutkimus, jossa vaskulaarista stentingiä verrattiin pelkkään PTA: han, tehtiin Schillingerin ja muiden toimesta vuonna 2006.3 ”as treated”-analyysissä 12 kuukauden primaarinen primääripatenssi oli selvästi korkeampi pelkillä metallisilla stenteillä (63% vs. 37% p=0, 001). Tätä seurasi RESILIENT randomized control trial, jossa bare metal stenting With The Lifestent® to PTA. Tutkimuksessa primääripatenssi parani jälleen 3 vuoden kohdalla (75, 5% vs. 41, 1% p< 0, 001).4
myöhempi SUPERB-Rekisteri arvioi Supra-kudotun nitinolistentin osoittaen primäärisen avoimuuden 86,3% ja nolla stenttimurtumaa.14 pidemmän aikavälin seurantatiedot osoittivat, että 36 kuukauden tavoite-leesion revaskularisaatiovapaa elinaika oli 82%.1 Superstentin julkaisun jälkeen useat yritykset ottivat käyttöön nitinol bare metal stentit, joilla oli myös alhainen stentti murtumanopeus ja hyvä ensisijainen avoimuus. Esimerkiksi täydellinen® itse laajeneva stentti (Medtronic, Minneapolis, MN) osoitti 1 vuoden primaarisen avoimuuden lähes 75% ja nolla stenttimurtumaa femoropopliteal segmenteissä (huomaa: distaalinen popliteal leesiot suljettiin pois).
Lääkeelutustekniikka
Lääkeelutustekniikka oli tärkeä edistysaskel perifeerisen valtimotaudin endovaskulaarisessa hoidossa. Zilver® paklitaxel eluting stent (Cook Medical, Bloomington, IN) tutkittiin Pää-to-head vs. optimaalinen PTA ja paljas metalli stenting tarpeen mukaan. Tutkimus osoitti, että zilver® DES: llä oli parempi 5 vuoden primaaripatenssi (66, 4% vs. 43, 4% p <0, 001). Tätä tutkimusta seurasi IMPERIAL trial, jossa tutkittiin Eluvia™ DES (Boston Scientific, Marlborough, MA) verrattuna Zilveriin®.16 Eluvia™ täytti ennalta määritetyt non-inferiority-kriteerit 1 vuoden kohdalla 88, 5% ja 79, 5%, p, kun non-inferiority < 0, 01. Eluvia™: lla oli myös numeerisesti vähemmän merkittäviä haittatapahtumia 4, 9% verrattuna 9, 0%: iin, p = 0, 098.17
uudet laitteet
laaja valikoima laitteita on kehitteillä, ja joillekin tehdään varhaisvaiheen kokeita alan jäljellä olevien tarpeiden tyydyttämiseksi. Alla kuvataan joitakin tuontiesimerkkejä uudesta tai kehittyvästä teknologiasta.
Bioabsorboituvia Verisuonitelineitä
liuotetaan bioabsorboituvia verisuonitelineitä (BVS) otettiin alun perin käyttöön sepelvaltimoissa. Näitä laitteita ympäröivä alkuinnostus lieveni, kun julkaistiin satunnaistetut absorboivat kokeet, joissa verrattiin absorboitua BVS: ää (Abbott Vascular, Chicago, IL) tavalliseen sepelvaltimotautiin (Kuva 2a).18-20
kuva 2a. absorboi Bioabsorboituva stentti (Abbott Vascular)

Kuva 2a

3 389 potilaalla tehty imukudoksen meta-analyysi osoitti laitteeseen liittyvän tromboosin olevan BVS: llä 2, 3% ja des: llä 0% 3 vuoden kohdalla [HR 3, 79 95% CI 1, 72-8, 36, p = 0, 002).21
ensimmäisen sukupolven BVS: ään liittyvistä huolista huolimatta perifeeristen BVS: ien kehitys näyttää kiihtyvän, kun äskettäin esiteltiin single arm absorbed BTK-pilottitutkimuksen 5-vuotiset tulokset. Tutkimus esiteltiin Vascular InterVentional Advance (VIVA) 2019 meeting22-tapahtumassa ja siinä raportoitiin tulokset 55 raajasta, joita hoidettiin BVS: llä, jotka osoittivat, että haavan täydellinen paraneminen oli 90%. Amputaatioaste oli 0% ja 5 vuoden alusläpimitta lähestyi 75%. Kahden tulevan koitoksen odotetaan lisäävän kenttää: LIFE-BTK satunnaistettu tutkimus, jossa arvioidaan Esprit BVS (Abbott Vascular) verrattuna pelkästään PTA: han, ja Credence BTK-1-tutkimus, joka on Credence BTK-laitteen yhden käsivarren pilottitutkimus (Meril, Gujarat, Intia).
Vascular Tack System
tack endovaskulaarinen järjestelmä (InTack Vascular, Wayne, PA) ovat pieniä, 6 mm pituisia nitinoli-implantteja, joita käytetään lisäystä ja lumen menetystä estävien dissektiosiipien uudelleen asettamiseen (Kuva 2b).
kuva 2b. Tack endovaskulaarinen järjestelmä (courtesy Tack Vascular)
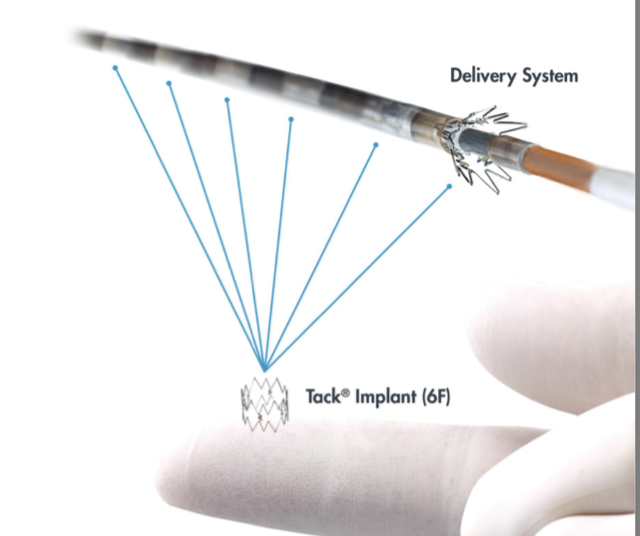
Kuva 2b

div>
näitä laitteita arvioitiin äskettäin julkaistussa yhden hoitoryhmän Toba II-tutkimuksessa, jossa arvioitiin 213 potilasta, jotka saivat Tac-hoitoa PTA: n jälkeen. Tutkimus osoitti 1 vuoden 79,3%: n primaarisen avoimuuden, ja 92,1%: lla leesioista oli täydellinen verisuonten dissektion resoluutio.23 Toba III-yksihaarainen monikeskustutkimus, jossa tarkasteltiin pitkien leesioiden nastoja yhdistettynä lopulliseen hoitoon huumepinnoitetuilla ilmapalloilla, raportoitiin äskettäin Transcatheter Cardiovascular Therapeutics Conferencessa (TCT) vuonna 2019. Tutkimuksessa primääripatenssi oli 95% 12 kuukauden kohdalla. Lisäksi Toba II BTK-tutkimus, jossa tutkittiin laitetta säärisuonissa, esiteltiin Vascular InterVentional Advances (VIVA) 2019-tapahtumassa. Esityksessä haavan paranemisprosentiksi ilmoitettiin 6 kuukautta 73, 8% ja leesion avoimuudeksi 87, 3%.
BioMimics 3D-Pyörrevirtausstentti
3D-pyörrevirtausstentti (Veryan Medical) on kierteinen stentti, joka toimii olettaen, että standardisuorien stenttien aiheuttama alhainen seinämän leikkausjännitys voi lisätä verisuonten restenoosin vaaraa. Pyörrevirtausstenttiä arvioineet eläinmallit ovat osoittaneet neointimaalisen paksuuden vähentyneen merkittävästi (p <0, 001). Laitetta tutkiva MIMICS 2-tutkimus on valmistumassa, ja se pitäisi esitellä lähitulevaisuudessa. Alustavat tulokset (10% potilaista tarvitsi vielä lopullista seurantaa) osoittivat 84%: n olleen 2 vuoden ajan Vapaa kohdeleesion revaskularisaatiosta.24
ChampioNIR®
ChampioNIR® stentti (Medinol Vascular, Tel Aviv, Israel, Kuva 2C) on hybridi itsestään laajeneva stentti, joka koostuu nitinolin säteittäisestä rungosta, jossa on pituussuuntainen polymeerikuituverkko, joka mahdollistaa ”äärettömän” joustavuuden ja tehostetun väsymiskestävyyden. Laite on tällä hetkellä ilmoittautumassa sen ensimmäinen ihmisen tutkimuksessa odotettavissa 3 vuoden seuranta.
2c. ChampioNIR® (Medinol Vascular)

Kuva 2C

johtopäätös
vaskulaarisilla stenteillä ja tukirangoilla on keskeinen rooli perifeerisen valtimotaudin endovaskulaarisessa hoitoalgoritmissa. Uudet laitteet sekä kestävissä että bioabsorboitavissa teknologioissa ovat osoittautuneet lupaaviksi, ja monia tutkitaan aktiivisesti kliinisissä tutkimuksissa. Vaikka koronaarien bioabsorboitavilla teknologioilla on ollut huonompia kliinisiä tuloksia, laitteen iteraatio ja tutkimukset perifeerisessä verisuonistossa antavat mahdollisuuden jatkaa teknologista kasvua.
- Garcia LA, Rosenfield KR, Metzger CD, et al. SUPERB lopullinen 3-vuoden tuloksia käyttäen kudottua nitinol biomimetic Super stent. Katetri Cardiovasc Interv 2017; 89: 1259-67.
- AbuRahma AF. Milloin endovaskulaarisia ja avoimia ohitushoitoja suositellaan femoropopliteal okklusiiviseen sairauteen? Ann Vasc Dis 2018; 11: 25-40.
- Schillinger M, Sabeti S, Loewe C, et al. Pallolaajennus ja nitinolistenttien istuttaminen reisivaltimoon. N Engl J Med 2006;354: 1879-88.
- Laird JR, Katzen BT, Scheinert D, et al. Nitinol – stentti-implantaatio vs. pallolaajennus claudication-potilaiden pinnallisten reisiluun ja proksimaalisten popliteaalisten valtimoiden leesioille: kolmen vuoden seuranta joustavasta satunnaistetusta tutkimuksesta. J Endovasc Toer 2012; 19: 1-9.
- Katsanos K, Spiliopoulos S, Kitrou P, Krokidis M, Karnabatidis D. Risk of death following application of paklitaksel-coated balloons and stents in the femoropopliteal Valtimo of the leg: a systematic review and meta-analysis of randomized controlled trials. J Am Heart Assoc 2018; 7: e011245.
- Schneider PA, Laird JR, Doros G, et al. Mortality not correlated with paklitaksel exposure: an independent patient-level meta-analysis of a drug-coated balloon. J Am Coll Cardiol 2019; 73: 2550-63.
- Ouriel K, Adelman MA, Rosenfield K, et al. Paklitakselilla päällystetyn pallolaajennuksen turvallisuus reisiluun perifeerisen valtimosairauden hoidossa. JACC Cardiovasc Interv 2019; 12: 2515-24.
- Gray WA, Jaff MR, Parikh SA, et al. Mortality assessment of paklitaxel-coated balloons: patient-level meta-analysis of the ILLUMENATE clinical program at 3 years. Levikki 2019;140: 1145-55.
- Secemsky EA, Kundi H, Weinberg I, et al. Eloonjäämisen yhteys femoropopliteal-valtimon revaskularisaatioon lääkkeillä päällystettyjen laitteiden kanssa. JAMA Cardiol 2019; 4: 332-40.
- Bailey SR, Beckman JA, Dao TD, et al. ACC / AHA / SCAI / SIR / SVM 2018 Appropriate use criteria for periferal Artimo intervention. J Am Coll Cardiol 2019; 73: 214-37.
- Feldman DN, Armstrong EJ, Aronow HD, et al. SCAI consensus guidelines for device selection in femoral-popliteal arterial interventions. Katetri Cardiovasc Interv 2018; 92: 124-40.
- Lawrence PF, Gloviczki P. Global vascular guidelines for patients with chronic raaja-threatchemia. J Vasc Surg 2019; 69: 1s-2S.
- Conte MS, Bradbury AW, Kolh P, et al. Global vascular guidelines on the management of chronic raajan uhkaava iskemia. Eur J Vasc Endovasc Surg 2019; 58: S1–109.
- Garcia L, Jaff MR, Metzger C, et al. Wire-interwoven nitinol stent outcome in the pinnallinen reisiluun ja proksimaalisen popliteal valtimot: kahdentoista kuukauden tulokset SUPERB tutkimus. Circ Cardiovasc Interv 2015; 8: e000937.
- Laird JR, Jain A, Zeller T, et al. Nitinolistentin kiinnittyminen pinnalliseen reisivaltimoon ja proksimaaliseen popliteaaliseen valtimoon: kahdentoista kuukauden tulokset täydellisestä SE-monikeskustutkimuksesta. J Endovasc Ther 2014; 21: 202-12.
- Dake MD, Ansel GM, Lottes AE. Zilver PTX RCT-kuolleisuusanalyysi: zilver PTX-lääkeainetta elutoivan stentin pitkäaikaiskuolleisuudessa ei ollut eroa PTA/BMS-arvoon verrattuna. CVIR Endovasc 2019;2: 25.
- Gray WA, Keirse K, Soga Y, et al. Polymeeripäällysteinen paklitakselielutoiva stentti (Eluvia) verrattuna polymeerittömään paklitakselipäällysteiseen stenttiin (Zilver PTX) endovaskulaariseen femoropopliteal-interventioon (IMPERIAL): satunnaistettu, non-inferiority-tutkimus. Lancet 2018;392: 1541-51.
- Stone GW, Ellis SG, Gori T, et al. Blinded outcomes and angina pectoris assessment of coronary bioresorbable scaffolds: 30 päivän ja 1 vuoden tulokset absorbed IV-satunnaistetusta tutkimuksesta. Lancet 2018;392: 1530-40.
- Ali ZA, Serruys PW, Kimura T, et al. 2-year outcomes with the absorbe bioresorbable scaffold for treatment of coronary coronary disease: a systematic review and meta-analysis of seven randomised trials with an individual patient data subtudy. Lancet 2017;390: 760-72.
- Stone GW, Ellis S, Simonton C, et al. Tulokset absorbe bioresorbable verisuonten tukiranka hyvin pieni ja ei kovin pieni sepelvaltimoiden: absorbe III satunnaistettu tutkimus. J Am Coll Cardiol 2016; 67: 35.
- Ali ZA, Gao R, Kimura T, et al. Kolmen vuoden tulokset absorboivat bioresorboituvan telineen avulla: individual-patiente data meta-analysis from the absorbe randomized trials. Levikki 2018;137: 474-79.
- viiden vuoden tulokset absorbe BTK-tutkimuksesta esitetty (endovaskulaarinen Today-sivusto). 2019. Saatavilla: https://evtoday.com/news/five-year-results-from-absorb-btk-trial-presented . Käytetty 02/25/20.
- Gray WA, Cardenas JA, Brodmann M, et al. Femoropopliteal-valtimoiden pallolaajennuksen jälkeinen dissektio Tack-Endovaskulaarisella järjestelmällä: 12 kuukauden tulokset TOBA II-tutkimuksesta. JACC Cardiovasc Interv 2019; 12: 2375-84.
- Swirling Flow®: nature ’ s ideal alternative to drug elution (endovaskulaarinen Today-sivusto). 2019. Available at: https://evtoday.com/articles/2019-sept/swirling-flow-natures-ideal-alternative-to-drug-elution. Accessed 02/25/20.
Clinical Topics: Invasive Cardiovascular Angiography and Intervention, Stable Ischemic Heart Disease, Vascular Medicine, Atherosclerotic Disease (CAD/PAD), Interventions and Vascular Medicine, Chronic Angina
Keywords: Verisuonisairaudet, aneurysma, perifeerinen valtimotauti, katkokävely, Lääkeainestentit, ahtauma, patologiset, paklitakseli, reisivaltimo, United States Food and Drug Administration, sepelvaltimoiden verisuonet, Medicare, ilmaantuvuus, pilottiprojektit, sepelvaltimon restenoosi, seurantatutkimukset
< Back to Listings